
【題目】[化學——選修3:物質結構與性質]氫化鋁鈉(NaAlH4)是一種新型輕質儲氫材料,摻入少量Ti的NaAlH4在150℃時釋氫,在170℃、15.2MPa條件下又重復吸氫。NaAlH4可由AlCl3和NaH在適當條件下合成。NaAlH4的晶胞結構如右下圖所示。

(1)基態Ti原子的價電子軌道表示式為 。
(2)NaH的熔點為800℃,不溶于有機溶劑。NaH屬于 晶體,其電子式為 。
(3)AlCl3在178℃時升華,其蒸氣的相對分子質量約為267,蒸氣分子的結構式為 (標明配位鍵)。
(4)AlH4-中,Al的軌道雜化方式為 ;例舉與AlH4-空間構型相同的兩種離子 (填化學式)。
(5)NaAlH4晶體中,與Na+緊鄰且等距的AlH4-有 個;NaAlH4晶體的密度為 g·cm-3(用含a的代數式表示)。若NaAlH4晶胞底心處的Na+被Li+取代,得到的晶體為 (填化學式)。
(6)NaAlH4的釋氫機理為:每3個AlH4-中,有2個分別釋放出3個H原子和1個Al原子,同時與該Al原子最近鄰的Na原子轉移到被釋放的Al原子留下的空位,形成新的結構。這種結構變化由表面層擴展到整個晶體,從而釋放出氫氣。該釋氫過程可用化學方程式表示為 。
【答案】(1)![]()
(2)離子;![]()
(3) 
(4)sp3 NH4+、BH4(或“SO42”“PO43” 等其他合理答案)
(5)8 (或“
(或“ ![]() ”) Na3Li(AlH4)4
”) Na3Li(AlH4)4
(6)3NaAlH4=Na3AlH6+2Al+3H2↑
【解析】
試題分析:(1)Ti的原子序數為22,電子排布為1s22s22p63s23p63d24s2,價電子排布式為3d24s2,價電子軌道表示式為![]() ;
;
(2)NaH的熔點為800℃,不溶于有機溶劑,屬于離子晶體;NaH是離子化合物,電子式為![]() ;
;
(3)氯化鋁中鋁原子最外層電子只有3個電子,形成3個共價鍵,每個鋁原子和四個氯原子形成共價鍵,且其中一個共用電子對是氯原子提供形成的配位鍵,如圖 ;
;
(4)AlH4-中,Al的價層電子對數=4+![]() =4,所以Al原子為sp3雜化;等電子體的結構相似,所以AlH4-空間構型相同的兩種離子NH4+、BH4-(或“SO42-”“PO43-”);
=4,所以Al原子為sp3雜化;等電子體的結構相似,所以AlH4-空間構型相同的兩種離子NH4+、BH4-(或“SO42-”“PO43-”);
(5)以底面Na+離子研究,與之最近的AlH4-距離為![]() anm,位于同一面的4個頂角以及其余4個側面的面心上,共有8個;根據均攤法可知,晶胞中鈉離子的個數為6×
anm,位于同一面的4個頂角以及其余4個側面的面心上,共有8個;根據均攤法可知,晶胞中鈉離子的個數為6×![]() +4×
+4×![]() =4,晶體的化學式為NaAlH4,所以晶胞中AlH4-的個數為4,該晶胞的質量為
=4,晶體的化學式為NaAlH4,所以晶胞中AlH4-的個數為4,該晶胞的質量為![]() g,該晶胞體積為2a3nm3=2a3×10-21cm3,則該晶胞的密度為
g,該晶胞體積為2a3nm3=2a3×10-21cm3,則該晶胞的密度為 。晶胞中AlH4-的個數為4,鈉離子的個數為4,若NaAlH4晶胞底心處的Na+被Li+取代,則晶胞中AlH4-的個數為4,鈉離子的個數為3,鋰離子的個數為1,晶體的化學式為:Na3Li(AlH4)4;
。晶胞中AlH4-的個數為4,鈉離子的個數為4,若NaAlH4晶胞底心處的Na+被Li+取代,則晶胞中AlH4-的個數為4,鈉離子的個數為3,鋰離子的個數為1,晶體的化學式為:Na3Li(AlH4)4;
(6)NaAlH4的釋氫機理為:每3個AlH4-中,有2個分別釋放出3個H原子和1個Al原子,同時與該Al原子最近鄰的Na原子轉移到被釋放的Al原子留下的空位,即產物有Al、H2和AlH63-,方程式為3NaAlH4=Na3AlH6+2Al+3H2↑。


 口算能手系列答案
口算能手系列答案科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A.CS2是極性鍵構成的極性分子
B.SO2與CO2為等電子體
C.金屬晶體的六方最密堆積和面心立方最密堆積的方式空間利用率最高
D.1molNaHSO4熔融態時有3mol離子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表為元素周期表的一部分,請參照元素①-⑨在表中的位置,回答問題:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)表中用于半導體材料的元素在周期表中的位置是__________________。
(2)③、④、⑧的原子半徑最小是___________________(用元素符號回答)。
(3)⑤、⑥、⑦的最高價氧化物對應的水化物,堿性最強的是__________(用化學式回答)。
(4)②、③、④的氣態氫化物,穩定性最強的是__________(用結構式回答
(5)②和③按原子數1:2形成的化合物的電子式為____________,該晶體氣化的過程中克
服的微粒間作用力為_______________________。
(6)③和⑧形成的化合物屬于_______________(填“離子化合物”或“共價化合物”),該晶體屬于________晶體(填“離子”、“分子”、“原子”)。
(7)元素⑤、⑦的最高價氧化物的水化物互相反應的化學方程式為:___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列變化中,一定需加還原劑才能實現的是( )
A. CO2 → CO32- B. FeCl3 → FeCl2 C. C → CO2 D. HCl → MgCl2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】近年我國汽車擁有量呈較快增長趨勢,汽車尾氣已成為重要的空氣污染物。回答下列問題:
(l)汽車發動機工作時會引起反應:N2(g)+O2(g)![]() 2NO(g),是導致汽車尾氣中含有NO的原因之一。2000K時,向容積為2L的密閉容器中充入2molN2與2molO2,發生上述反應,經過5min達到平衡,此時容器內NO的體積分數為0.75% .則該反應在5min內的平均反應速率v(O2)=_______mol/(Lmin),N2的平衡轉化率為_______,2000K時該反應的平衡常數K=_____。
2NO(g),是導致汽車尾氣中含有NO的原因之一。2000K時,向容積為2L的密閉容器中充入2molN2與2molO2,發生上述反應,經過5min達到平衡,此時容器內NO的體積分數為0.75% .則該反應在5min內的平均反應速率v(O2)=_______mol/(Lmin),N2的平衡轉化率為_______,2000K時該反應的平衡常數K=_____。
(2)一定量NO發生分解的過程中,NO的轉化率隨時間變化的關系如右圖所示。

① 反應2NO(g)![]() N2(g)+O2(g)為______反應(填“吸熱”或“放熱”) ;
N2(g)+O2(g)為______反應(填“吸熱”或“放熱”) ;
②一定溫度下,能夠說明反應2NO(g)![]() N2(g)+O2(g)已達到平衡的是_____(填序號);
N2(g)+O2(g)已達到平衡的是_____(填序號);
a.容器內的壓強不發生變化
b.混合氣體的密度不發生變化
c. 2NO、N2、O2的濃度保持不變
d.單位時間內分解4molNO,同時生成2molN2
③ 在四個容積和溫度均完全相同的密閉容器中分別加入下列物質,相應物質的量(mol)如下表所示。相同條件下達到平衡后,N2的體積分數最大的是_______(填容器代號);
容器代號 | NO | N2 | O2 |
A | 2 | 0 | 0 |
B | 0 | l | l |
C | 0.4 | 0.6 | 0.8 |
D | l | 0.5 | 0.4 |
(3)當發動機采用稀薄燃燒時,尾氣中的主要污染物為NOx。可用CH4催化還原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ·mol-1
①寫出CH4與NO反應生成N2、CO2、H2O(g)的熱化學方程式:___________;
②使用催化劑可以將汽車尾氣的主要有害成分一氧化碳(CO)和氮氧化物(NOx)轉化為無毒氣體,該反應的化學方程式為___________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. Si有導電性,可用于制備光導纖維
B. Na2O2能與CO2反應,可用作呼吸面具的供氧劑
C. 硅膠常用作實驗室和食品、藥品等的干燥劑,也可作催化劑載體
D. 小蘇打是一種膨松劑,可用于制作饅頭和面包
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】等電子體之間具有相似的結構和化學鍵類型。根據等電子原理,由短周期元素組成的粒子,只要其原子總數和原子最外層電子總數相同,均可互稱為等電子體.下列各組粒子不能互稱為等電子體的是
A.CO32-和NO3- B.O3和SO2
C.CO2和NO2- D.SCN-和N3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業生產中產生的SO2、NO直接排放將對大氣造成嚴重污染.利用電化學原理吸收SO2和NO,同時獲得 Na2S2O4和 NH4NO3產品的工藝流程圖如下(Ce為鈰元素).
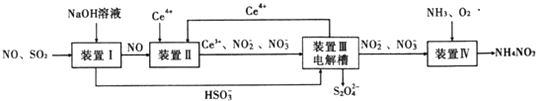
請回答下列問題.
(1)裝置Ⅱ中NO在酸性條件下生成NO2-的離子方程式__________________;
(2)含硫各微粒(H2SO3、HSO3-和SO32-)存在于SO2與NaOH溶液反應后的溶液中,它們的物質的量分數ω與溶液pH的關系如圖1所示

①下列說法正確的是 (填標號)。
A.pH=7時,溶液中c( Na+)<c (HSO3-)+c(SO32-)
B.由圖中數據,可以估算出H2SO3的第二級電離平衡常數Ka2≈10-7
C.為獲得盡可能純的 NaHSO3,應將溶液的pH控制在 4~5為宜
D.pH=9時溶液中c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3)
②若1L1mol/L的NaOH溶液完全吸收13.44L(標況下)SO2,則反應的總離子方程式為 。
③取裝置Ⅰ中的吸收液vmL,用cmol/L的酸性高錳酸鉀溶液滴定。酸性高錳酸鉀溶液應裝在 (填“酸式”或“堿式”)滴定管中,判斷滴定終點的方法是 。
(3)裝置Ⅲ 的作用之一是再生Ce4+ ,其原理如下圖所示。

圖中A為電源的 (填“正”或“負”)極。右側反應室中發生的主要電極反應式為 。
(4) 已知進入裝置Ⅳ的溶液中NO-2的濃度為 0.4 mol/L ,要使 1m3該溶液中的NO-2完全轉化為 NH4NO3,需至少向裝置Ⅳ中通入標準狀況下的 O2的體積為 L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com