
 .
. ,元素D在元素周期表中的位置是第三周期VIIA族.
,元素D在元素周期表中的位置是第三周期VIIA族.分析 地殼中含量最高的元素是O元素,故A為O,D的氫化物和最高價氧化物對應的水化物均為強酸,應為Cl元素,B、C、D的最高價氧化物的水化物兩兩混合均能發生反應生成鹽和水,則C為Al元素,B為Na元素,E的原子數序最大,且位于20號元素之內,E和其他元素既不在同一周期也不在同一主族,應為Ca元素,根據對應原子結構特點以及對應單質、化合物的性質解答該題即可.
解答 解:地殼中含量最高的元素是O元素,故A為O,D的氫化物和最高價氧化物對應的水化物均為強酸,應為Cl元素,B、C、D的最高價氧化物的水化物兩兩混合均能發生反應生成鹽和水,則C為Al元素,B為Na元素,E的原子數序最大,且位于20號元素之內,E和其他元素既不在同一周期也不在同一主族,應為Ca元素,
綜上所述:A為O、B為Na、C為Al、D為Cl、E為Ca,
(1)氧氣單質中兩個O原子形成2對共價鍵,故結構式為O=O,Na的最高價氧化物的水化物為氫氧化鈉,氫氧化鈉屬于離子化合物,電子式中需要標出陰陽離子所帶電荷,鈉離子直接用離子符號表示,氫氧根離子需要標出最外層電子,氫氧化鈉的電子式為: ,故答案為:O=O;
,故答案為:O=O; ;
;
(2)由于H2O分子間存在氫鍵,其沸點高于HCl,故答案為:H2O;
(3)E為Ca,有4個電子層,最外層電子數為2,失去最外層2個電子形成陽離子,離子結構示意圖為: ,Cl的原子核外有3個電子層,最外層電子數為7,則位于第三周期VIIA族,故答案為:
,Cl的原子核外有3個電子層,最外層電子數為7,則位于第三周期VIIA族,故答案為: ;第三周期VIIA族;
;第三周期VIIA族;
(4)鈣、氯、氧可形成Ca(ClO)2、Ca(ClO3)2、Ca(ClO4)2,其中滿足題設條件下的鹽為Ca(ClO)2(次氯酸鈣),由于在酸性環境中ClO-具有強氧化性,Cl-具有還原性,二者發生氧化還原反應生成Cl2和H2O,離子反應為ClO-+Cl-+2H+═Cl2↑+H2O,
故答案為:次氯酸鈣;ClO-+2H++Cl-═Cl2↑+H2O.
點評 本題考查元素的推斷,為高頻考點,側重于學生的分析能力的考查,題目難度中等,以此為載體,考查了結構式、電子式的書寫,離子化合物的形成過程,離子結構示意圖、離子反應方程式書寫等,綜合性較強,注意整理.


 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1:1 | B. | 2:1 | C. | 2:3 | D. | 1:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等物質的量的CaCl2和CaO2含有的離子數 | |
| B. | 等溫等壓下,質子數相等的CO、N2、C2H2三種氣體含有的原子數 | |
| C. | 同溫、同壓、同體積的CO和NO含有的質子數 | |
| D. | 物質的量相同的鐵和鋁分別與足量氯氣完全反應時轉移的電子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 需要加熱的反應一定是吸熱反應 | |
| B. | 放熱反應在常溫下一定很容易發生 | |
| C. | 化學鍵的斷裂和形成是化學反應中能量變化的主要原因 | |
| D. | 伴隨能量變化的物質變化都是化學變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | B. | 3Cu+8HO3(濃)=3Cu(NO3)2+2NO↑+4H2O | ||
| C. |  | D. | 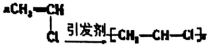 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬原子失去電子越多,還原性越強 | |
| B. | 鹽酸酸化的高錳酸鉀溶液氧化性更強 | |
| C. | 工業上鎂鋁單質都是電解對應熔融的氯化物得到的 | |
| D. | 強氧化劑與強還原劑不一定能發生氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O2與水反應:Na2O2+H2O=2Na++2OH-+O2↑ | |
| B. | 用惰性電極電解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | 硫酸亞鐵溶液中加入酸化的雙氧水:2Fe2++2H++H2O2=2Fe3++2H2O | |
| D. | Ba(OH)2溶液中加入過量的NaHSO4溶液:Ba2++SO42-+OH-+H+=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com