
【題目】下表是實驗室制備氣體的有關內容:
編號 | 實驗內容 | 實驗原理 |
① | 制氧氣 | H2O2→O2 |
② | 制氨氣 | NH4Cl→NH3 |
③ | 制氯氣 | HCl→Cl2 |
(1)上述氣體中:從制備過程看,必須選擇合適的氧化劑才能實現的是_________(填氣體的化學式,下同);從反應中有無電子轉移的角度看,明顯不同于其他氣體的是______,寫出實驗室制取該氣體的化學方程式_______________________________
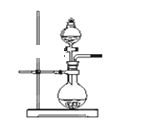
(2)若用上述裝置制備NH3,則選擇的試劑為____________________。
(3)制備Cl2需用8 mol/L的鹽酸100mL,現用12 mol/L的鹽酸來配制。
①需要12 mol/L的鹽酸的體積為__________mL(精確到0.1 mL)
②在容量瓶的使用方法中,下列操作不正確的是_______________(填寫標號)。
A.使用容量瓶前檢查它是否漏水
B.容量瓶用蒸餾水洗凈后,再用待配溶液潤洗
C.配制溶液時用量筒量取濃鹽酸后用玻璃棒引流入容量瓶中,緩慢加入蒸餾水到接近標線1cm~2cm處,用膠頭滴管滴加蒸餾水直到凹液面的最低處和標線相平
D.定容后蓋好瓶塞,用食指頂住,用另一只手手指托住瓶底,把容量瓶倒轉和搖動多次
【答案】Cl2 NH3 Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O 濃氨水和生石灰(或氫氧化鈉或堿石灰) 66.7mL BC
CaCl2+2NH3↑+2H2O 濃氨水和生石灰(或氫氧化鈉或堿石灰) 66.7mL BC
【解析】
(1)反應①為分解反應,不需另加氧化劑;反應②為非氧化還原反應;反應③制備氯氣的反應,HCl中的Cl化合價升高,HCl作還原劑,反應需要額外加入氧化劑,。答案為Cl2。
反應①、③為氧化還原反應,有電子轉移;反應②為非氧化還原反應,無電子轉移。明顯不同于其他氣體的是NH3。答案為NH3;
實驗室用氯化銨和熟石灰反應制取氨氣,反應的化學方程式為
Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O 答案為Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O 答案為Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(2)若用圖中不需加熱的裝置制備NH3,可選擇濃氨水和生石灰(或氫氧化鈉或堿石灰),利用生石灰(或氫氧化鈉或堿石灰)吸水放熱的特點制備氨氣。答案為:濃氨水和生石灰(或氫氧化鈉或堿石灰);
(3) ①利用稀釋前后溶液的物質的量相等建立等量關系式
需要12 mol/L的鹽酸的體積為![]() 答案為66.7mL
答案為66.7mL
②A.使用容量瓶前檢查它是否漏水,正確;
B.容量瓶用蒸餾水洗凈后,再用待配溶液潤洗,必然產生誤差,錯誤;
C.配制溶液時用量筒量取濃鹽酸后用玻璃棒引流入容量瓶中,此操作錯誤,因為溶質必須放入燒杯內加水溶解,不能直接放入容量瓶內;
D.定容后蓋好瓶塞,用食指頂住,用另一只手手指托住瓶底,把容量瓶倒轉和搖動多次,正確;
故答案為BC。


科目:高中化學 來源: 題型:
【題目】關于氫鍵,下列說法正確的是
A. 分子中有N、O、F原子,分子間就存在氫鍵
B. 因為氫鍵的緣故,![]() 比
比![]() 熔沸點高
熔沸點高
C. 由于氫鍵比范德華力強,所以H2O分子比H2S分子穩定
D. “可燃冰”——甲烷水合物(例如:8CH4·46H2O)中CH4與H2O之間存在氫鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鎵(Ga)、鍺( Ge)、砷(As)、硒(Se)均為第四周期的元素,它們在高科技尖端科學特別是信息領域有著廣泛的用途。試回答下列問題:
(1)基態鍺原子的價電子排布圖為_____。
(2)沸點:NH3_______AsH3(填“>”、“<”或“=”),原因是____________。
(3)H2SeO4和H2SeO3是硒的兩種含氧酸,請根據結構與性質的關系,解釋H2SeO4比H2SeO3 酸性強的原因________。
(4)砷化鎵可由(CH3)3Ga和AsH3在700℃下反應制得,同時得到一種最簡單的有機物,寫出該反應的方程式為_____;砷化鎵的晶胞結構如下圖所示,其晶胞邊長為a pm(1pm=10-12m),則每立方厘米該晶體中所含砷元素的質量為_____g(用NA表示阿伏加德羅常數的值)。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧化鎂在醫藥、建筑等行業應用廣泛。硫酸鎂還原熱解制備高純氧化鎂是一種新的探索。以菱鎂礦(主要成分為MgCO3,含少量FeCO3 )為原料制備高純氧化鎂的實驗流程如下:

(1)MgCO3 與稀硫酸反應的化學方程式為__________________________。
(2)加入H2O2 氧化時,發生反應的離子方程式為__________________________。
(3)濾渣2 的成分是____________(填化學式)。
(4)煅燒過程存在以下反應:
2MgSO4+C![]() 2MgO+2SO2↑+CO2↑ MgSO4+C
2MgO+2SO2↑+CO2↑ MgSO4+C![]() MgO+SO2↑+CO↑ MgSO4+3C
MgO+SO2↑+CO↑ MgSO4+3C![]() MgO+S↑+3CO↑
MgO+S↑+3CO↑
利用下圖裝置對煅燒產生的氣體進行分步吸收或收集。

①D中通過排水法收集的氣體可以是___________(填化學式)。
②C中溶液用于吸收CO2,B中盛放的溶液可以是___________(填字母)。
a.NaOH 溶液 b.Na2CO3 溶液 c.稀硝酸 d.KMnO4溶液
③A中得到的淡黃色固體與熱的NaOH溶液反應,產物中元素最高價態為+4,寫出該反應的離子方程式:______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】解釋下列事實的方程式正確的是
A.用碳酸鈉溶液處理水垢中的硫酸鈣:Ca2++CO32-=CaCO3↓
B.SO2使紫色石蕊溶液變紅色:SO2+H2O=2H++SO32-
C.用石墨電極電解AlCl3溶液,陰極附近生成沉淀:2Al3++6H2O+6e- =2Al(OH)3↓+3H2↑
D.工業上制取硅:SiO2+C![]() Si+CO2
Si+CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】蘋果醋是一種由蘋果發酵而形成的具有解毒、降脂、減肥等明顯藥效的健康食品。蘋果酸(2-羥基丁二酸)是這種飲料的主要酸性物質,蘋果酸的結構簡式為![]() 。下列相關說法不正確的是 ( )。
。下列相關說法不正確的是 ( )。
A.蘋果酸能發生酯化反應的官能團有3個
B.蘋果酸在一定條件下能發生催化氧化反應
C.1 mol蘋果酸與足量Na反應生成33.6 L H2
D.1 mol蘋果酸與NaHCO3溶液反應,最多消耗2 mol NaHCO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“封管實驗”具有簡易、方便、節約、綠色等優點,下列關于三個“封管實驗”(夾持裝置未畫出)的說法正確的是( )

A. 加熱時,①中上部匯集了NH4Cl固體
B. 加熱時,②中溶液變紅,冷卻后又都變為無色
C. 加熱時,③中溶液紅色褪去,冷卻后溶液變紅,體現SO2的漂白性
D. 三個“封管實驗”中所發生的化學反應都是可逆反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高錳酸鉀是錳的重要化合物和常用的氧化劑。以下是工業上用軟錳礦制備高錳酸鉀的一種工藝流程:
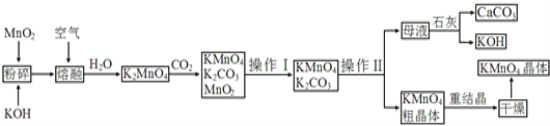
(1) KMnO4稀溶液是一種常用的消毒劑。其消毒原理與下列_____物質相似。
A.75%酒精 B.雙氧水 C.苯酚 D.“84”消毒液(NaClO溶液)
(2)操作Ⅰ的名稱是________;操作Ⅱ是根據KMnO4和K2CO3兩物質在__________ (填性質)上差異,采用 __________(填操作步驟)、趁熱過濾得到KMnO4粗晶體的。
(3)上述流程中可以循環使用的物質有石灰、CO2、____和____ (寫化學式)。
(4) 向K2MnO4溶液中通入CO2以制備KMnO4,該反應中的還原劑是_______。
(5) 鉍酸鈉(NaBiO3,不溶于水)用于定性檢驗酸性溶液中Mn2+的存在(鉍元素的還原產物為Bi3+,Mn的氧化產物為+7價),寫出反應的離子方程式:__________________。
(6) 寫出MnO2、KOH的熔融混合物中通入空氣時發生的主要反應的化學方程式:________________。
(7)若不考慮物質循環與制備過程中的損失,則1mol MnO2可制得_____mol KMnO4。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是
A. 甲酸與碳酸鈉溶液反應:2H++CO32-=CO2↑+H2O
B. 醋酸溶液與Cu(OH)2:2CH3COOH+Cu(OH)2=Cu2++2CH3COO-+2H2O
C. 苯酚鈉溶液通少量CO2 :2C6H5O-+CO2+H2O→2C6H5OH+CO32-
D. 甲醛溶液與足量的銀氨溶液共熱:HCHO +4Ag(NH3)2++4OH-![]() CO32-+2NH4++4Ag↓ +6NH3+2H2O
CO32-+2NH4++4Ag↓ +6NH3+2H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com