
下列圖示中,A為一種常見的單質,B、C、D、E是含A元素的常見化合物,它們的焰色反應均為黃色。

填寫下列空白:
(1)寫出化學式:A________,B_________,D_________E_______。
(2)以上反應中不屬于氧化還原反應的有______________(填序號)。
(3)寫出反應②④⑥的化學方程式:
②_______________________________。
④_______________________________。
⑥_______________________________。
(4)寫出反應⑤的離子方程式:_____________________,寫出鋁粉和C溶液反應的離子方程式:___________________
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源:2015-2016學年遼寧省高一上學期期末考試化學試卷(解析版) 題型:選擇題
用NA表示阿伏加德羅常數的值。下列說法正確的是
A.7.1gCl2與足量的氫氧化鈉溶液反應轉移的電子數一定為0.2NA
B.在常溫常壓下,11.2 升氯氣含有的分子數為0.5NA
C.常溫常壓下,32 g O2和O3的混合氣體所含原子數為2NA
D.1 molFe與足量的Cl2反應轉移的電子數為2NA
查看答案和解析>>
科目:高中化學 來源:2016屆黑龍江省高三上12月月考化學試卷(解析版) 題型:選擇題
在生產、生活中為增大反應速率而采取的措施合理的是
A.食物放在冰箱中
B.塑料制品中添加抑制劑
C.在糕點包裝內放置小包除氧劑
D.燃煤發電時用煤粉代替煤塊
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高二上12月月考化學試卷(解析版) 題型:選擇題
用惰性電極電解下列物質的水溶液時,在陽極上不生成O2的是( )
A.NaOH B.H2SO4 C.ZnCl2 D.Na2SO4
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省邯鄲市高二上學期第三次月考化學試卷(解析版) 題型:選擇題
含有一個碳碳三鍵的炔烴,與氫氣充分加成后的產物的結構簡式為:
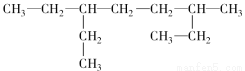 ,此炔烴可能的結構有( )
,此炔烴可能的結構有( )
A.1種 B.2種 C.3種 D.4種
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省衡水市高一上第四次月考化學試卷(解析版) 題型:選擇題
加入適量的H2SO4溶液,可使下列離子在溶液中的數目顯著減少的是
A.Cl- B.NO3- C.Na+ D.CO32-
查看答案和解析>>
科目:高中化學 來源:2015-2016學年廣西欽州港經濟開發區中學高二上12月月考化學試卷(解析版) 題型:填空題
空氣污染監測儀是根據SO 2 與Br 2 的定量反應測定空氣中SO 2 的含量:SO 2 +Br 2 + 2H 2 O==H 2 SO 4 +2HBr,上述反應的溴,來自一個裝滿酸性KBr溶液的電解槽陽極上的氧化反應。電解槽的陰、陽極室是隔開的。當測空氣中SO 2 的含量時,空氣(經過除塵)以1.5×10 - 4 m 3·min - 1 的流速進入電解槽的陽極室,電流計顯示每秒通過的電子是8.56×10 - 1 1mol時,此條件下能保持溴濃度恒定,并恰與SO 2 完全反應(設被測空氣中不含與溴反應的物質)。
(1)寫出監測過程中主要發生的化學反應方程式;_______________________。
(2)計算空氣中SO 2 的含量(g·m - 3 空氣)。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一上學期12月月考化學試卷(解析版) 題型:選擇題
下列關于鈉的敘述正確的是
A.鈉在空氣中露置會立刻被空氣氧化成過氧化鈉
B.鈉單質具有強還原性,可將銅從其鹽溶液中置換出來
C.鈉與鈉離子都具有強的還原性
D.鈉與稀鹽酸反應的實質是與氫離子的反應
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省高三上1月階段測理綜化學試卷(解析版) 題型:填空題
礦物燃料在使用的過程中會產生大量污染性物質,如SO2和CO2,而H2和NH3都被認為是理想的清潔能源。
(1)某些合金可用于儲存氫,金屬儲氫的原理可表示為:M(s)+xH2═MH2x(s)△H<0(M表示某種合金)如圖1表示溫度分別為T1、T2時,最大吸氫量與氫氣壓強的關系.則下列說法中,正確的是___________;
a.T1>T2
b.增大氫氣壓強,加快氫氣的吸收速率
c.增大M的量,上述平衡向右移動
d.上述反應可實現多次儲存和釋放氫氣
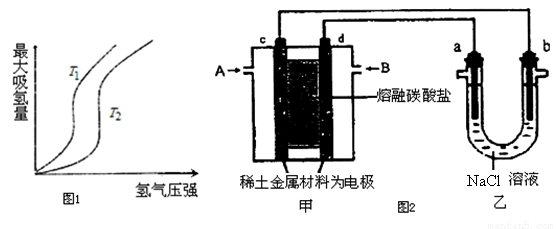
(2)以熔融碳酸鹽為電解質,稀土金屬材料為電極組成氫氧燃料電池(如圖2裝置甲所示),其中負極通入H2,正極通入O2和CO2的混合氣體.圖2乙裝置中a、b為石墨電極,電解一段時間后,b電極附近滴入酚酞溶液變紅,NaCl溶液的體積為100mL。
①工作過程中,甲裝置中d電極上的電極反應式是________________;乙裝置中電極a為_______極(填電極名稱)。
②若在a極產生112mL(標準狀況)氣體,25℃時乙裝置中所得溶液pH=__________。(忽略電解前后溶液的體積變化)
(3)氨在氧氣中燃燒,生成水和一種空氣組成成分的單質.
已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ•mol-1 2H2(g)+O2(g)═2H2O(1)△H=-572KJ•mo1-1試寫出氨氣在氧氣中燃燒生成液態水的熱化學方程式________________;
(4)在一定條件下,將lmolN2和3molH2混臺于一個10L的密閉容器中發生反應:
N2(g)+3H2(g) 2NH3(g)△H<0 已知5分鐘后達到平衡,平衡時氨氣的體積分數為25%。
2NH3(g)△H<0 已知5分鐘后達到平衡,平衡時氨氣的體積分數為25%。
①該反應的平衡常數表達式為:K=______________;
②能判斷該反應是否達到化學平衡狀態的依據是____________
a、容器中壓強不變 b、混合氣體的密度不變 c、3v正(H2)=2v逆(NH3) d、c(N2): c(H2): c(NH3)=1:3:2
③對于上述平衡狀態,改變下列條件能使反應速率增大,且平衡向正向移動的___________
a、選用更高效的催化劑 b、升高溫度 c、及時分離出氨氣
d、增加H2的濃度 e、充入He,使體系總壓強增大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com