
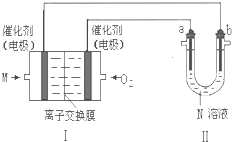
 A、B、C、D、E為短周期元素,且原子序數依次遞增.其中B元素形成化合物種類最多,A、E同主族.A與 E的質子數之和是B質子數的2倍,且E與D分別形成的最簡單離子都含有10個電子.由以上元素組成的物質BD和C2具有相同的電子數.
A、B、C、D、E為短周期元素,且原子序數依次遞增.其中B元素形成化合物種類最多,A、E同主族.A與 E的質子數之和是B質子數的2倍,且E與D分別形成的最簡單離子都含有10個電子.由以上元素組成的物質BD和C2具有相同的電子數.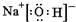 ,故答案為:
,故答案為: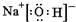 ;
;

 53隨堂測系列答案
53隨堂測系列答案科目:高中化學 來源: 題型:
| A、向某溶液中加入稀鹽酸,產生能使石灰水變渾濁的氣體,該溶液一定含有CO32- |
| B、向某溶液中滴加氯水后,滴加KSCN溶液,溶液呈紅色,該溶液中一定含有Fe2+ |
| C、向某溶液中加入氯化鋇溶液,產生不溶于稀鹽酸白色沉淀,該溶液一定含有SO42- |
| D、往某溶液中加入NaOH,微熱,產生能使濕潤的紅色石蕊試紙變藍的氣體,該溶液中一定含有NH4+ |
查看答案和解析>>
科目:高中化學 來源: 題型:
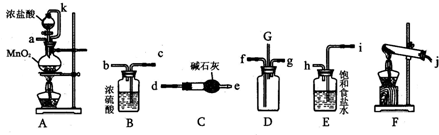
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗步驟 | 預期現象和結論 |
| 步驟1:用試管取樣品溶液2~3mL,再用滴管取 | 若出現血紅色,則假設1成立; 若未出現血紅色,則假設2或假設3成立. |
| 步驟2: | 結合步驟1的現象和結論, |
查看答案和解析>>
科目:高中化學 來源: 題型:
 有A、B、C、D、E、F六種短周期元素,其元素特征信息如表:
有A、B、C、D、E、F六種短周期元素,其元素特征信息如表:| 元素編號 | 元素特征信息 |
| A | A的單質是密度最小的物質 |
| B | B的單質能與冷水劇烈反應,所得強堿性溶液中含有兩種電子數相同的陰、陽離子 |
| C | C的原子最外層電子數是其內層電子數的三倍 |
| D | D與B同周期,該周期中D的簡單離子半徑最小 |
| E | B、C、E組成的36電子的化合物Y是家用消毒劑的主要成分 |
| F | F元素最高正價與最低負價的代數和為4 |
查看答案和解析>>
科目:高中化學 來源: 題型:
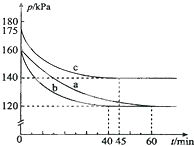 化合物AX3和單質X2在一定條件下反應可生成化合物AX5.回答下列問題:
化合物AX3和單質X2在一定條件下反應可生成化合物AX5.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
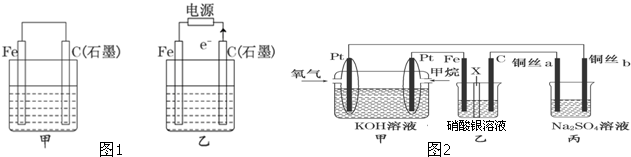
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com