
【題目】有X、Y、Z、W四種短周期元素,原子序數依次增大,其核電荷數總和為38.Y元素原子最外層電子數占核外總電子數的 ![]() ;W元素原子最外層電子比同周期Z元素多5個電子;W和Y不屬同一主族.
;W元素原子最外層電子比同周期Z元素多5個電子;W和Y不屬同一主族.
(1)寫出元素符號:X , Y , Z , W .
(2)Z、W兩元素最高價氧化物對應水化物反應的方程式是 .
(3)把Z的單質(片狀)放入滴有酚酞的沸水中,觀察到的現象是 , 反應的化學方程式是 .
【答案】
(1)H;O;Mg;Cl
(2)Mg(OH)2+2HClO4=Mg(ClO4)2+2H2O
(3)有氣泡、變紅;Mg+2H2O ![]() Mg(OH)2+H2↑
Mg(OH)2+H2↑
【解析】解:(1)Y元素原子最外層電子數占核外總電子數的3/4,判斷出Y為O元素.設X、Y、Z、W的核電核數分別為x、y、z、w,則x+y+z+w=38,x<y,y=8,z>y,w=z+5<18,w≠16 即x<8,x+2z=25,8<z<13,z≠11.①假設x=1則z=12(合理);②假設x=2,則z=23/2(舍去);③假設x=3,則z=11(舍去);④假設x=4,則z=21/2(舍去); ⑤假設x=5,則z=10(舍去);⑥假設x=6,則z=19/2(舍去);⑦假設x=7,則z=9(舍去).故X為H元素,Z為Mg元素,W為Cl元素,所以答案是:H; O; Mg; Cl;(2)Mg、Cl兩元素最高價氧化物對應水化物分別是氫氧化鎂和高氯酸,反應生成高氯酸鎂和水,反應方程式為Mg(OH)2+2HClO4=Mg(ClO4)2+2H2O,所以答案是:Mg(OH)2+2HClO4=Mg(ClO4)2+2H2O;(3)Mg和沸水反應置換出H2且生成堿Mg(OH)2 , 故反應的現象為有氣泡、溶液變紅.反應的方程式為Mg+2H2O ![]() Mg(OH)2+H2↑, 所以答案是:有氣泡、變紅;Mg+2H2O
Mg(OH)2+H2↑, 所以答案是:有氣泡、變紅;Mg+2H2O ![]() Mg(OH)2+H2↑.
Mg(OH)2+H2↑.


 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案科目:高中化學 來源: 題型:
【題目】有機物A由碳、氫、氧三種元素組成。現取2.3 g A與2.8 L氧氣(標準狀況)在密閉容器中燃燒,燃燒后生成二氧化碳、一氧化碳和水蒸氣(假設反應物沒有剩余)。將反應生成的氣體依次通過濃硫酸和堿石灰,濃硫酸增重2.7 g,堿石灰增重2.2 g。回答下列問題:
(1)2.3 g A中所含氫原子、碳原子的物質的量分別是n(H)=______mol;n(C)=_______mol
(2)該有機物的分子式_____________,寫出所有可能結構簡式____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室中需要配制2mol/L的NaCl溶液950mL,配制時應選用的容量瓶的規格和稱取的NaCl的質量分別是( )
A.950 mL 111.2 g
B.500 mL 117 g
C.1 000 mL 117 g
D.任意規格 111.2 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,集氣瓶內充滿某混合氣體(括號內為體積比),若將滴管內的水擠入集氣瓶后,燒杯中的水會進入集氣瓶,則集氣瓶中的混合氣體可能是( ) ①CO、O2(2:1)②NH3、O2(8:1)③NO2、O2(4:1)④N2、H2(1:3)
A.①②
B.②③
C.②④
D.③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿性硼化釩(VB2)—空氣電池工作時反應為:4VB2+ 11O2= 4B2O3+ 2V2O5。用該電池為電源,選用惰性電極電解硫酸銅溶液,實驗裝置如圖所示。當外電路中通過0.04mol電子時,B裝置內共收集到0.448L氣體(標準狀況),則下列說法正確的是
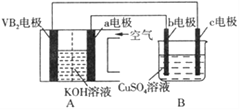
A. VB2電極發生的電極反應為:2VB2+ 11H2O - 22e-= V2O5+ 2B2O3+ 22H+
B. 外電路中電子由c電極流向VB2電極
C. 電解過程中,c電極表面先有紅色物質析出,b電極有氣泡產生
D. 若B裝置內的液體體積為200 mL,則CuSO4溶液的物質的量濃度為0.1mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某校化學實驗興趣小組在“探究鹵素單質的氧化性”的系列實驗中發現:在足量的稀氯化亞鐵溶液中,加入1~2滴溴水,振蕩后溶液呈黃色.
(1)提出問題:Fe3+、Br2哪個氧化性更強? 猜想:①甲同學認為氧化性:Fe3+>Br2 , 故上述實驗現象不是發生氧化還原反應所致,則溶液呈黃色是含(填化學式,下同)所致.
②乙同學認為氧化性:Br2>Fe3+ , 故上述現象是發生氧化還原反應所致,則溶液呈黃色是含所致.
(2)設計實驗并驗證丙同學為驗證乙同學的觀點,選用下列某些試劑設計出兩種方案進行實驗,并通過觀察實驗現象,證明了乙同學的觀點是正確的. 供選用的試劑:a、酚酞試液 b、CCl4 c、無水酒精 d、KSCN溶液.
請你在表中寫出丙同學選用的試劑及實驗中觀察到得現象.
選用試劑(填序號) | 實驗現象 | |
方案1 | ||
方案2 |
(3)結論 氧化性:Br2>Fe3+ . 故在足量的稀氯化亞鐵溶液中,加入1~2滴溴水,溶液呈黃色所發生的離子反應方程式為 .
(4)實驗后的思考 ①根據上述實驗推測,若在溴化亞鐵溶液中通入氯氣,首先被氧化的離子是 .
②在100mLFeBr2溶液中通入2.24LCl2(標準狀況),溶液中有 ![]() 的Br﹣被氧化成單質Br2 , 則原FeBr2溶液的物質的量濃度為 .
的Br﹣被氧化成單質Br2 , 則原FeBr2溶液的物質的量濃度為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列為元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
關于已知元素C、N、S和未知的元素X、Y、Z,回答下列問題:
(1)Z元素在周期表中的位置為______________。
(2)表中元素原子半徑最大的是______________ (寫元素符號)。
(3)①S與Z可形成化合物S2Z2,寫出它的電子式______________。
②C、N、S三元素形成的陰離子常用于檢驗Fe3+的存在,寫出它的結構式______________。
(4)銅與一定濃度的硝酸和硫酸的混合酸反應,生成的鹽只有硫酸銅,同時生成的兩種氣體A、B均由表中兩種元素組成,氣體的相對分子質量都小于50。為防止污染,將產生的氣體完全轉化為最高價含氧酸鹽,消耗1L2.2mol·L-1NaOH溶液和1molO2,則兩種氣體的分子式及物質的量分別為______________,生成硫酸銅物質的量為______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com