(2011?錦州模擬)海水資源豐富,海水中主要含有Na
+、K
+、Mg
2+、Cl
-、SO
2-4、Br
-、CO
2-3、HCO
-3等離子.合理利用海水資源和保護環境是我國可持續發展的重要保證.
Ⅰ.火力發電燃燒煤排放的SO
2會造成一系列環境和生態問題.利用海水脫硫是一種有效的方法,其工藝流程如下圖所示:
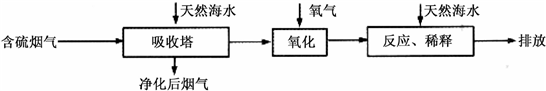
(1)天然海水的pH≈8,呈弱堿性.用離子方程式解釋原因
CO32-+H2O?HCO3-+OH-或HCO3-+H2O?H2CO3+OH-
CO32-+H2O?HCO3-+OH-或HCO3-+H2O?H2CO3+OH-
.
(2)天然海水吸收了含硫煙氣后,要用O
2進行氧化處理,其反應的化學方程式是
2H2SO3+O2═2H2SO4
2H2SO3+O2═2H2SO4
;氧化后的“海水”需要用大量的天然海水與之混合后才能排放,該操作的主要目的是
中和、稀釋經氧氣氧化后海水中生成的酸
中和、稀釋經氧氣氧化后海水中生成的酸
.
Ⅱ.重金屬離子對河流及海洋造成嚴重污染.某化工廠廢水(pH=2.0,ρ≈1g?mL
-1)中含有Ag
+、Pb
2+等重金屬離子,其濃度各約為0.1mol?L
-1.排放前擬用沉淀法除去這兩種離子,查找有關數據如下:
| 難溶電解質 |
AgI |
AgOH |
Ag2S |
pbI2 |
Pb(OH)2 |
PbS |
| Ksp |
8.3×10-17 |
5.6×10-8 |
6.3×10-50 |
7.1×10-9 |
1.2×10-15 |
3.4×10-28 |
(3)你認為往廢水中投入
B
B
(填字母序號),沉淀效果最好.
A.NaOH B.Na
2S C.KID.Ca(OH)
2(4)如果用生石灰處理上述廢水,使溶液的pH=8.0,處理后的廢水中c(Pb
2+)=
1.2×10-3mol?L-1
1.2×10-3mol?L-1
.
(5)如果用食鹽處理其只含Ag
+的廢水,測得處理后的廢水中NaCl的質量分數為0.117%.若環境要求排放標準為c(Ag
+)低于1.0×10
-8mol?L
-1,問該工廠處理后的廢水中c(Ag
+)=
9×10-9mol?L-1
9×10-9mol?L-1
,是否符合排放標準
是
是
(填“是”或“否”).
已知K
SP(AgCl)=1.8×1
-10mol?L
2.




 寒假樂園北京教育出版社系列答案
寒假樂園北京教育出版社系列答案 (2011?錦州模擬)【化學--物質結構與性質】
(2011?錦州模擬)【化學--物質結構與性質】