
【題目】紅葡萄酒密封儲存時間越長,質量越好,原因之一是儲存過程中生成了有香味的酯.在實驗室也可以用如下圖所示的裝置制取乙酸乙酯,請回答下列問題.
(1)該實驗反應物與生成物有機物的官能團種類有(填寫名稱).
(2)試管a中加入幾塊碎瓷片的目的是 .
(3)試管a中發生反應的化學方程式為 , 反應類型是 .
(4)反應開始前,試管b中盛放的溶液是 . 作用是 .
(5)反應結束后,振蕩試管b,靜置.反應結束后,試管b內的液體分成兩層,乙酸乙酯在層(填寫“上”或“下”).若分離10mL該液體混合物需要用到的主要玻璃儀器是 .
【答案】
(1)羥基、羧基、酯基
(2)防止暴沸
(3)CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O;酯化反應(取代反應)
CH3COOC2H5+H2O;酯化反應(取代反應)
(4)飽和碳酸鈉溶液;中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分層
(5)上;分液漏斗、燒杯
【解析】解:(1)乙醇與乙酸反應生成乙酸乙酯,乙醇中含﹣OH、乙酸中含﹣COOH、乙酸乙酯中含﹣COOC﹣,則官能團的名稱分別為羥基、羧基、酯基,所以答案是:羥基、羧基、酯基; (2)試管a中加入幾塊碎瓷片的目的是防止暴沸,所以答案是:防止暴沸;(3)試管a中發生反應的化學方程式為CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O,屬于酯化反應(取代反應),所以答案是:CH3COOH+C2H5OH
CH3COOC2H5+H2O,屬于酯化反應(取代反應),所以答案是:CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O;酯化反應(取代反應);(4)反應開始前,試管b中盛放的溶液是飽和碳酸鈉溶液,其作用為中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分層,所以答案是:飽和碳酸鈉溶液;中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分層;(5)試管b內的液體分成兩層,乙酸乙酯的密度小在上層,分離10mL該液體混合物選擇分液法,需要用到的主要玻璃儀器是分液漏斗、燒杯,所以答案是:上;分液漏斗、燒杯.
CH3COOC2H5+H2O;酯化反應(取代反應);(4)反應開始前,試管b中盛放的溶液是飽和碳酸鈉溶液,其作用為中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分層,所以答案是:飽和碳酸鈉溶液;中和乙酸,吸收乙醇,降低乙酸乙酯的溶解度,有利于分層;(5)試管b內的液體分成兩層,乙酸乙酯的密度小在上層,分離10mL該液體混合物選擇分液法,需要用到的主要玻璃儀器是分液漏斗、燒杯,所以答案是:上;分液漏斗、燒杯.


科目:高中化學 來源: 題型:
【題目】醋酸亞鉻水合物[Cr(CH3COO)2]2·2H2O是一種氧氣吸收劑,為紅棕色晶體,易被氧化,微溶于乙醇,不溶于水和乙醚(易揮發的有機溶劑)。其制備裝置及步驟如下:

①檢查裝置氣密性,往三頸燒瓶中依次加入過量鋅粉、適量CrCl3溶液。
②關閉k2打開k1,旋開分液漏斗的旋塞并控制好滴速。
③待三頸燒瓶內的溶液由深綠色(Cr3+)變為亮藍色(Cr2+)時,把溶液轉移到裝置乙中,當出現大量紅棕色晶體時,關閉分液漏斗的旋塞。
④將裝置乙中混合物快速過濾、洗滌和干燥,稱量得到2.76 g[Cr(CH3COO)2]2·2H2O。
(1)裝置甲中連通管a的作用是______________________。
(2)三頸燒瓶中的Zn除了與鹽酸生成H2外,發生的另一個反應的離子方程式為______________________。
(3)實驗步驟③中溶液自動轉移至裝置乙中的實驗操作為______________________。
(4)裝置丙中導管口水封的目的是______________________。
(5)洗滌產品時,為了去除可溶性雜質和水分,下列試劑的正確使用順序是________(填字母)。
a.乙醚 b.去氧冷的蒸餾水 c.無水乙醇
(6)若實驗所取用的CrCl3溶液中含溶質3.17 g,則[Cr(CH3COO)2]2·2H2O(相對分子質量為376)的產率是______________________。
(7)一定條件下,[Cr(CH3COO)2]2·2H2O受熱得到CO和CO2的混合氣體,請設計實驗檢驗這兩種氣體的存在________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是部分短周期元素原子(用字母表示)最外層電子數與原子序數的關系圖.下列說法正確的是( ) 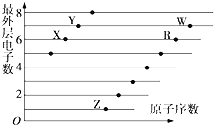
A.X和R在同一周期
B.原子半徑:W>R>X
C.氣態氫化物的穩定性:X>Y
D.X,Z形成的化合物中可能含有共價鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】由短周期元素組成的中學常見無機物A、B、C、D、E、X存在如下圖轉化關系(部分生成物和反應條件略去)。下列推斷不正確的是
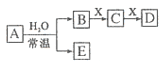
A. 若A 是單質,B和D 的反應是OH-+HCO3-=H2O+ CO32-,則E一定能還原Fe2O3
B. 若D為CO,C能和E反應,則A一定為Na2O2
C. 若X是Na2CO3,C為CO2,則A一定是氯氣,且D和E不反應
D. 若D為白色沉淀,與A摩爾質量相等,則X一定是鋁鹽
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】馬鈴薯有望成為水稻、小麥、玉米之后的我國第四大主糧作物.馬鈴薯約含20%淀粉,淀粉屬于(填“糖類”或“油脂”). 醫療上常用作“鋇餐”的是(填“硫酸鋇”或“碳酸鋇”).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列示意圖表示正確的是

A. A圖表示Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H1=+26.7kJ/mol反應的能量變化
B. B圖表示碳的燃燒熱
C. C圖表示實驗的環境溫度20℃,將物質的量濃度相等、體積分別為V1、V2的H2SO4、NaOH溶液混合,測量混合液溫度,結果如圖(已知:V1+V2=60mL)
D. D圖己知穩定性順序:B![]() B
B![]() C構成,反應過程中的能量變化曲線如圖(E1、E3表示兩反應的活化能)
C構成,反應過程中的能量變化曲線如圖(E1、E3表示兩反應的活化能)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應的發生與沉淀溶解平衡或鹽類水解平衡的移動無關的是
A. 鹽酸與碳酸鈣反應生成二氧化碳
B. 鎂條與氯化銨溶液反應生成氫氣
C. 硝酸銀溶液與鹽酸反應生成氯化銀
D. 硫酸鋁溶液和小蘇打溶液反應生成二氧化碳
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各組離子能共存的是:
A.K+、Cl-、HCO3-、H+B.NH4+、Cl-、OH-、SO42-
C.Na+、Cl-、Fe3+、NO3-D.Ba2+、Cl-、Al3+、SO42-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com