
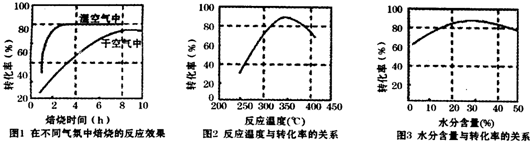
分析 (1)生成物濃度的冪之積比上反應濃度的冪之積,固體不代入表達式;2MnCO3+O2═2MnO2+2CO2為方程①②之和,所以K=K1×K2;
(2)反應自發進行的判斷依據是△H-T△S<0,反應自發進行,△H-T△S>0,反應非自發進行;
(3)由圖分析在在指定溫度下和水分含量下碳酸錳轉化率要高;
(4)陽極發生氧化反應,錳由+2價變成+4價,產生大量的氫離子.
解答 解:(1)反應①的平衡常數表達式K1=$\frac{{c}^{2}(C{O}_{2})}{c({O}_{2})}$=$\frac{({P×\frac{{n}_{1}}{{n}_{1}+{n}_{2}})}^{2}}{P×\frac{{n}_{2}}{{n}_{1}+{n}_{2}}}$=$\frac{P{{n}_{1}}^{2}}{{n}_{2}({n}_{1}+{n}_{2})}$,K與反應①、②的平衡常數K1、K2關系為:2MnCO3+O2═2MnO2+2CO2為方程①的系擴大2倍后與②之和所以K=K12×K2,
故答案為:=$\frac{P{{n}_{1}}^{2}}{{n}_{2}({n}_{1}+{n}_{2})}$;K=K12×K2;
(2)反應②在低溫下能,只有△H<0,△G<0反應自發,
故答案為:<;
(3)由圖2分析,在350℃左右碳酸錳轉化率比較高,由圖3可知水分含量的30%左右碳酸錳轉化率比較高(或20%-40%都正確),
故答案為:350℃;含水量30%;
(4)陽極發生氧化反應,錳由+2價變成+4價,電極反應為Mn2++2H2O-2e-=MnO2+4H+,產生大量的氫離子,電解后溶液的pH將減小,
故答案為:Mn2++2H2O-2e-=MnO2+4H+;減小.
點評 本題考查化學平衡常數的含義,平衡移動、電化學相關知識,題目難度中等,試題綜合性強,學生要有一定的化學基本功才能解決,試題培養了學生的靈活應用能力.


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化學 來源: 題型:選擇題
| A. | 2P1>P2 | B. | 2P1=P2 | C. | 2P1<P2 | D. | P1>P2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.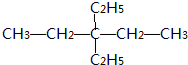 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
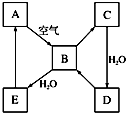 如圖表示某淡黃色固態單質A及其化合物之間的轉化關系(某些產物和反應條件已略去).B和C的相對分子質量相差16,化合物D是重要的工業原料.
如圖表示某淡黃色固態單質A及其化合物之間的轉化關系(某些產物和反應條件已略去).B和C的相對分子質量相差16,化合物D是重要的工業原料.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在101 kPa時,2 g H2完全燃燒生成液態水,放出285.8 kJ熱量,氫氣燃燒的熱化學方程式表示為2H2+O2=2H2O△H=+285.8 kJ•mol-1 | |
| B. | 由C(石墨)→C(金剛石)△H=+119 kJ•mol-1可知,石墨不及金剛石穩定 | |
| C. | 在稀溶液中:H++OH-=H2O△H=-57.3 kJ•mol-1,若將含1mol CH3COOH的醋酸溶液與含1 mol NaOH的溶液混合,放出的熱量大于57.3 kJ | |
| D. | CO(g)的燃燒熱是283.0 kJ•mol-1,則2CO2(g)=2CO(g)+O2(g)反應的△H=+(2×283.0 )kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com