
| A. | Na2CO3和HNO3;NaHCO3和HNO3 | B. | BaCl2和Na2CO3;Ba(OH)2和K2CO3 | ||
| C. | Ba(OH)2和NaHSO4;Ba(OH)2和H2SO4 | D. | NaOH和HF;Ba(OH)2和HNO3 |
分析 A.碳酸氫鈉電離生成碳酸氫根;
B.反應實質均為碳酸鋇與鋇離子反應;
C.反應均生成硫酸鋇和水;
D.氫氟酸是弱酸.
解答 解:A.碳酸鈉電離生成碳酸根,離子方程式:CO32-+2H+=CO2↑+H2O,碳酸氫鈉電離生成碳酸氫根,離子方程式:HCO3-+H+=H2O+CO2↑,離子方程式不同,故A錯誤;
B.反應實質均為碳酸鋇與鋇離子反應,則能用同一離子方程式表示,離子方程式:Ba2++CO32═BaCO3↓,故B正確;
C.反應均生成硫酸鋇和水,則能用同一離子方程式表示,離子方程式:Ba2++2H++2OH-+SO42-═BaSO4↓+2H2O.故C正確
D.氫氟酸是弱酸應分子式表示,離子方程式:HF+OH-═F-+H2O,硝酸是強酸,離子方程式:H++OH-=H2O,離子方程式不同,故D錯誤.
故選BC.
點評 本題考查離子反應方程式的書寫,明確發生的化學反應及離子反應中應保留化學式的物質即可解答,題目難度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
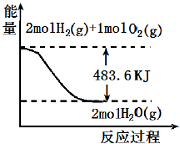
| A. | 表示 2molH2 (g)完全燃燒生成水蒸氣吸收241.8 kJ熱量 | |
| B. | 表示的熱化學方程式為:H2(g)+$\frac{1}{2}$02(g)═H20(g)△H=-241.8 kJ/mol | |
| C. | 表示2mol H2(g)所具有的能量一定比2 mol氣態水所具有的能量多483.6 kJ | |
| D. | H20(g)的能量低于H2(g)和O2(g)的能量之和 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
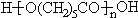 }及阻燃劑四溴雙酚A.合成線路如下:
}及阻燃劑四溴雙酚A.合成線路如下: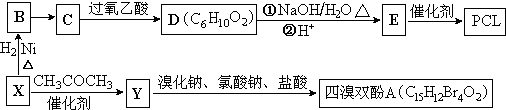


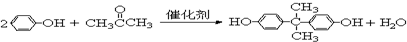 .
.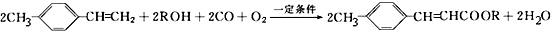
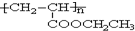 ,寫出合成該涂料的反應流程圖:
,寫出合成該涂料的反應流程圖: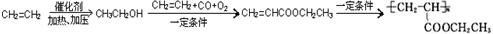 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 弱酸的化學式 | CH3COOH | HCN | H2S |
| 電離常數 | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
| A. | 等物質的量濃度的各溶液,pH關系為:pH(CH3COONa)>pH(Na2S)>pH(NaCN) | |
| B. | a mol/L HCN溶液與b mol/LNaOH溶液等體積混合,所得溶液中c( Na+)>c(CN-),則a 一定小于或等于b | |
| C. | NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) | |
| D. | 將少量的H2S通入NaCN溶液中,反應為:H2S+2CN-=2HCN+S2- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
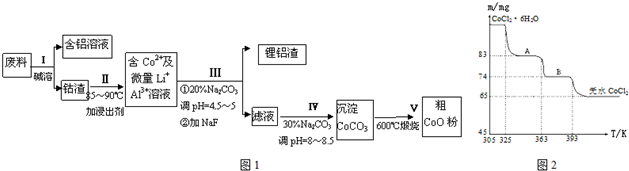
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
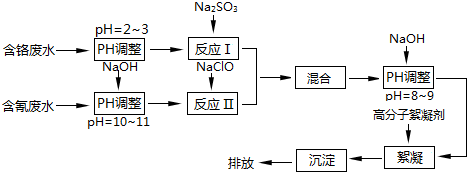
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ④HCl ⑤C2H4 ⑥Br2 ⑦HNO3 ⑧SO2.
④HCl ⑤C2H4 ⑥Br2 ⑦HNO3 ⑧SO2.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SiO2是制造太陽能電池板的主要材料 | |
| B. | NO、NO2是大氣污染物,能在空氣中穩定存在 | |
| C. | 漂白精的有效成分是Ca(ClO)2 | |
| D. | Fe與S化合生成Fe2S3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
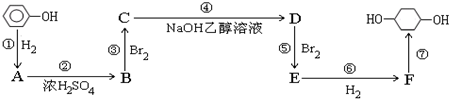
 ,F
,F ;A含有的官能團名稱是羥基;
;A含有的官能團名稱是羥基;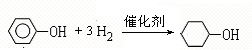 ;
; +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$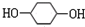 +2NaBr.
+2NaBr.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com