
 2NH3現向一密閉容器中充入1mol N2和3mol H2,在一定條件下使該反應發生,下列有關說法正確的是( )
2NH3現向一密閉容器中充入1mol N2和3mol H2,在一定條件下使該反應發生,下列有關說法正確的是( )| A.達到化學平衡時,N2將完全轉化為NH3 |
| B.達到化學平衡時,N2、H2和NH3的物質的量濃度一定相等 |
| C.達到化學平衡時,N2、H2和NH3的物質的量濃度不再變化 |
| D.達到化學平衡時,正、逆反應速率為0 |
科目:高中化學 來源:不詳 題型:計算題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 pC (g)+q(g);△H<0。下列結論中不正確的是( )
pC (g)+q(g);△H<0。下列結論中不正確的是( ) 查看答案和解析>>
科目:高中化學 來源:不詳 題型:計算題
 2NO2(g) △H>0 ,在溫度為T1、 T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。T1 T2(填“>”、“<”或“=”);A、C兩點的速率vA vC(同上)。
2NO2(g) △H>0 ,在溫度為T1、 T2時,平衡體系中NO2的體積分數隨壓強變化曲線如圖所示。T1 T2(填“>”、“<”或“=”);A、C兩點的速率vA vC(同上)。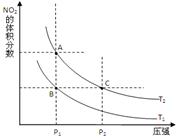
| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
 N2O4(g)的平衡常數K的值為 。
N2O4(g)的平衡常數K的值為 。 查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.配制FeSO4溶液時在溶液中加入稀硫酸 |
| B.溫度控制在450℃有利于二氧化硫的催化氧化 |
| C.增大壓強有利于合成氨反應 |
D.工業制取金屬鉀Na(l)+ KCl(l)  NaCl(l)+K(g)選取適宜的溫度,使K成蒸氣從反應混合物中分離出來 NaCl(l)+K(g)選取適宜的溫度,使K成蒸氣從反應混合物中分離出來 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.縮小容器體積,使壓強增大 | B.保持體積不變,充入O2 |
| C.保持體積不變,充入氦氣 | D.保持壓強不變,充入氦氣 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
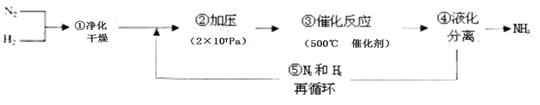
| A.①②③ | B.②④⑤ | C.①③⑤ | D.②③④ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2Z(g) 此反應達到平衡的標志是( )
2Z(g) 此反應達到平衡的標志是( )| A.正反應和逆反應的速率都為零 |
| B.容器內各物質的濃度不隨時間變化 |
| C.容器內X、Y、Z的濃度之比為1∶2∶2 |
| D.單位時間消耗0.1molX同時生成0.2molZ |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.平衡時,體系內含NO2為0.04mol·L-1 |
| B.平衡時,N2O4的轉化率為60% |
| C.前2s,N2O4的平均反應速率為0.005mol·L-1·s-1 |
| D.在2s時,體系內壓強為反應前的1.1倍 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com