
| A. | 原子半徑 A>B>D>C | B. | 原子序數 D>C>B>A | ||
| C. | 離子半徑 C3->D->B+>A2+ | D. | 單質的還原性 A>B>D>C |
分析 短周期元素的離子:aA2+、bB+、cC3-、dD-都具有相同的電子層結構,所以有:a-2=b-1=c+3=d+1,且A、B在周期表中C、D的下一周期,原子序數:a>b>d>c,A、B處于同一周期,C、D處于同一周期,且A、B處于C、D所在周期的相鄰下一周期,A、B形成陽離子,則A、B為金屬,C、D形成陰離子,則C、D為非金屬,且A、B、C、D分別是Mg、Na、N、F元素,結合元素周期律遞變規律解答該題.
解答 解:短周期元素的離子:aA2+、bB+、cC3-、dD-都具有相同的電子層結構,所以有:a-2=b-1=c+3=d+1,且A、B在周期表中C、D的下一周期,原子序數:a>b>d>c,A、B處于同一周期,C、D處于同一周期,且A、B處于C、D所在周期的相鄰下一周期,A、B形成陽離子,則A、B為金屬,C、D形成陰離子,則C、D為非金屬,且A、B、C、D分別是Mg、Na、N、F元素,
A.A、B在周期表中C、D的下一周期,并且原子序數:a>b>d>c,原子核外電子層數越多,半徑越大,同周期元素原子序數越大,原子半徑越小,則有原子半徑:B>A>C>D,故A錯誤;
B.aA2+、bB+、cC3-、dD-都具有相同的電子層結構,所以有:a-2=b-1=c+3=d+1,所以原子序數:a>b>d>c,故B錯誤;
C.aA2+、bB+、cC3-、dD-都具有相同的電子層結構,核電荷數越大,離子半徑越小,核電荷數a>b>d>c,所以離子半徑C3->D->B+>A2+,故C正確;
D.A、B處于同一周期,A、B形成陽離子,則A、B為金屬,原子序數A>B,單質還原性B>A,C、D處于同一周期,C、D形成陰離子,則C、D為非金屬,原子序數D>C,單質氧化性D>C,故D錯誤;
故選C.
點評 本題考查位置結構性質關系及應用,根據核外電子排布確定元素所在周期表中的位置,理解掌握元素周期律的遞變規律,難度不大,注意由于是短周期元素,可以確定具體的元素.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | SO2 | B. | NO2 | C. | PM2.5 | D. | CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 密度比為1:1 | B. | 密度比為11:16 | C. | 體積比為16:11 | D. | 體積比為11:16 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
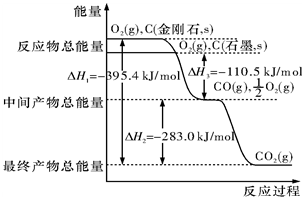 金剛石和石墨均為碳的同素異形體,它們在氧氣不足時燃燒生成一氧化碳,在氧氣充足時充分燃燒生成二氧化碳,反應中放出的熱量如圖所示.
金剛石和石墨均為碳的同素異形體,它們在氧氣不足時燃燒生成一氧化碳,在氧氣充足時充分燃燒生成二氧化碳,反應中放出的熱量如圖所示.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com