
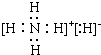 .
.分析 A、B、C、D、E都是短周期主族元素,原子半徑D>A>E>B,D和E的一種化合物為淡黃色,且D為金屬,則D為Na,E為O,其中D、B處在同一主族,B為H;A、C、E處在同一周期,均為第二周期元素,E原子核內質子數等于A、B原子核內質子之和,A為N,C原子最外層上的電子數是B原子最外層電子數的4倍,C為C,然后結合元素周期律及元素化合物知識來解答.
解答 解:A、B、C、D、E都是短周期主族元素,原子半徑D>A>E>B,D和E的一種化合物為淡黃色,且D為金屬,則D為Na,E為O,其中D、B處在同一主族,B為H;A、C、E處在同一周期,均為第二周期元素,E原子核內質子數等于A、B原子核內質子之和,A為N,C原子最外層上的電子數是B原子最外層電子數的4倍,C為C,
(1)C的元素在元素周期表中的位置為第二周期第ⅣA族;具有相同電子排布的離子中原子序數大的離子半徑小,則D、E、A簡單離子半徑由大到小的順序是N3->O2->Na+,
故答案為:第二周期第ⅣA族;N3->O2->Na+;
(2)非金屬性越強,對應氫化物越穩定,則A、C、E能形成的最簡單的液態或氣態氫化物的穩定性由大到小的順序是H2O>NH3>CH4,
故答案為:H2O>NH3>CH4;
(3)E與B形成的四原子分子為H2O2,其結構式是H-O-O-H,已知B與A可形成AB5的物質,它的所有原子的最外層都符合相應稀有氣體原子的最外電子層結構,為離子化合物NH4H,電子式為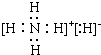 ,故答案為:H-O-O-H;
,故答案為:H-O-O-H;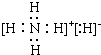 ;
;
(4)由以上5種元素中部分元素形成的物質,發生置換反應方程式如2Na+2H2O=2NaOH+H2↑、C+H2O(g)$\frac{\underline{\;高溫\;}}{\;}$CO+H2,
故答案為:2Na+2H2O=2NaOH+H2↑;C+H2O(g)$\frac{\underline{\;高溫\;}}{\;}$CO+H2.
點評 本題考查位置、結構與性質,為高頻考點,把握元素的推斷、元素化合物、元素周期律為解答的關鍵,側重分析與推斷能力的考查,注意淡黃色固體為過氧化鈉為推斷的突破口,題目難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 聚乙烯塑料的老化是由于發生了加成反應 | |
| B. | 乙酸乙酯在堿性條件下的水解反應稱為皂化反應 | |
| C. | 葡萄糖注射液不能產生丁達爾效應現象,不屬于膠體 | |
| D. | 棉、麻、合成纖維完全燃燒都只生成CO2和H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
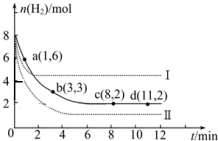 工業上“固定”和利用CO2能有效地減輕“溫室”效應,可用CO2生產燃料甲醇:
工業上“固定”和利用CO2能有效地減輕“溫室”效應,可用CO2生產燃料甲醇:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向Mg(HCO3)2溶液中加入過量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O | |
| B. | FeBr2溶液中通入等物質的量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | 酸性KMnO4溶液中加H2O2,紫色褪去:2MnO4-+H2O2+6H+=2Mn2++3O2↑+4H2O | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 如圖為實驗室某濃鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題:
如圖為實驗室某濃鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 H++OH-、HCO3-+H2O
H++OH-、HCO3-+H2O +H2CO3+OH-、HCO3-+H2O
+H2CO3+OH-、HCO3-+H2O H3O++CO32-
H3O++CO32- 查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O2可作漂白劑和供氧劑,碳酸鈉可用于治療胃酸過多 | |
| B. | 工業上用次氯酸制漂白粉,保存漂白粉的塑料袋要密封 | |
| C. | 氯氣用于自來水消毒,是因為生成的次氯酸有殺菌、消毒的作用 | |
| D. | 溴化銀用于人工降雨,單質碘加入食鹽中用于制加碘鹽 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
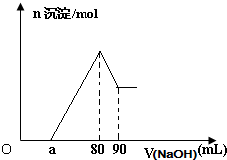 將一塊鎂鋁合金投入一定體積的1mol/L稀鹽酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物質的量與加入NaOH溶液體積的關系如圖.下列說法中不正確的是( )
將一塊鎂鋁合金投入一定體積的1mol/L稀鹽酸中,待合金完全溶解后往溶液里滴入1mol/L的NaOH溶液,生成沉淀物質的量與加入NaOH溶液體積的關系如圖.下列說法中不正確的是( )| A. | 由圖可以確定該鎂鋁合金中鋁的質量為0.27 g | |
| B. | 由圖可以確定該合金中兩元素的物質量之比的最大值為4 | |
| C. | 當滴入1mol/L的NaOH溶液85mL時,所得沉淀的成分為Mg(OH)2和Al(OH)3 | |
| D. | 由圖可以確定a的取值范圍為:0≤a≤50 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com