
下表是元素周期表的一部分。表中所列的字母分別代表一種化學元素。
| | | | |||||||||||||||
| | | | | | a | | b | | |||||||||
| | | c | | | d | e | | ||||||||||
| | | | | | | | | f | | g | | | | | | | |
1) 三角錐 sp3 平面三角形 sp2 非極性分子
(2)HF ,HF中有氫鍵
(3)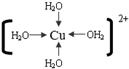 (4)[Co(NH3)5SO4]Br, NH3、SO42-
(4)[Co(NH3)5SO4]Br, NH3、SO42-
(5) 12、 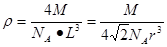
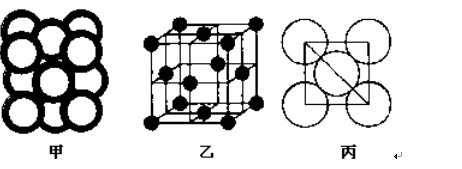
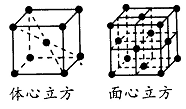
解析試題分析:根據元素在周期表中的位置可確定a是N;b是F;c是Al;d是S;e是Cl;f是Co;g是Cu。(1)NH3分子構型為三角錐型;中心原子N的雜化形式為sp3雜化;SO3分子構型為平面三角形;中心原子S的雜化形式為sp2;由于各個化學鍵的排列是對稱的,所以該分子是非極性分子。(2)在HF、H2S、HCl三種物質中由于在HF的分子之間存在氫鍵,增加了分子之間的相互作用力,所以HF的沸點最高。(3)在溶液中Cu2+是以四水和銅離子的形式存在的,其結構簡式是 。(4)Co(NH3)5BrSO4。Co3+ 的配位數是6可形成兩種配合物為確定f的配合物的結構,在第一種配合物的溶液中加BaCl2溶液時,產生白色沉淀,證明SO42-不是配位體;在第二種配合物溶液中加入BaCl2溶液時,則無明顯現象,證明在化合物中SO42-是配位體。則第二種配合物的化學式[Co(NH3)5SO4]Br;該配合物的配體是NH3及SO42-。(5)Al單質晶體中原子的堆積方式為立方面心堆積。則Al單質晶體中原子的配位數為(3×8)÷2=12;在每個晶胞中含有的Al原子的個數為8×1/8+6×1/2=4.由于的原子半徑為r,所以晶胞的邊長
。(4)Co(NH3)5BrSO4。Co3+ 的配位數是6可形成兩種配合物為確定f的配合物的結構,在第一種配合物的溶液中加BaCl2溶液時,產生白色沉淀,證明SO42-不是配位體;在第二種配合物溶液中加入BaCl2溶液時,則無明顯現象,證明在化合物中SO42-是配位體。則第二種配合物的化學式[Co(NH3)5SO4]Br;該配合物的配體是NH3及SO42-。(5)Al單質晶體中原子的堆積方式為立方面心堆積。則Al單質晶體中原子的配位數為(3×8)÷2=12;在每個晶胞中含有的Al原子的個數為8×1/8+6×1/2=4.由于的原子半徑為r,所以晶胞的邊長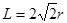 。則該晶體的密度為
。則該晶體的密度為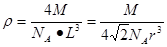 。
。
考點:考查元素的推斷、物質的分子結構、晶體結構及晶體密度的計算的知識。


 芒果教輔達標測試卷系列答案
芒果教輔達標測試卷系列答案科目:高中化學 來源: 題型:填空題
生物質能是一種潔凈、可再生能源。生物質氣(主要成分為CO、CO2、H2等)與混合,在含有Zn、Cu等元素的催化劑條件下能合成一種生物質能——甲醇。
(1) 與CO互為等電子體的物質的化學式是 。
(2) CO2分子中碳原子的雜化類型是 雜化。
(3) 按電子排布Zn在元素周期表中屬于 區,
其晶體屬于六方最密堆積,它的配位數是 。
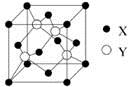
(4) Cu的一種氯化物晶體的晶胞結構如圖所示。(空心球代表氯離子),則一個晶胞中所含的數目是 。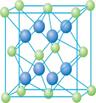
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(14分)某配位化合物為深藍色晶體,由原子序數依次增大的A、B、C、D、E五種元素組成,其原子個數比為l4:4:5:1:1。其中C、D元素同主族且原子序數D為C的二倍,E元素的外圍電子排布為(n-1)dn+6nsl,回答下列問題。
(1)元素D在周期表中的位置是 。
(2)該配位化合物的化學式為 。
(3)C元素可與A元素形成兩種常見的化合物,其原子個數比分別為1:1和l:2,兩種化合物可任意比互溶,解釋其主要原因為 。
(4)A元素與B元素可形成分子式為A2B2的某化合物,該化合物的分子具有平面結構,則其結構式為 。
(5)已知E的晶胞結構如下圖所示,又知晶胞邊長為3.61×10-8cm,則E的密度為 ;EDC4常作電鍍液,其中DC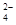 的空間構型是 ,其中D原子的雜化軌道類型是 。
的空間構型是 ,其中D原子的雜化軌道類型是 。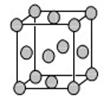
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(12分)【化學-物質結構與性質】
原子序數依次增大的A、B、C、D、E、F六種元素。其中A的基態原子有3個不同的能級,各能級中的電子數相等;C的基態原子2p能級上的未成對電子數與A原子的相同;D為它所在周期中原子半徑最大的主族元素;E和C位于同一主族,F的原子序數為29。
(1)F原子基態的核外電子排布式為 。
(2)在A、B、C三種元素中,第一電離能由小到大的順序是 (用元素符號回答)。
(3)元素B的簡單氣態氫化物的沸點遠高于元素A的簡單氣態氫化物的沸點,其主要原因是 。
(4)由A、B、C形成的離子CAB-與AC2互為等電子體,則CAB-的結構式為 。
(5)在元素A與E所形成的常見化合物中,A原子軌道的雜化類型為 。
(6)由B、C、D三種元素形成的化合物晶體的晶胞如圖所示,則該化合物的化學式為 。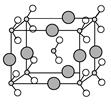
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
(12分)【化學一物質結構與性質】
根據物質結構與性質的關系,請回答下列問題:
(1)基態鉻(Cr)原子的價電子排布式是________,這樣排布使整個體系能量最低,原因是________。
(2)氨水中存在多種形式的氫鍵,其中與“氨極易溶于水”這種性質相關的氫鍵可表示為:_________。解釋NH3分子中鍵角大于H2O中的鍵角的原因是_________ 。
(3)下列各項的比較中正確的是_________。
| A.第一電離能:Mg>Al | B.電負性:P>Ge |
| C.穩定性:AsH3>H2S | D.金屬性: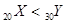 |
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
A、B、C、D、E、F六種元素,其中A、B、C、D、E為短周期主族元素。它們之間的關系如下:
Ⅰ.原子半徑:A < C< B < E< D
Ⅱ.原子的最外層電子數:A=D C=E A + B=C
Ⅲ.原子的核外電子層數:B=C=2A
Ⅳ.B元素的主要化合價:最高正價+最低負價=2
請回答:
(1)甲為由A、B兩種元素組成的常見氣體,寫出其電子式 ;
(2)寫出某黑色含F的磁性氧化物與E最高價氧化物對應水化物的稀溶液反應的離子方程式 。裝置1經過一段時間向插入碳棒的玻璃筒內滴入酚酞溶液,可觀察到碳棒附近的溶液變紅,該電極反應為 。單質F發生 (填電化學腐蝕類型)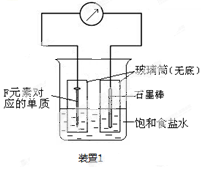
(3)向A、B、C三種元素組成的某鹽稀溶液中滴加AgNO3溶液生成白色沉淀,該反應的化學方程式為 ,已知該鹽溶液常溫下呈酸性,則0.1mol/L該鹽溶液中離子濃度的大小順序為 。
(4)上述元素中的五種元素可形成一種常見復鹽,經檢測該復鹽中三種離子的個數比為2:1:2,則該復鹽的化學式為 。為檢驗該復鹽中的某種有色離子存在,請寫出實驗的操作步驟和現象 。
查看答案和解析>>
科目:高中化學 來源: 題型:問答題
【物質結構與性質】
過渡元素具有較多的空軌道,所以第四周期的Cr、Fe、Co、Ni、Cu、Zn等多種金屬能形成配合物。
(1)基態Cu原子的核外電子排布式為 ;
(2)科學家通過X射線測得膽礬結構示意圖可簡單表示如下: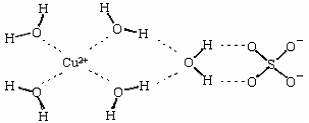
圖中虛線表示的作用力為 ;
(3)膽礬溶液與氨水在一定條件下可以生成Cu(NH3)4SO4·H2O晶體。在Cu(NH3)4SO4·H2O晶體中,[Cu(NH3)4]2+為平面正方形結構,則呈正四面體結構的原子團是 ,其中心原子的雜化軌道類型是 ;
(4)金屬鎳粉在CO氣流中輕微加熱,生成無色揮發性液態Ni(CO)4,呈正四面體構型。試推測四羰基鎳的晶體類型是 , Ni(CO)4易溶于下列 。
| A.水 | B.四氯化碳 | C.苯 | D.硫酸鎳溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
某同學設計實驗以探究元素性質的遞變規律,實驗裝置如圖所示。
實驗Ⅰ:根據元素最高價含氧酸的酸性強弱探究元素非金屬性遞變規律。
已知A裝置的燒瓶里裝有大理石,分液漏斗里裝有稀HNO3,B裝置中裝有飽和碳酸氫鈉溶液,裝置C中裝有Na2SiO3溶液,試回答:
(1)A中反應的離子方程式為____________________,C中可觀察到的現象是________。
(2)B裝置的作用是__________________________________________________________。
(3)根據實驗現象推知,碳酸、硝酸、硅酸的酸性強弱順序是________,由此得出碳、硅、氮三種元素非金屬性的強弱順序是________。
實驗Ⅱ:已知常溫下高錳酸鉀與濃鹽酸混合可產生氯氣,利用該裝置探究氯和溴元素的非金屬性強弱。
(4)寫出B裝置中發生反應的離子方程式:_______________________________________。
(5)C裝置的作用是_________________________________________________________。
(6)實驗結論:氧化性:____________________,非金屬性:____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:單選題
下列敘述錯誤的是
①離子鍵沒有方向性和飽和性,而共價鍵有方向性和飽和性
②配位鍵在形成時,是由成鍵雙方各提供一個電子形成共用電子對
③金屬鍵的實質是金屬中的“自由電子”與金屬陽離子形成的一種強烈的相互作用
④在冰晶體中,既有極性鍵、非極性鍵,又有氫鍵
⑤化合物NH4Cl和CuSO4·5H2O都存在配位鍵
⑥NaCl、HF、CH3CH2OH、SO2都易溶于水,但原因不完全相同
| A.①③ | B.②④ | C.②⑤ | D.④⑥ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com