
【題目】高鐵酸鉀是綠色、環保型水處理劑。工業上利用硫酸亞鐵為原料,通過鐵黃(FeOOH)制備高鐵酸鉀,可降低生產成本且產品質量優。工藝流程:
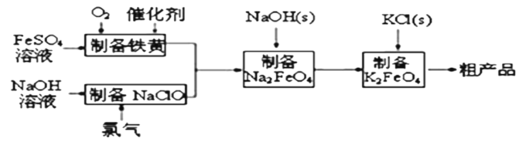
回答下列問題:
(1)已知:常溫下,Ksp[Fe(OH)3]=4.0×10—38。高鐵酸鉀的凈水能力與廢水的pH有關,當溶液pH=2時,廢水中c(Fe3+)=_______________molL﹣1
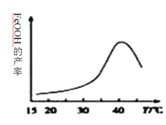
(2)制備鐵黃的離子方程式為_______________。實驗測得反應溶液的pH、溫度對鐵黃產率的影響如圖所示。反應溫度宜選擇_________。
(3)①高鐵酸鹽在水溶液中有四種含鐵形體。25℃時,它們的物質的量分數隨pH的變化如圖所示:
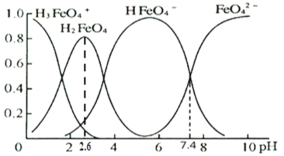
pH=2.6時,溶液中主要含鐵形體濃度的大小關系為________。
②已知H3FeO4+電離常數分別為:K1=2.51×10—2,K2=4.16×10—4,K3=5.01×10—8,當pH=4時,溶液中![]() =________。
=________。
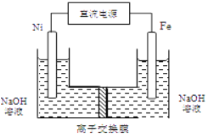
(4)工業上還可用通過電解濃NaOH溶液制備Na2FeO4,其工作原理如圖所示:陽極的電極反應式為__________;其中可循環使用的物質____________。
【答案】0.04 12Fe2++3O2+2H2O=4FeOOH+8Fe3+ 40℃ c(H2FeO4)>c(HFeO4-)>c(H3FeO4+) 4.16 Fe+8OH--6e-=FeO42- +4H2O NaOH溶液
【解析】
FeSO4溶液中通入O2,在催化劑作用下發生反應12FeSO4+3O2+2H2O=4FeOOH+4Fe2(SO4)3;NaOH溶液中通入Cl2,發生反應2NaOH+Cl2=NaCl+NaClO+H2O,兩溶液混合后發生反應2FeOOH+3NaClO+4NaOH=2Na2FeO4+3NaCl+3H2O。高鐵酸鈉與氯化鉀反應生成高鐵酸鉀,據此解答。
(1)pH=2時,c(OH-)=10-12mol/L,廢水中c(Fe3+)=![]() molL﹣1=0.04molL﹣1。答案為:0.04;
molL﹣1=0.04molL﹣1。答案為:0.04;
(2)由以上分析知,制備鐵黃的離子方程式為12Fe2++3O2+2H2O=4FeOOH+8Fe3+。從圖中可以看出,40℃時FeOOH的產率最大,所以反應溫度宜選擇40℃。答案為:12Fe2++3O2+2H2O=4FeOOH+8Fe3+;40℃;
(3)①從圖中可以看出,pH=2.6時,溶液中主要含鐵形體濃度的大小關系為c(H2FeO4)>c(HFeO4-)>c(H3FeO4+)。答案為:c(H2FeO4)>c(HFeO4-)>c(H3FeO4+);
②pH=4時,計算溶液中![]() ,應使用包含兩種離子的電離平衡H2FeO4
,應使用包含兩種離子的電離平衡H2FeO4![]() H++HFeO4-,K2=
H++HFeO4-,K2=![]() ,所以
,所以![]() =
=![]() =4.16。答案為:4.16;
=4.16。答案為:4.16;
(4)通過電解濃NaOH溶液制備Na2FeO4,陽極為Fe,電極反應式為Fe+8OH--6e-=FeO42- +4H2O,陰極為Ni,電極反應式為6H2O+6e-=6OH- +3H2↑,電解后NaOH溶液的濃度減小,但可以循環使用,所以可循環使用的物質為NaOH溶液。答案為:Fe+8OH--6e-=FeO42- +4H2O;NaOH溶液。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】某二元弱酸的酸式鹽NaHA溶液,若pH<7,則溶液中各離子的濃度關系不正確的是( )
A. c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) B. c(H+)+ c(A2-)= c(OH-)+ c(H2A)
C. c(Na+)= c(HA-)+ c(H2A)+ c(A2-) D. c(Na+)+ c(H+)= c(HA-)+2 c(A2-)+ c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下是合成一種功能高分子I的路線圖。
 已知以下信息:
已知以下信息:
①RCN![]() RCOOH
RCOOH
②烴E的相對分子質量為92
回答下列問題:
(1)G中官能團的名稱為__,__;
(2)反應①和⑥的反應類型分別為__,__;
(3)下列關于物質C的說法錯誤的是__(填字母標號)
A.可利用紅外光譜法確定物質C中的官能團
B.物質C存在順反異構體
C.物質C能與NaHCO3反應產生氣體
D.物質C最多有8個原子共平面
(4)反應④的化學方程式為__;
(5)F的同分異構體中含有苯環且苯環上連有3個硝基的結構共有__種。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖所示,U形管內盛有100mL的溶液,按要求回答下列問題:
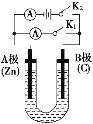
(1)斷開K2,閉合K1,若所盛溶液為CuSO4溶液,則A極為________極,B極的電極反應式為_________________________________________。若所盛溶液為KCl溶液,則B極的電極反應式為__________________________________。
(2)斷開K1,閉合K2,若所盛溶液為滴有酚酞的NaCl溶液,則:
①A電極附近可以觀察到的現象是________,Na+移向________(填“A”或“B”)極。
②B電極上的電極反應式為______________________________________,總反應的化學方程式是_________________________________________。
③反應一段時間后斷開K2,若忽略溶液的體積變化和氣體的溶解,B極產生氣體的體積(標準狀況)為11.2mL,將溶液充分混合,溶液的pH約為________。若要使電解質溶液恢復到原狀態,需向U形管內加入或通入一定量的________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘及其化合物在人類活動中占有重要地位。已知反應H2(g) + I2(g)![]() 2HI(g) ΔH=﹣11 kJ·mol-1。716K時,在一密閉容器中按物質的量比1:1充入H2(g)和I2(g),測得氣體混合物中碘化氫的物質的量分數與反應時間的關系如下圖:
2HI(g) ΔH=﹣11 kJ·mol-1。716K時,在一密閉容器中按物質的量比1:1充入H2(g)和I2(g),測得氣體混合物中碘化氫的物質的量分數與反應時間的關系如下圖:

(1)若反應開始時氣體混合物的總壓為p kPa,則反應在前20 min內的平均速率![]() (HI)=_____kPa·min-1(用含p的式子表示)。
(HI)=_____kPa·min-1(用含p的式子表示)。
(2)反應達平衡時,H2的轉化率α(H2)=____________。
(3)上述反應中,正反應速率為v正= k正·c(H2)·c(I2),逆反應速率為v逆=k逆·c2(HI),其中k正、k逆為速率常數。升高溫度,![]() ________(填“增大”“減小”或“不變”)。
________(填“增大”“減小”或“不變”)。
(4)降低溫度,平衡可能逆向移動的原因是__________。
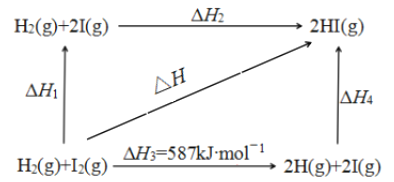
(5)1 mol H2(g)分子中化學鍵斷裂時需要吸收436 kJ的能量,下圖中的ΔH2=________kJmol-1
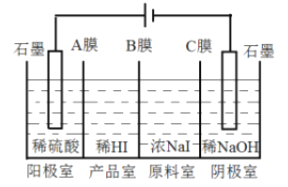
(6)氫碘酸可用“四室式電滲析法”制備,電解裝置及起始的電解質溶液如上圖所示。
①陽極電極反應式為______________。
②陽膜和陰膜分別只允許陽離子、陰離子通過,A膜為陽膜,則B膜為______膜,C膜為______膜。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,下列溶液中,有關微粒物質的量濃度關系正確的是( )
A. 0.1mol·L-1(NH4)2Fe(SO4)2溶液:c(![]() )>c(
)>c(![]() )>c(H+)>c(Fe2+)
)>c(H+)>c(Fe2+)
B. 將100mL 0.1mol·L-1Na2CO3溶液逐滴滴加到100mL 0.1mol·L-1鹽酸中:c(Na+)>c(C1-)>c(![]() )>c(
)>c(![]() )
)
C. pH=12的NaOH溶液與等體積pH=2的醋酸溶液混合后:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
D. 0.1mol·L-1NaHCO3溶液:c(H+)+2c(H2CO3)=c(OH-)+c(![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
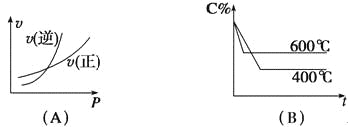
【題目】圖中C%表示某反應物在體系中的百分含量,v表示反應速率,p表示壓強,t表示反應時間,圖(A)為溫度一定時壓強與反應速率的關系曲線;圖(B)為壓強一定時,在不同時間C%與溫度的關系曲線。同時符合以下兩個圖像的反應是( )
A.4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=-808.7 kJ/mol
4NO(g)+6H2O(g) △H=-808.7 kJ/mol
B.N2O3(g)![]() NO2(g)+NO(g) △H=+41.8 kJ/mol
NO2(g)+NO(g) △H=+41.8 kJ/mol
C.3NO2(g)+H2O(l)![]() 2HNO3(l)+NO(g) △H=-261.3 kJ/mol
2HNO3(l)+NO(g) △H=-261.3 kJ/mol
D.CO2(g)+C(s)![]() 2CO(g) △H=+171.4kJ/mol
2CO(g) △H=+171.4kJ/mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】肯定屬于同族元素且性質相似的是( )
A. 原子核外電子排布式:A為1s22s2,B為1s2
B. 結構示意圖:A為![]() ,B為
,B為![]()
C. A原子基態時2p軌道上有1個未成對電子,B原子基態時3p軌道上也有1個未成對電子
D. A原子基態時2p軌道上有一對成對電子,B原子基態時3p軌道上也有一對成對電子
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】膳食纖維具有突出的保健功能,是人體的“第七營養素”。木質素是一種非糖類膳食纖維,其單體之一——芥子醇結構簡式如圖所示。下列有關芥子醇的說法正確的是( )
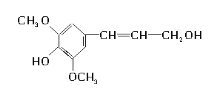
A.芥子醇分子中含9種不同化學環境的H原子
B.芥子醇分子中所有碳原子不可能在同一平面上
C.芥子醇屬于芳香族化合物,分子式是C11H12O4
D.芥子醇能發生的反應類型有氧化、取代、加成
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com