
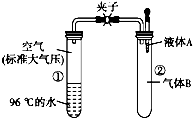
 如圖所示,夾子開始處于關閉狀態,將液體A滴入試管②中,一段時間后打開夾子,可發現試管①內的水立刻沸騰 了.(已知,氣壓減小,水的沸點降低)則液體A和氣體B的組合不可能是下列的( )
如圖所示,夾子開始處于關閉狀態,將液體A滴入試管②中,一段時間后打開夾子,可發現試管①內的水立刻沸騰 了.(已知,氣壓減小,水的沸點降低)則液體A和氣體B的組合不可能是下列的( )| A. | 氫氧化鈉溶液、二氧化碳 | B. | 飽和食鹽水、氯化氫 | ||
| C. | 氫氧化鈉溶液、一氧化碳 | D. | 石灰水、二氧化硫 |
 開心練習課課練與單元檢測系列答案
開心練習課課練與單元檢測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 12 | B. | 16 | C. | 24 | D. | 32 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | S→SO3→H2SO4 | B. | Fe→FeCl3→FeCl2 | ||
| C. | Si→H2SiO3→Na2SiO3 | D. | Al2O3→Al(OH)3→NaAlO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 米酒變酸的過程涉及了氧化反應 | |
| B. | 汽油、柴油、植物油都是碳氫化合物 | |
| C. | 含5個碳原子的有機物分子中最多可形成4個碳碳單鍵 | |
| D. | 蛋白質的水解和油脂的皂化都是由高分子生成小分子的過程 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
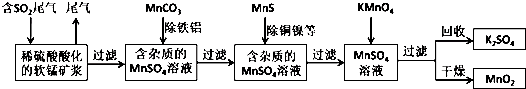
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將標準狀況下的2.24L CO2通入150mL 1mol•L-1 NaOH溶液中,所得溶液中c(CO32-)>c(HCO3-) | |
| B. | 常溫下0.1 mol•L-1的下列溶液①NH4Al(SO4)2 ②NH4Cl ③NH3•H2O ④CH3COONH4中,c(NH4+)由大到小的順序是:②>①>④>③ | |
| C. | 0.1 mol•L-1 pH為9的NaHB溶液中:c(HB-)>c(B2-)>c(H2B) | |
| D. | 室溫下,將0.4mol/L HA溶液和0.2mol/LNaOH溶液等體積混合(忽略混合時溶液體積的變化)測得混合液pH=5,則c(A-)+c (OH-)>c (H+)+c(HA) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 稀醋酸中加入少量冰醋酸能增大醋酸的電離程度 | |
| B. | 25℃時,等體積等濃度的鹽酸與氨水混合后,溶液pH=7 | |
| C. | 0.1 mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) | |
| D. | 25℃時,0.1mol•L-1的硫化氫溶液比等濃度的硫化鈉溶液的導電能力弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若誤飲c(Ba2+)=1.0×10-5mol/L溶液時,不會引起Ba2+中毒 | |
| B. | 因為Ksp(BaCO3)>Ksp(BaSO4),所以BaCO3不能作內服造影劑 | |
| C. | 向同濃度Na2SO4和Na2CO3的混合溶液中滴加BaCl2溶液,BaSO4先析出 | |
| D. | 在BaSO4和BaCO3共存的懸濁液中,c(SO42-):c(CO32-)=1:51 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com