
圖中是在實驗室進行氨氣快速制備與性質實驗的組合裝置,部分固定裝置未畫出。
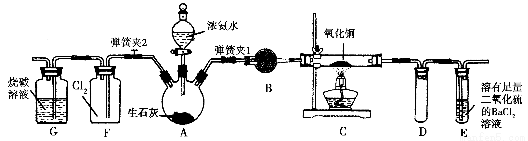
(1)在組裝好裝置后,若要檢驗A~E裝置的氣密性,其操作是首先________,然后微熱A,觀察到E中有氣泡冒出,移開酒精燈或松開雙手,E中導管有水柱形成,說明裝置氣密性良好。
(2)裝置B中盛放的試劑是________。
(3)點燃C處酒精燈,關閉彈簧夾2,打開彈簧夾1,從分液漏斗放出濃氨水至浸沒燒瓶中固體后關閉分液漏斗,稍候片刻,裝置C中黑色固體逐漸變紅,裝置E中溶液里出現大量氣泡,同時產生________(答現象);從E中逸出液面的氣體可以直接排入空氣,請寫出在C中發生反應的化學方程式:________________________。
(4)當C中固體全部變紅色后,關閉彈簧夾1,慢慢移開酒精燈,待冷卻后,稱量C中固體質量,若反應前固體質量為16 g,反應后稱重固體質量減少2.4 g,通過計算確定該固體產物的成分是_________
__________(用化學式表示)。
(5)在關閉彈簧夾1后,打開彈簧夾2,殘余氣體進入F中,很快發現裝置F中產生白煙,同時發現G中溶液迅速倒吸流入F中,寫出產生白煙的化學方程式:____________________,迅速產生倒吸的原因是____________________________。
(1)關閉彈簧夾2和分液漏斗活塞,打開彈簧夾1,在E中裝入水
(2)堿石灰(或生石灰)
(3)白色沉淀 2NH3+3CuO 3Cu+N2↑+3H2O
3Cu+N2↑+3H2O
(4)Cu2O、Cu
(5)3Cl2+8NH3=N2+6NH4Cl
盛滿氯氣的集氣瓶中因氨氣消耗氯氣生成部分固體,導致瓶內壓強減小,引起溶液倒吸
【解析】A是制備NH3的裝置,B是干燥NH3的裝置,C是NH3與CuO的反應裝置,E是處理NH3的尾氣裝置,F是NH3與Cl2的反應裝置,G是處理尾氣Cl2的裝置。
(2)干燥NH3需使用堿性干燥劑。(3)C中CuO與NH3發生氧化還原反應生成紅色的Cu、N2和H2O;E中發生反應:2NH3+BaCl2+SO2+H2O=BaSO3↓+2NH4Cl。(4)若產物全部是Cu,則由差量法知減小的部分全部是O元素的質量,即n(CuO)=n(O)=2.4 g÷16 g·mol-1=0.15 mol,所以反應的CuO的質量為0.15 mol×80 g/mol=12 g<16 g,所以CuO未完全轉化成Cu,剩余固體中可能含有Cu2O。(5)Cl2可將NH3氧化為N2,同時生成的HCl會和NH3反應生成NH4Cl,產生白煙現象,F瓶內壓強變小從而出現倒吸現象。
點撥:本題考查NH3的制備及性質、化學實驗基本操作,考查考生記憶和知識的應用能力。難度中等。


 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 物質的量及其應用練習卷(解析版) 題型:選擇題
下列敘述中正確的是( )
A.相同條件下,N2和O3的混合氣體與等體積的N2所含原子數相等
B.標準狀況下,28 g CO和22.4 L SO3所含分子數相等
C.5.6 g鐵粉與足量氯氣充分反應,有0.2 mol電子轉移
D.等物質的量的CH5+和NH2—所含電子數相等
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 常見無機物及其應用練習卷(解析版) 題型:選擇題
下列說法中正確的是( )
A.硅主要以單質、氧化物、硅酸鹽的形式存在于自然界中
B.青銅是我國使用最早的合金,鋼是用量最大、用途最廣泛的合金
C.漂白粉、漂粉精可用來漂白棉、麻、紙張,不能用作游泳池及環境的消毒劑
D.合成纖維和光導纖維都是高分子化合物
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化工生產流程、無機物的判斷練習卷(解析版) 題型:選擇題
如圖所示是一系列含硫化合物的轉化關系(反應中生成的水已略去),其中說法正確的是( )

A.反應①說明SO2具有漂白性,反應②說明SO2具有酸性
B.反應②中生成物n(Na2SO3):n(NaHSO3)=1:1時,則反應物n(SO2):n(NaOH)=1:2
C.反應③④⑤均屬于氧化還原反應
D.工業上可利用反應②和反應④回收SO2
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化學能與熱能練習卷(解析版) 題型:選擇題
已知25℃時:
①HF(aq)+OH-(aq)=F-(aq)+H2O(l) ΔH1=-67.7 kJ·mol-1
②H+(aq)+OH-(aq)=H2O(l) ΔH2=-57.3 kJ·mol-1
③Ba2+(aq)+SO42—(aq)=BaSO4(s) ΔH3<0
下列說法正確的是( )
A.HF的電離方程式及熱效應:HF(aq)=H+(aq)+F-(aq) ΔH>0
B.在氫氧化鈉溶液與鹽酸的反應中,鹽酸量一定,氫氧化鈉溶液量越多,中和熱越大
C.ΔH2=-57.3 kJ·mol-1是強酸和強堿在稀溶液中反應生成可溶鹽的中和熱
D.稀硫酸與稀氫氧化鋇溶液反應的熱化學方程式為H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)ΔH=-114.6 kJ·mol-1
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化學實驗基礎練習卷(解析版) 題型:選擇題
下列化學實驗事實及其解釋都正確的是( )
A.向KMnO4溶液中滴加鹽酸,KMnO4溶液的氧化能力增強。說明鹽酸具有氧化性
B.向澄清的AlCl3稀溶液中加入NaOH濃溶液,振蕩,溶液仍為澄清。說明該兩種溶液混合是物理變化
C.向FeCl3溶液中加入過量Cu粉,振蕩、靜置,溶液由黃色變為綠色。說明Fe3+具有氧化性
D.向CaCl2溶液中滴入少量Na2CO3溶液,產生白色沉淀。說明CaCO3難溶于水
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化學實驗基礎練習卷(解析版) 題型:選擇題
有一無色透明溶液,可能含有Na+,Al3+,Mg2+,Fe3+,NH4+,Cl-,SO42—,HCO3—中的幾種,取該溶液三份分別進行實驗:①滴加甲基橙溶液顯紅色;②逐漸加入NaOH溶液,產生白色沉淀,最后白色沉淀部分溶解;③加入5 mL 0.1 mol·L-1 BaCl2溶液至不再產生白色沉淀,取上層清液加入足量AgNO3溶液,得到0.2 g沉淀。由此推知,原溶液中( )
A.一定有Al3+,Mg2+,Cl-,SO42—
B.一定沒有Mg2+,Fe3+,HCO3—
C.不能確定是否含有Cl-
D.可能有Na+,NH4+,Cl-,SO42—
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化學基本理論練習卷(解析版) 題型:選擇題
在恒溫恒壓下,向密閉容器中充入4 mol SO2和2 mol O2,發生如下反應:2SO2(g)+O2(g)  2SO3(g) ΔH<0。2 min后,反應達到平衡,生成SO2為1.4 mol,同時放出熱量Q kJ。則下列分析正確的是( )
2SO3(g) ΔH<0。2 min后,反應達到平衡,生成SO2為1.4 mol,同時放出熱量Q kJ。則下列分析正確的是( )
A.在該條件下,反應前后的壓強之比為6?5.3
B.若反應開始時容器體積為2 L,則有v(SO3)=0.35 mol/(L·min)
C.若把“恒溫恒壓下”改為“恒壓絕熱條件下”反應,平衡后n(SO3)<1.4 mol
D.若把“恒溫恒壓下”改為“恒溫恒容下”反應,達平衡時放出熱量大于Q kJ
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化學反應速率與化學平衡練習卷(解析版) 題型:填空題
在1.0 L密閉容器中放入0.10 mol A(g),在一定溫度進行如下反應:A(g)  B(g)+C(g) ΔH=+85.1 kJ·mol-1
B(g)+C(g) ΔH=+85.1 kJ·mol-1
反應時間(t)與容器內氣體總壓強(p)的數據見下表:
時間t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列問題:
(1)欲提高A的平衡轉化率,應采取的措施為________。
(2)由總壓強p和起始壓強P0計算反應物A的轉化率a(A)的表達式為________,平衡時A的轉化率為________,列式并計算反應的平衡常數K________。
(3)①由總壓強p和起始壓強P0表示反應體系的總物質的量n(總)和反應物A的物質的量n(A),n(總)=________mol,n(A)=________mol。
②下表為反應物A濃度與反應時間的數據,計算:a=________。
反應時間t/h | 0 | 4 | 8 | 16 |
c(A)/(mol·L-1) | 0.10 | a | 0.026 | 0.0065 |
分析該反應中反應物的濃度c(A)變化與時間間隔(t)的規律,得出的結論是________,由此規律推出反應在12 h時反應物的濃度c(A)為________mol·L-1。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com