
【題目】下列各能層中不包含P能級的是()
A.NB.KC.LD.M
 通城學典默寫能手系列答案
通城學典默寫能手系列答案科目:高中化學 來源: 題型:
【題目】下列關于物質的性質或用途說法正確的是
A. 鋁的表面易形成致密氧化物薄膜,故鋁制器皿耐腐蝕
B. 合金的硬度和熔點都高于成分金屬
C. SiO2不能與任何酸發生反應
D. 明礬常用于水的凈化和消毒
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法與圖示含義不相符合的是
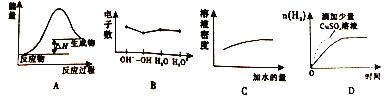
A. 可用圖A表示炭粉和二氧化碳反應的能量變化
B. 可用圖B表示個粒子核外電子數
C. 可用圖C表示硫酸加水稀釋的密度變化
D. 可用圖D表示一定量的硫酸溶液和過量鋅粉反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】金屬鈦性能優越,被稱為繼鐵、鋁之后的“第三金屬”,工業上用鈦礦石(主要成分:FeO、TiO2,SiO2等)為原料制取鈦,工藝流程如下,回答下列問題:

已知:TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O
(1)鈦礦石在加入濃硫酸酸溶前要先粉碎,其目的是__________。
(2)操作1名稱為_______,固體2的主要成分是______, 寫出金屬鈉與TiCl4共熱的化學反應方程式_________________。
(3)一定溫度下,在一個固定容積的容器中發生反應:TiO2(s)+2Cl2(g)+2C(s)![]() TiCl4(g)+2CO(g),反應中氧化劑是________,下列說法能夠說明該反應已達化學平衡狀態的是_________________。
TiCl4(g)+2CO(g),反應中氧化劑是________,下列說法能夠說明該反應已達化學平衡狀態的是_________________。
A.反應每斷裂2個Cl一Cl鍵,同時生成2 個C![]() O鍵
O鍵
B. 容器內壓強不再發生變化
C. Cl2和TiCl4的濃度不再變化
D.v(TiCl4)正=2v(C)逆
(4)將50噸鈦礦石經上述變化后,最終可得金屬鈦12噸,假設各步反應均完全,則原礦石中TiO2的百分含量為_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有A、B、C、D四種元素,其中A和B原子都有1個未成對電子,A+比B-少一個電子層。B原子得一個電子填入3p軌道后,3p軌道已充滿,C原子的p軌道中有3個未成對電子,其氣態氫化物的水溶液的pH在同族氫化物中最大,D的最高化合價和最低化合價的代數和為4,其最高價氧化物中含D 40%,且其核內質子數等于中子數,據此判斷:
(1)D是_______。(填元素名稱)
(2)B-的電子排布式____,A+的結構示意圖____,D原子的軌道表示式______。
(3)在A、B、D三種元素的簡單離子中,其離子還原性最強的是________。(填離子符號)
(4)用電子式表示化合物AB的形成過程________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為實驗室某濃鹽酸試劑瓶標簽上的有關數據,試根據標簽上的有關數據回答下列問題.

(1)該濃鹽酸中HCl的物質的量濃度為 ______ molL-1.
(2)取用任意體積的該鹽酸時,下列物理量中不隨所取體積的多少而變化的是______ .
A.溶液中HCl的物質的量
B.溶液的濃度
C.溶液中Cl-的數目
D.溶液的密度
(3)配制時,其正確的操作順序是(用字母表示,每個字母只能用一次并在操作步驟空白處填上適當儀器名稱) ______ .
A.用30mL水洗滌 ______ 2~3次,洗滌液均注入容量瓶,振蕩
B.用量筒準確量取所需的濃鹽酸的體積,沿玻璃棒倒入燒杯中,再加入少量水(約30mL),用玻璃棒慢慢攪動,使其混合均勻
C.將已冷卻的鹽酸沿玻璃棒注入容量瓶中
D.將容量瓶蓋緊,振蕩,搖勻
E.改用 ______ 加水,使溶液凹液面恰好與刻度線相切
F.繼續往容量瓶內小心加水,直到液面接近刻度線1~2cm處
(4)在配制過程中,下列實驗操作對所配制的稀鹽酸的物質的量濃度有何影響?(在括 號內填“偏大”,“偏小”,或“無影響”)
a.用量筒量取濃鹽酸時俯視觀察凹液面 ______
b.定容后經振蕩、搖勻、靜置,發現液面下降,再加適量的蒸餾水 ______ .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法錯誤的是
A. 在共價化合物中一定含有共價鍵
B. 由非金屬元素組成的化合物一定是共價化合物
C. 含有離子鍵的化合物一定是離子化合物
D. 雙原子單質分子中的共價健一定是非極性鍵
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com