
X、Y、Z、W是元素周期表中原子序數依次增大的四種短周期元素,其相關信息如下表:
| 元素 | 相關信息 |
| X | X的最高價氧化物對應的水化物化學式為H2XO3 |
| Y | Y是地殼中含量最高的元素 |
| Z | Z的基態原子最外層電子排布式為3s23p1 |
| W | W的一種核素的質量數為28,中子數為14 |
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F是原子序數依次增大的同周期元素,已知A、C、F的原子最外層電子數之和為11,且這三種元素的最高價氧化物的水化物之間兩兩皆能反應,均生成鹽和水,D元素原子的次外層電子數比最外層電子數多4個,E元素原子最外層與最內層電子數的差是3,試回答:
(1)寫出下列元素的元素符號:A__________,C________,D__________,E__________。
(2)用電子式表示B和F形成化合物的過程:__________。
(3)寫出A、C、F三種元素最高價氧化物的水化物相互反應的化學方程式__________________,__________________,________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F六種短周期元素,其原子序數依次增大,其中B與C同周期,D與E和F同周期,A與D同主族,C與F同主族,C元素的原子最外層電子數是次外層電子數的三倍,D是所在周期原子半徑最大的主族元素。又知六種元素所形成的常見單質在常溫常壓下有三種是氣體,三種是固體。請回答下列問題:
(1)元素D在周期表中的位置__________。
(2)C、D、F三種元素形成的簡單離子的半徑由大到小的順序是(用離子符號表示)______。
(3)由A、B、C三種元素以原子個數比4∶2∶3形成化合物X,X中所含化學鍵類型有________________________________________________________________________。
(4)若E是金屬元素,其單質與氧化鐵反應常用于焊接鋼軌,請寫出反應的化學方程式:________________________________________________________________________。
若E是非金屬元素,其單質在電子工業中有重要應用,請寫出其氧化物溶于強堿溶液的離子方程式:_______________________________________________________________。
(5)FC2氣體有毒,排放到大氣中易形成酸雨,寫出FC2與氧氣和水蒸氣反應的化學方程式______________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E是5種短周期元素,原子序數逐漸增大,A的最簡單氣態氫化物是一種溫室氣體,A與C、B與C組成的化合物是機動車排出的大氣污染物,C和D能形成原子個數比為1∶1和1∶2的兩種化合物,E的最高價氧化物的水化物分別與B、D的最高價氧化物的水化物反應生成鹽M和N。試回答下列問題:
(1)A在元素周期表中的位置是___,D2C2中含有的化學鍵有____________。
(2)工業合成B的氣態氫化物BH3是放熱反應。下列措施中,既能加快反應速率,又能提高原料轉化率的是________(填字母序號)。實驗室里檢驗BH3的方法是_________________。
a.升高溫度 b.加入催化劑
c.將BH3及時分離出去 d.增大反應體系的壓強
(3)鹽M和鹽N不能同時存在于水溶液中,用離子方程式表示其原因:__。
(4)A的最高價氧化物與D的最高價氧化物的水化物反應生成的正鹽溶液呈________性,其原因是___________________(用離子方程式表示)。
(5)已知:A(s)+C2(g)=AC2(g) ΔH=-393.5 kJ·mol-1
AC(g)+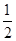 C2(g)=AC2(g) ΔH=-283.0 kJ·mol-1
C2(g)=AC2(g) ΔH=-283.0 kJ·mol-1
則A與C反應生成AC的熱化學方程式為____________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E、F元素是原子序數依次增大的6種短周期元素。已知A是短周期元素中原子半徑最小的元素,A和B形成的18電子的化合物X常用作火箭的燃料,C原子最外層電子數與核外電子總數之比為3∶4,E與C同主族,D和C可以形成原子個數比為1∶1和2∶1的兩種離子化合物。
據此回答下列問題:
(1)D和C形成1∶1的化合物中陰陽離個數比為____________。
(2)化合物X的結構式為____________。1 mol氣態X在適量C2中燃燒,生成B2和氣態A2C, 放出534 kJ的熱量,1 mol液態A2C完全汽化需吸收44 kJ熱量。請寫出氣態X在C2中燃燒生成B2和液態A2C時的熱化學方程式_____________________________________
(3)某化合物由上述6種元素中的3種元素組成,為常見家用消毒劑的主要成分,其中化學鍵類型為__________________;該化合物水溶液不呈中性的原因是(用離子方程式表示)__________________________________,該化合物可以通過電解D和F形成化合物的水溶液獲得,電解時反應的化學方程式為_________________________________
(4)寫出一個可以證明C的非金屬性大于E的化學反應方程式:_____________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
部分中學化學常見元素原子結構及性質如表所示:
| 序號 | 元素 | 結構及性質 |
| ① | A | A單質是生活中常見金屬,它有兩種氯化物,相對分子質量相差35.5 |
| ② | B | B原子最外層電子數是內層電子總數的 |
| ③ | C | C是常見化肥的主要元素,單質常溫下呈氣態 |
| ④ | D | D單質被譽為“信息革命的催化劑”,是常用的半導體材料 |
| ⑤ | E | 通常情況下,E沒有正化合價,A、B、C、D、F都能與E形成化合物 |
| ⑥ | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
W、X、Y、Z是元素周期表中原子前四周期的四種元素,有關它們的信息如下表所示。
| 元素 | 相關信息 |
| W | W的基態原子L層電子數是K層電子數的3倍 |
| X | X與氫元素形成的一種化合物可以使濕潤的紅色石蕊試紙變藍 |
| Y | 單質為黃綠色氣體,最高價氧化物對應的水化物化學式為HYO4 |
| Z | Z的基態原子外圍電子排布式為(n-1)d10ns1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
前四周期原子序數依次增大的元素A、B、C、D中,A和B的價電子層中未成對電子均只有1個,并且A_和B+的電子相差為8;與B位于同一周期的C和D,它們價電子層中的未成對電子數分別為4和2,且原子序數相差為2。回答下列問題:
(1)D2+的價層電子排布圖為_______________。
(2)四種元素中第一電離最小的是_________________,電負性最大的是________________。(填元素符號)
(3)A、B和D三種元素組成的一個化合物的晶胞如圖所示。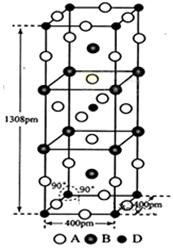
①該化合物的化學式為_____________;D的配位數為_______;
②列式計算該晶體的密度為___________g·cm-3。(列式并計算)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、E五種短周期元素,A與D同周期,A的單質既可與鹽酸反應,又可與NaOH溶液反應,B的單質在放電條件下能與氧氣反應,C元素的離子不含電子,D元素原子的最外層電子數是其次外層電子數的3/4,E元素原子的最外層電子數是其次外層電子數的3倍。
(1)A的原子結構示意圖為 。
(2)0.1 mol/L A的硫酸鹽溶液與0.1 mol/L NaOH溶液等體積混合,反應的離子
方程式為 。
(3)以A的單質和NiO(OH)為電極,NaOH溶液為電解液組成一種新型電池,放電時NiO(OH)轉化為Ni(OH)2,該電池總反應的化學方程式是 。
(4)化合物甲由元素A、B組成,具有良好電絕緣性。
化合物甲能與水緩慢反應生成含B的化合物乙,乙分子中含有10個電子。寫出該
反應的化學方程式: 。
工業用A的單質和化合物乙在高于1700K反應制備甲。已知該反應可以認為是置
換反應,該反應的化學方程式是 。
(5)D和E兩種元素相比較,非金屬性較強的是(填元素名稱) ,可以驗證該結論的是(填寫編號) ;
a.比較這兩種元素的常見單質的沸點
b.比較這兩種元素的單質與氫氣化合的難易
c.比較這兩種元素的氣態氫化物的穩定性
(6)C、D、E間可形成丙、丁兩種分子,它們均含有18個電子,則丙與丁反應生成D單質的化學方程式為 ;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com