
分析 (1)溫度升高C的物質(zhì)的量增大,結(jié)合平衡移動原理分析判斷,升溫平衡向吸熱反應(yīng)方向進行;
(2)在一容積為2L的密閉容器中加入2molA和3molB,保持溫度為30℃,在催化劑存在的條件下進行下列反應(yīng):A(g)+2B(g)3C(g),達到平衡后生成1.2mol C,此時,平衡混合氣中C的體積分數(shù)為ω,依據(jù)化學(xué)平衡三段式列式計算得到;
A(g)+2B(g)=3C(g),
起始量(mol) 2 3 0
變化量(mol) 0.4 0.8 1.2
平衡量(mol) 1.6 2.2 1.2
解答 解:(1)若將溫度升高到70℃后,其他條件均不變,當(dāng)反應(yīng)重新達到平衡時,C的物質(zhì)的量為2.1mol大于30°C生成的C的物質(zhì)的量,說明反應(yīng)正向進行,平衡常數(shù)增大,升溫反應(yīng)向吸熱反應(yīng)方向進行,說明正向反應(yīng)是吸熱反應(yīng),△H>0,
故答案為:增大;>;
(2)在一容積為2L的密閉容器中加入2molA和3molB,保持溫度為30℃,在催化劑存在的條件下進行下列反應(yīng):A(g)+2B(g)3C(g),達到平衡后生成1.2mol C,此時,平衡混合氣中C的體積分數(shù)為ω;
A(g)+2B(g)=3C(g),
起始量(mol) 2 3 0
變化量(mol) 0.4 0.8 1.2
平衡量(mol) 1.6 2.2 1.2
平衡混合氣中C的體積分數(shù)ω=$\frac{1.2mol}{5mol}$×100%=24%;
A物質(zhì)的轉(zhuǎn)化率與B物質(zhì)的轉(zhuǎn)化率之比=$\frac{0.4}{2}$:$\frac{0.8}{3}$=3:4;
故答案為:24%;3:4.
點評 本題考查化學(xué)平衡影響因素的分析判斷,化學(xué)平衡的計算應(yīng)用,等效平衡的分析方法,題目難度中等.


 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學(xué) 來源: 題型:選擇題
| A. | 粗鹽提純 | B. | 蒸餾法將海水淡化為飲用水 | ||
| C. | 活性炭使紅墨水褪色 | D. | 四氯化碳萃取碘水中的碘 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
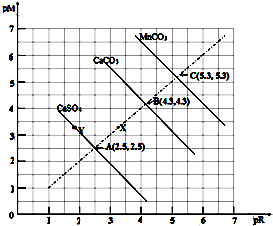
| A. | MnCO3在常溫下的Ksp=2.5 x10-11(已知100.4=2.5) | |
| B. | 三種物質(zhì)在常溫下的溶解度大小順序為MnCO3>CaCO3>CaSO4 | |
| C. | 處于Y點的CaSO4溶液中c(Ca2+)>c(SO42-) | |
| D. | Ca2+、CO32-濃度為X點的溶液可通過蒸發(fā)溶劑變?yōu)锽點的溶液 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
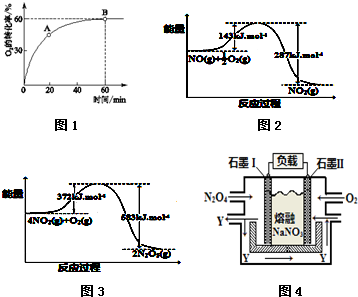
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
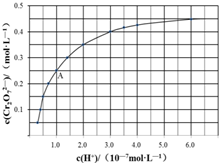 元素鉻(Cr)在溶液中主要以Cr3+(藍紫色)、Cr(OH)4-(綠色)、Cr2O72-(橙紅色)、CrO42-(黃色)等形式存在,Cr(OH)3為難溶于水的灰藍色固體,回答下列問題:
元素鉻(Cr)在溶液中主要以Cr3+(藍紫色)、Cr(OH)4-(綠色)、Cr2O72-(橙紅色)、CrO42-(黃色)等形式存在,Cr(OH)3為難溶于水的灰藍色固體,回答下列問題:查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
| 溫度/℃ | 200 | 250 | 300 | 350 |
| 平衡常數(shù)K | 9.94 | 5.2 | 1 | 0.5 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | 常溫常壓下,28 g 14CO和N2的混合物所含的質(zhì)子數(shù)為14NA | |
| B. | 常溫下,100mL 1mol•L-1 Na2CO3溶液中陰離子總數(shù)大于0.1NA | |
| C. | 將NA個NH3分子溶于1 L水中得到1 mol•L-1的氨水 | |
| D. | 將標況下22.4LC12通入足量NaOH溶液中充分反應(yīng)轉(zhuǎn)移電子數(shù)是2NA |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | KCl | B. | Mg(OH)2 | C. | Na2CO3 | D. | MgSO4 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com