
在相同條件下(500K),相同體積的甲、乙兩密閉容器,甲容器充入1g SO2(g)和1g O2(g),乙容器充入2gSO2(g)和2g O2(g),發生下列反應:2SO2(g)+O2(g) 2SO3(g),下列敘述錯誤的是
2SO3(g),下列敘述錯誤的是
[ ]
A.起始時的化學反應速率:乙>甲
B.平衡后SO3的濃度:乙>甲
C.SO2的轉化率:乙>甲
D.平衡后SO2的體積分數:乙>甲
 點睛新教材全能解讀系列答案
點睛新教材全能解讀系列答案 小學教材完全解讀系列答案
小學教材完全解讀系列答案科目:高中化學 來源: 題型:閱讀理解

| c(CH3CH2OH)?c(H2O) |
| c2(CO)?c4(H2) |
| c(CH3CH2OH)?c(H2O) |
| c2(CO)?c4(H2) |
| 溫度(K) CO2轉化率(%) n(H2)/n(CO2) |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
| n(H2) |
| n(CO2) |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
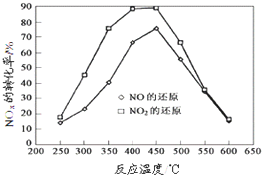 在一定條件下可用SnO2/Al2O3等多種催化劑實現丙烯選擇性還原NOx,
在一定條件下可用SnO2/Al2O3等多種催化劑實現丙烯選擇性還原NOx,查看答案和解析>>
科目:高中化學 來源: 題型:
合成氨生產技術的創立開辟了人工固氮的途徑,對化學工業技術也產生了重大影響。
(1) 500℃、50MPa時,在容積為5L的密閉容器中加入4 mol N2、8 mol H2,反應達平衡時N2的轉化率為25%,該反應的平衡常數為K,則K=__________________。
(2) 500℃、50MPa時,在容積為5L的密閉容器中,按下列配比作為起始物質,達到平衡后N2的轉化率仍為25%的是_____________
A.2molN2+4molH2 B.2molN2+4molH2+ 6molHe
C.4molN2+8molH2+6molHe D.3molN2+5molH2+2molNH3
(3)希臘阿里斯多德大學的 George Marnellos 和 Michael Stoukides,發明了一種合成氨的新方法,在常壓下,把氫氣和用氦氣稀釋的氮氣分別通入一個加熱到570℃的電解池,利用能通過氫離子的多孔陶瓷固體作電解質,氫氣和氮氣在電極上合成了氨,轉化率達到78%,試寫出電解池陰極的電極反應式 。
(4)合成氨工廠常通過測定反應前后混合氣體的密度來確定N2的轉化率。某工廠測得反應前合成塔中N2和H2混合氣體的密度為0.554g·L-1,從合成塔出來的混合氣體在相同條件下密度為0.693g·L-1(密度均在標準狀況下測定),則該合成氨廠N2的轉化率_____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com