
【題目】某小組在探究Fe2+性質的實驗中觀察到異常現象。
實驗Ⅰ | 現象 |
| 溶液變紅,片刻紅色褪去,有氣體生成(經檢驗為O2)。 |
資料:ⅰ.Fe3++3SCN-=Fe(SCN)3(紅色),Fe(SCN)3中S元素的化合價為2價
ⅱ.BaSO4是不溶于鹽酸的白色沉淀
(1)實驗Ⅰ體現了Fe2+的__性,補全H2O2與FeCl2酸性溶液反應的離子方程式:__Fe2+ +__H2O2+__H+ =__Fe3++__H2O
(2)探究“紅色褪去”的原因,進行實驗Ⅱ:將褪色后的溶液分三份分別進行實驗。

實驗Ⅱ得出的結論是:紅色褪去的原因是__。
(3)為進一步探究“紅色褪去”的原因,進行了實驗Ⅲ。
實驗Ⅲ | 現象 |
| 溶液變紅,一段時間后不褪色。 |
取上述反應后的溶液,滴加鹽酸和BaCl2溶液 | 無白色沉淀產生。 |
分析上述三個實驗,下列敘述正確的是__(填字母)。
A.實驗Ⅲ中發生了氧化還原反應:4Fe2++O2+4H+=4Fe3++2H2O
B.通過實驗Ⅲ推出實驗Ⅰ中氧化FeCl2的只有O2
C.O2在該實驗條件下不能使紅色溶液褪色
D.實驗Ⅰ中紅色褪去與H2O2的氧化性有關
(4)上述實驗探究過程用到的實驗方法有__(寫出一條)。
【答案】還原 2 1 2 2 2 SCN-[或Fe(SCN)3]被氧化為SO42- ACD 對比、控制變量等
【解析】
(1)實驗Ⅰ向氯化亞鐵和硫氰化鉀的混合溶液中加入雙氧水,溶液變為血紅色,說明二價鐵被氧化為三價鐵,三價鐵離子與硫氰根離子結合變紅色溶液,體現了Fe2+的還原性;
(2)將褪色后的溶液分三份分別進行實驗對褪色溶液研究,實驗Ⅱ說明溶液中鐵離子沒有變化,有硫酸根離子生成;
(3)為進一步探究“紅色褪去”的原因,進行了實驗Ⅲ,另取同濃度的 FeCl2溶液滴加2滴試劑KSCN溶液,再通入O2,溶液變紅,說明O2能氧化亞鐵離子生成三價鐵離子,取上述反應后的溶液,滴加鹽酸和BaCl2溶液,無白色沉淀產生,說明氧氣不能氧化SCN,則該硫酸根離子由H2O2將SCN氧化成SO42;
(4)實驗Ⅰ和實驗Ⅲ同種(同濃度,同體積)溶液中加入不同的物質,得到不同的反應現象,運用了對比、控制變量的試驗方法。
(1)實驗Ⅰ向氯化亞鐵和硫氰化鉀的混合溶液中加入雙氧水,溶液變為血紅色,說明二價鐵被氧化為三價鐵,三價鐵離子與硫氰根離子結合變紅色溶液,體現了Fe2+的還原性, H2O2與FeCl2酸性溶液反應的離子方程式:2Fe2+ +H2O2 +2H+ =2Fe3++2H2O;
故答案為:還原;2;1;2;2;2;
(2)通過實驗Ⅱ三分溶液的變化現象,說明溶液中鐵離子沒有變化,有硫酸根離子生成,說明實驗Ⅰ中加入的雙氧水將SCN-[或Fe(SCN)3]被氧化為SO42-,
故答案為:SCN-[或Fe(SCN)3]被氧化為SO42-;
(3)另取同濃度的 FeCl2溶液滴加2滴試劑KSCN溶液,再通入O2,溶液變紅,說明O2能氧化亞鐵離子生成三價鐵離子,取上述反應后的溶液,滴加鹽酸和BaCl2溶液,無白色沉淀產生,說明氧氣不能氧化SCN,則該硫酸根離子由H2O2將SCN氧化成SO42;
A. FeCl2溶液滴加2滴試劑KSCN溶液,再通入O2,溶液變紅,說明O2能氧化亞鐵離子生成三價鐵離子實驗Ⅲ中發生了氧化還原反應:4Fe2++O2+4H+=4Fe3++2H2O,故A正確;
B. 通過實驗Ⅲ推出實驗Ⅰ中被氧化FeCl2的有雙氧水,故B錯誤;
C. 滴加鹽酸和BaCl2溶液,無白色沉淀產生,說明氧氣不能氧化SCN,在該實驗條件下不能使紅色溶液褪色,故C正確;
D. 實驗Ⅰ中紅色褪去是由于H2O2將SCN氧化成SO42,因此與H2O2的氧化性有關,故D正確;
故答案為ACD;
(4)實驗Ⅰ和實驗Ⅲ同種(同濃度,同體積)溶液中加入不同的物質,得到不同的反應現象,運用了對比、控制變量的試驗方法,
故答案為:對比、控制變量等。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】已知N≡N、N—H、H—H的鍵能分別為946 kJ·mol-1、391 kJ·mol-1、436 kJ·mol-1。下列說法正確的是( )
A.N2與H2在一定條件下化合生成2 mol NH3時放出的熱量為92 kJ
B.一定條件下合成氨反應N2+3H2![]() 2NH3達平衡時,3v(H2)正=2v(NH3)逆
2NH3達平衡時,3v(H2)正=2v(NH3)逆
C.用液氨和液氧制成的燃料電池放電時可實現將化學能全部轉化為電能
D.反應NH3(g)+HCl(g)=NH4Cl(s)常溫下能自發進行,該反應的ΔH>0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國化學家侯德榜發明的“聯合制堿法”為世界制堿工業做出了巨大貢獻。如圖為聯合制堿法的主要過程(部分物質已略去)。
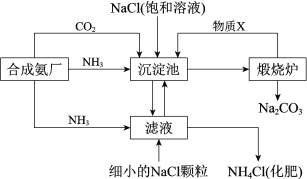
資料:ⅰ.沉淀池中的反應為NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl
ⅱ.溶解度
物質 | NaCl | NH4HCO3 | NaHCO3 | NH4Cl |
20°C溶解度/g | 36.0 | 21.7 | 9.6 | 37.2 |
(1)煅燒爐中反應的化學方程式是___,物質X是___(填化學式)。
(2)下列說法正確的是__(填字母)。
A.沉淀池中有NaHCO3析出,因為一定條件下NaHCO3的溶解度最小
B.濾液中主要含有NaCl、Na2CO3和NH4Cl
C.設計循環的目的是提高原料的利用率
(3)工業可用純堿代替燒堿生產某些化工產品,如用飽和純堿溶液與Cl2反應可制得一種在生產生活中常用于漂白、消毒的物質,同時有NaHCO3生成,該反應的化學方程式是___。
(4)某純堿樣品中含雜質NaCl,取質量為ag的樣品,加入足量的稀鹽酸,充分反應后,加熱、蒸干、灼燒,得到bg固體物質,則此樣品中Na2CO3的質量分數為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組利用H2C2O4溶液和酸性KMnO4溶液的反應探究“外界條件的改變對化學反應速率的影響”,進行了如下實驗:
實驗序號 | 實驗 溫度/K | 有關物質 | 溶液顏色褪至無色所需時間/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
V/mL | c/ mol·L-1 | V mL | c/ mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(1)其中V1=_____、T1=_____;通過實驗_____(填實驗序號)可探究出溫度變化對化學反應速率的影響,其中V2=______。
(2)若t1<8,則由此實驗可以得出的結論是_____;忽略溶液體積的變化,利用實驗B中數據計算,0~8s內,用KMnO4的濃度變化表示的反應速率v(KMnO4)=_______。
(3)該小組的一位同學通過查閱資料發現,上述實驗過程中n(Mn2+)隨時間的變化情況如圖所示,并認為造成這種變化的原因是反應體系中的某種粒子對KMnO4與草酸之間的反應有某種特殊作用,則該作用是_______。
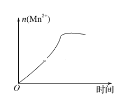
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖裝置中X和Y均為石墨電極,電解液為500mL某CuCl2溶液,電解時X電極表面有紅色固體生成,Y電極有氣體產生。一段時間后,取出X電極,洗滌、干燥、稱量,電極增重1.6g。下列有關說法中正確的是
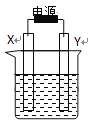
A. X電極連接電源正極
B. 生成氣體體積為0.56L
C. Y電極上發生氧化反應
D. 該CuCl2溶液濃度為0.05mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于相同溫度、相同壓強下,相同物質的量的SO2和SO3,下列說法中正確的是( )
A.硫元素的質量比為5:4B.質量之比為1:1
C.分子數之比為5:4D.密度之比為4:5
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在下列條件的溶液中,各組離子一定能夠大量共存的是( )
A.使酚酞溶液變紅的溶液:Na+、Cl-、SO42-、Fe3+
B.無色透明溶液中:K+、SO42-、MnO4-、H+
C.含有大量OH-的溶液中:Ba2+、Na+、NO3-、Cl-
D.可與鋅反應放出氫氣的溶液中:Na+、Ca2+、Cl-、CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)工業上利用N2和H2合成NH3,NH3又可以進一步制備聯氨(N2H4)等。由NH3制備N2H4的常用方法是NaClO氧化法,其離子反應方程式為___________,有學者探究用電解法制備的效率,裝置如圖,試寫出其陽極電極反應式_________;

(2)乙醇汽油是被廣泛使用的新型清潔燃料,工業生產乙醇(CH3CH2OH)的一種反應原理為:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H=-akJ/mol,己知:CO(g)+H2O(g)
CH3CH2OH(g)+H2O(g) △H=-akJ/mol,己知:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-bkJ/mol,以CO2(g)與H2(g)為原料也可合成氣態乙醇,并放出熱量,寫出該反應的熱化學反應方程式:_________________。
CO2(g)+H2(g) △H=-bkJ/mol,以CO2(g)與H2(g)為原料也可合成氣態乙醇,并放出熱量,寫出該反應的熱化學反應方程式:_________________。
(3)如下圖所示,某研究性學習小組利用上述燃燒原理設計一個肼(N2H4)─空氣燃料電池(如圖甲)并探究某些工業原理,其中乙裝置中X為陽離子交換膜(即只允許陽離子通過)。

根據要求回答相關問題:
①甲裝置中正極的電極反應式為:________________。
②乙裝置中石墨電極產生產物如何檢驗______,電解一段時間后,乙池中的溶液呈___性。
③圖中用丙裝置模擬工業中的________原理,如果電解后丙裝置精銅質量增加3.2g,則理論上甲裝置中肼消耗質量為_____g。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將HI(g)置于密閉容器中,某溫度下發生下列變化:2HI(g)H2(g)+I2(g) △H<0
(1)該反應平衡常數的表達式為K=___。
(2)當反應達到平衡時c(I2)=0.5mol/L,c(HI)=4mol/L,則c(H2)為____,HI的分解率為____。
(3)若該反應800℃時達到平衡狀態,且平衡常數為1.0,某時刻,測得容器內各物質的溶度分別為c(HI)=2.0mol/L,c(I2)=1.0mol/L,c(H2)=1.0mol/L,則該時刻,反應向____(填“正向”或“逆向”,下同)進行。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com