
【題目】哈爾濱醫(yī)科大學附屬第一醫(yī)院張亭棟教授被認為最有可能獲諾貝爾生理學或醫(yī)學獎的學者之一,他是使用砒霜(As2O3)治療白血病的奠基人,回答下列問題:
(1)基態(tài)As原子核外電子排布中能級最高的是___________,與As同周期且相鄰原子的第一電離能由大到小的順序為___________。
(2)NH3的沸點比PH3___________(填“高”或“低”),原因是___________。
(3)NH5中所有原子最外層都滿足穩(wěn)定結(jié)構(gòu),則NH5中含有的化學鍵類型為___________。
A、離子鍵 B、配位鍵 C、共價鍵 D、氫鍵 E、σ鍵 F、π鍵
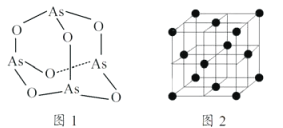
(4)As4O6的分子結(jié)構(gòu)如圖1所示,則該化合物中As的雜化方式是__________。與AsO43-互為等電子體的微粒是___________(寫一種)
(5)白磷(P4)的晶體屬于分子晶體,其晶胞結(jié)構(gòu)如圖2(小黑點表示白磷分子),已知晶胞的邊長為anm,阿伏加德羅常數(shù)為 NAmol-1,則該晶胞中含有的P4分子數(shù)為___________,該晶體的密度為___________g·cm-3(用含NA、a的式子表示)。
【答案】4p As>Se>Ge 高 NH3分子間存在氫鍵 ABCE sp3 PO43-或SO42-或ClO4- 4 ![]()
【解析】
(1)根據(jù)構(gòu)造原理,基態(tài)As原子核外電子排布中能級最高的是4p,As的4p能級處于半充滿狀態(tài),第一電離能比相鄰同期元素均大,與As同周期且相鄰原子的第一電離能由大到小的順序為As>Se>Ge。
(2)根據(jù)分子晶體影響沸點的因素分析;
(3)NH5是離子化合物,含有離子鍵和共價鍵,以此分析。
(4)根據(jù)雜化軌道理論判斷中心As的雜化方式;原子總數(shù)和價電子總數(shù)相同的稱為等電子體。
(5)根據(jù)均攤法可知,晶胞中P4分子數(shù)目為4,則晶胞中含有16個P原子,計算晶胞質(zhì)量,再根據(jù)ρ=m/V計算晶胞密度。
(1)根據(jù)構(gòu)造原理,基態(tài)As原子核外電子排布中能級最高的是4p,As的4p能級處于半充滿狀態(tài),第一電離能比相鄰同期元素均大,與As同周期且相鄰原子的第一電離能由大到小的順序為As>Se>Ge。
(2)NH3的沸點比PH3高,原因是NH3分子間存在氫鍵,相對分子質(zhì)量對沸點的影響占次要地位。
(3)NH5中所有原子最外層都滿足穩(wěn)定結(jié)構(gòu),其中N與H形成共價鍵,是σ鍵,4個共價鍵中有一個是配位鍵,NH4+與H-之間形成離子鍵,則NH5中含有的化學鍵類型為A B C E 。
(4)價電子對數(shù)=3+(5-1×3)/2=4,VSEPR模型為四面體,所以其空間構(gòu)型為正四面體,根據(jù)雜化軌道理論,中心As的雜化方式為sp3,原子總數(shù)和價電子總數(shù)相同的稱為等電子體,與AsO43-互為等電子體的微粒是PO43-或SO42-或ClO4- ;
(5)根據(jù)均攤法可知,晶胞中P4分子數(shù)目為8×1/8+6×1/2=4,則晶胞中P原子數(shù)目為4×4=16,晶胞質(zhì)量為16×31/NAg,晶胞體積為(a×10-7 cm)3,則晶胞密度為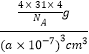 g·cm-3,即:
g·cm-3,即:![]() g·cm-3
g·cm-3


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】有機高分子材料M的結(jié)構(gòu)簡式為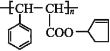 ,下圖是由有機物A(分子式為C5H8O)和苯甲醛為原料生產(chǎn)該有機物的合成路線。
,下圖是由有機物A(分子式為C5H8O)和苯甲醛為原料生產(chǎn)該有機物的合成路線。
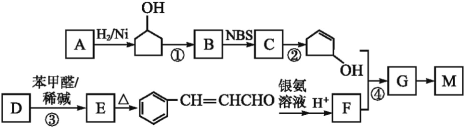
已知:①A分子中有兩種不同環(huán)境的氫原子
②CH3CH2CH![]() CH2
CH2![]() CH3CHBrCH
CH3CHBrCH![]() CH2
CH2
CH3CHO+CH3CHO![]()
![]()
![]()
![]() CH3CH
CH3CH![]() CHCHO+H2O
CHCHO+H2O
請回答以下問題:
(1)A的結(jié)構(gòu)簡式為____,B的名稱為____,F中所含官能團的名稱是__________。
(2)①和③的反應類型分別是____、____;反應②的反應條件為_____________。
(3)反應④的化學方程式為_____________________________________________。
(4)有機物E有多種同分異構(gòu)體,其中同時符合下列條件的同分異構(gòu)體有___種。
①屬于芳香酯類 ②其酸性水解產(chǎn)物遇FeCl3顯紫色
(5)以1-丙醇和NBS為原料可以制備聚丙烯醇(![]() )。請設計合成路線(其他無機原料任選)并用如下方式表示_____________________。
)。請設計合成路線(其他無機原料任選)并用如下方式表示_____________________。
A![]() B……
B……![]() 目標產(chǎn)物
目標產(chǎn)物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
鐵氮化合物(FexNy)在磁記錄材料領域有著廣泛的應用前景。某FexNy的制備需鐵、氮氣、丙酮和乙醇參與。
(1)Fe3+基態(tài)核外電子排布式為____________________。
(2)丙酮(![]() )分子中碳原子軌道的雜化類型是_______________,1 mol 丙酮分子中含有σ鍵的數(shù)目為______________。
)分子中碳原子軌道的雜化類型是_______________,1 mol 丙酮分子中含有σ鍵的數(shù)目為______________。
(3)C、H、O 三種元素的電負性由小到大的順序為________________。
(4)乙醇的沸點高于丙酮,這是因為____________________。
(5)某FexNy的晶胞如題21圖-1所示,Cu可以完全替代該晶體中a位置Fe或者b位置Fe,形成Cu替代型產(chǎn)物Fe(x-n) CunNy。FexNy轉(zhuǎn)化為兩種Cu替代型產(chǎn)物的能量變化如題21圖-2 所示,其中更穩(wěn)定的Cu替代型產(chǎn)物的化學式為___________。
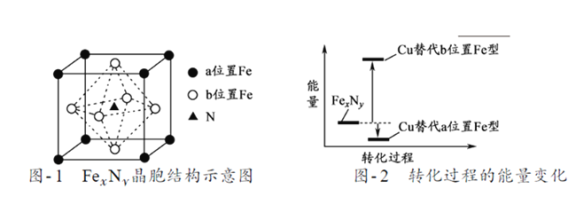
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數(shù)的值,下列說法正確的是
A. 1L0.5mol·L-1NH4C1溶液中含有NH4+的數(shù)目為0.5NA
B. 25℃時,pH=12的NaOH溶液含有的OH-數(shù)目為0.01NA
C. 32g18O2中含有的氧原子數(shù)是2NA
D. 質(zhì)量均為78g的Na2O2和Na2S固體,其離子總數(shù)均為3NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,向某Na2CO3溶液中加入稀鹽酸,溶液中含碳微粒的物質(zhì)的量分數(shù)(φ)隨溶液pH變化的部分情況如圖所示。下列說法中正確的是
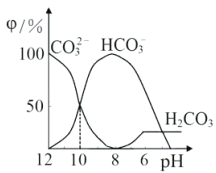
A. pH=7時, c(Na+)=(Cl- )+c(HCO3-)+2c(CO32-)
B. pH=8時,c(Na+)=c(C1-)
C. pH=12時, c(Na+ )>c(OH- )>c(CO32-)>c(HCO3-)>c(H+)
D. 25℃時,CO32-+H2O![]() HCO3-+OH-的水解平衡常數(shù)Kh=10-10mol·L-1
HCO3-+OH-的水解平衡常數(shù)Kh=10-10mol·L-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H是合成抗炎藥洛縈洛芬鈉的關鍵中間體,它的一種合成路線如下:
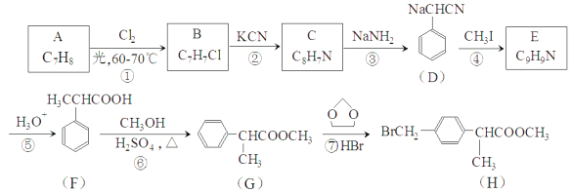
(1)A的物質(zhì)名稱為___________,H中官能團名稱是___________。
(2)E的結(jié)構(gòu)簡式為___________,反應②的反應類型為___________。
(3)反應①的化學方程式為___________,反應⑥的化學方程式為___________。
(4)寫出滿足下列條件的F的同分異構(gòu)體的結(jié)構(gòu)簡式___________。
I.能發(fā)生水解反應生成酸和醇
Ⅱ.能發(fā)生銀鏡反應
Ⅲ.核磁共振氫譜有5組峰且峰面積之比為3:2:2:2:1
(5)仿照H的合成線,設計一種由![]() 合成
合成![]() 的合成路線______________________。
的合成路線______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)從1L1mol/LNaOH溶液中取出100mL,則這100mLNaOH溶液的物質(zhì)的量濃度是____mol/L,含NaOH的質(zhì)量____g。
(2)某同學將標準狀況下44.8L的HCl氣體溶于水,配成500mL的溶液,該HCl氣體的物質(zhì)的量為______,可知所配成的鹽酸溶液的物質(zhì)的量濃度為_____。
(3)在標準狀況下15gCO與CO2的混合氣體,體積為11.2L。則:
①混合氣體的密度是_____。
②混合氣體的平均摩爾質(zhì)量是______。
③CO2和CO的體積之比是_______。
④CO的體積分數(shù)是______。
⑤CO2和CO的質(zhì)量之比是_______。
⑥CO的質(zhì)量分數(shù)是______。
⑦混合氣體中所含氧原子的物質(zhì)的量是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數(shù)的值,下列說法正確的是
A. 粗銅精煉中,外電路轉(zhuǎn)移電子數(shù)為NA時,陽極質(zhì)量減小32g
B. 5.6gFe與足量的硫充分反應,轉(zhuǎn)移電子數(shù)為0.3NA
C. 室溫下,醋酸銨的水溶液呈中性,溶液中所含H+數(shù)目為10-7NA
D. S8分子結(jié)構(gòu)如圖,1mol該分子中含有S—S鍵個數(shù)為8NA
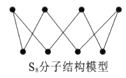
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知2SO2(g)+O2(g)![]() 2SO3(g) △H=-197kJ·mol-1。向同溫、同體積的三個密閉容器中分別充入氣體:(甲)2molSO2和lmolO2;(乙) lmolSO2和0.5molO2;(丙)2 mol SO3。恒溫、恒容下反應達平衡時,下列關系一定正確的是
2SO3(g) △H=-197kJ·mol-1。向同溫、同體積的三個密閉容器中分別充入氣體:(甲)2molSO2和lmolO2;(乙) lmolSO2和0.5molO2;(丙)2 mol SO3。恒溫、恒容下反應達平衡時,下列關系一定正確的是
A. 容器內(nèi)壓強P:P甲=P丙>2P乙
B. SO3的質(zhì)量m:m甲=m丙>2m乙
C. c(SO2)與c(O2)之比 k:k甲=k丙>k乙
D. 反應放出或吸收熱量的數(shù)值Q:Q甲=Q丙>2Q乙
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com