
分析 (1)開始時加入A物質m mol,B物質n mol,起始量符合化學方程式系數之比,依據轉化率是轉化量除以起始量計算分析;
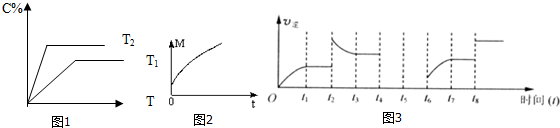
(2)根據先拐先平衡,如圖1中T1<T2,溫度高C的百分含量也大,所以升溫平衡向正反應方向移動,故正反應為吸熱反應;
(3)根據圖乙可知,從正反應開始達到化學平衡過程中,混合氣體的平均相對分子質量逐漸增大的,而反應中氣體質量是守恒的,所以m+n>p+q,
①若在恒溫恒容的條件下,向該平衡體系中再通入A、B、C、D1mol,即相當于對原平衡加壓,平衡向正反應方向移動,氣體的平均相對分子質量會增大,據此答題;
②若恒溫恒壓的條件下,向原平衡體系中再通入A、B、C、D各1mol,相當于體積增大到原來的2倍,氣體的總質量也為原來的2倍,平衡不移動,氣體的密度也不變,據此答題;
(4)根據速率圖象分析,t2時逆反應速率瞬間變大,所以可能增加了生成物的量;根據t4時降壓,t5時達到平衡,t6時增大反應物的濃度,分析繪制圖象.
解答 解:(1)開始時加入A物質m mol,B物質n mol,起始量符合化學方程式系數之比,轉化率是轉化量除以起始量計算,所以A、B的轉化率相等,故答案為:相等;
(2)根據先拐先平衡,如圖1中T1<T2,溫度高C的百分含量也大,所以升溫平衡向正反應方向移動,故正反應為吸熱反應,故答案為:<;>;
(3)根據圖乙可知,從正反應開始達到化學平衡過程中,混合氣體的平均相對分子質量逐漸增大的,而反應中氣體質量是守恒的,根據n=$\frac{m}{M}$知該反應是一個氣體體積減小的反應,即m+n>p+q,
①若在恒溫恒容的條件下,向該平衡體系中再通入A、B、C、D1mol,即相當于對原平衡加壓,平衡向正反應方向移動,氣體的平均相對分子質量會增大,
故答案為:增大;
②若恒溫恒壓的條件下,向原平衡體系中再通入A、B、C、D各1mol,相當于體積增大到原來的2倍,平衡不移動,氣體的密度也不變,故答案為:不變;
(4)據速率圖象分析,t2時逆反應速率瞬間變大,所以可能增加了生成物的量,故答案為:增大生成物的濃度.
點評 本題考查連續多個條件改變引起v-t圖的變化,反應速率、化學平衡影響因素,圖象的理解應用和平衡移動原理實質是解題關鍵,題目難度中等.


 新課標快樂提優暑假作業陜西旅游出版社系列答案
新課標快樂提優暑假作業陜西旅游出版社系列答案 暑假銜接培優教材浙江工商大學出版社系列答案
暑假銜接培優教材浙江工商大學出版社系列答案科目:高中化學 來源:2016-2017學年山東省高一上10月月考化學試卷(解析版) 題型:填空題
同溫同壓下,相同體積的氫氣和氣體A的質量分別是0.2g和3.4g,則氣體A的摩爾質量為 。A的分子數為 。
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
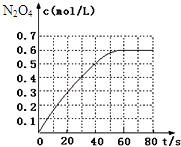 298K時,在2L固定體積的密閉容器中,發生可逆反應:2NO2(g)?N2O4(g)△H=-a kJ/mol (a>0).N2O4的物質的量濃度隨時間變化如圖.達平衡時,N2O4的濃度為NO2的2倍,若反應在398K進行,某時刻測得n(NO2)=0.6mol、n(N2O4)=1.2mol,則此時,下列大小關系正確的是( )
298K時,在2L固定體積的密閉容器中,發生可逆反應:2NO2(g)?N2O4(g)△H=-a kJ/mol (a>0).N2O4的物質的量濃度隨時間變化如圖.達平衡時,N2O4的濃度為NO2的2倍,若反應在398K進行,某時刻測得n(NO2)=0.6mol、n(N2O4)=1.2mol,則此時,下列大小關系正確的是( )| A. | v(正)>v(逆) | B. | v(正)<v(逆) | ||
| C. | v(正)=v(逆) | D. | v(正)、v(逆)大小關系不確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+ | B. | Al3+ | C. | Fe3+ | D. | Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 離子 | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 1 | 4 | 4 | 1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .乙的單質的電子式為
.乙的單質的電子式為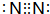 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
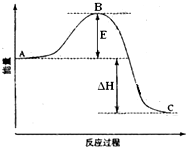 2SO2(g)+O2(g)═2SO3(g)反應過程的能量變化如圖所示.已知1mol SO2(g)氧化為1mol SO3(g)的△H=-99kJ•mol-1.請回答下列問題:
2SO2(g)+O2(g)═2SO3(g)反應過程的能量變化如圖所示.已知1mol SO2(g)氧化為1mol SO3(g)的△H=-99kJ•mol-1.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com