
【題目】25℃ 時,三種酸的電離平衡常數如下:
化學式 | CH3COOH | H2CO3 | HClO |
電離平衡常數 | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
回答下列問題:
(1)一般情況下,當溫度升高時,Ka________(填“增大”、“減小”或“不變”)。
(2)下列四種離子結合質子能力由大到小的順序是___________________(填字母)。
a.CO32- b.ClO- c.CH3COO- d.HCO3-
(3)下列反應不能發生的是________(填字母)。
a. 2ClO-+CO2+H2O = CO32-+2HClO
b. ClO-+CH3COOH = CH3COO-+HClO
c. CO32-+2HClO = CO2↑+H2O+2ClO-
d. CO32-+2CH3COOH = 2CH3COO-+CO2↑+H2O
(4)用蒸餾水稀釋0.10mol·L-1的醋酸,下列各式表示的數值隨水量的增加而增大的是________(填字母)。
a.c(CH3COOH)/c(H+) b.c(CH3COO-)/c(CH3COOH) c.c(H+)/Ka d.c(H+)/c(OH-)
(5)體積均為10 mL、pH均為2的醋酸溶液與HX溶液分別加水稀釋至1000 mL,稀釋過程中pH變化如圖所示。

則醋酸的電離平衡常數________(填“>”、“=”或“<”,下同)HX的電離平衡常數;稀釋后,醋酸溶液中水電離出來的c(H+)____ HX溶液中水電離出來的c(H+);用同濃度的NaOH溶液分別中和上述兩種酸溶液,恰好中和時消耗NaOH溶液的體積:醋酸________HX。
(6)25℃時,若測得CH3COOH與CH3COONa的混合溶液的pH=6,則溶液中c(CH3COO-)-c(Na+)=________mol·L-1(填精確數值)。
【答案】增大 a>b>d>c cd b > > > 9.9×10-7 moL·L-1
【解析】
(1)升高溫度促進弱電解質的電離;
(2)酸根離子對應的酸的酸性越強,酸根離子結合氫離子的能力越弱;
(3)酸性強弱為CH3COOH > H2CO3> HClO > HCO3-,強酸能夠制取弱酸,據此對各選項進行判斷;
(4)醋酸是弱電解質,加水稀釋醋酸,促進醋酸電離,則n(CH3COO-)、n(H+)增大,n(CH3COOH)減小,但醋酸根離子、氫離子濃度增大的程度小于溶液體積增大的程度,所以n(CH3COO-)、n(H+)、n(CH3COOH)都減小,據此分析解答;
(5)加水稀釋促進弱酸電離,pH相同的不同酸稀釋相同的倍數,pH變化大的酸酸性強,變化小的酸酸性弱;酸或堿抑制水電離,酸中氫離子或堿中氫氧根離子濃度越大其抑制水電離程度越大;酸性不同的兩種一元弱酸,體積相同,pH相同,酸越弱,濃度越大,中和時消耗的氫氧化鈉越多;
(6)根據混合液中的電荷守恒計算。
(1)升高溫度促進弱電解質的電離,所以當溫度升高時,Ka增大;
因此,本題正確答案是:增大;
(2)電離平衡常數越大,越易電離,溶液中離子濃度越大,則酸性強弱為:CH3COOH > H2CO3> HClO > HCO3-,酸根離子對應的酸的酸性越強,酸根離子結合氫離子的能力越弱,則四種離子結合質子的能力由大到小的順序是:CO32->ClO- >HCO3- >CH3COO- ,即a>b>d>c,
因此,本題正確答案是:a>b>d>c;
(3) a. CO32-+2CH3COOH=2CH3COO-+CO2↑+H2O:碳酸的酸性小于CH3COOH,所以CH3COOH能夠制取碳酸,該反應能夠發生,故a錯誤;
b. ClO-+CH3COOH=CH3COO-+HClO:CH3COOH的酸性大于HClO,CH3COOH能夠制取HClO,該反應能夠發生,故b錯誤;
c. CO32-+2HClO=CO2↑+H2O+2ClO-:HClO的酸性小于碳酸,該反應無法發生,故c正確;
d. 2ClO-+CO2+H2O=CO32-+2HClO:因為酸性H2CO3> HClO > HCO3-,則碳酸與次氯酸根離子反應只能生成碳酸氫根離子,不會生成CO32-,該反應不能發生,故d正確;
因此,本題正確答案是:cd;
(4)a.加水稀釋醋酸促進醋酸電離,氫離子物質的量增大,醋酸分子的物質的量減小,所以![]() 的比值減小,故a錯誤;
的比值減小,故a錯誤;
b.加水稀釋醋酸促進醋酸電離,醋酸根離子物質的量增大,醋酸分子的物質的量減小,則![]() 的比值增大,故b正確;
的比值增大,故b正確;
c.加水稀釋促進醋酸電離,但氫離子濃度減小,溫度不變,水的離子積常數不變,所以![]() 的比值減小,故c錯誤;
的比值減小,故c錯誤;
d.加水稀釋醋酸促進醋酸電離,氫離子濃度減小,溫度不變,水的離子積常數不變,則氫氧根離子濃度增大,![]() 的比值減小,故d錯誤;
的比值減小,故d錯誤;
因此,本題正確答案是:b;
(5)加水稀釋促進弱酸電離,pH相同的不同酸稀釋相同的倍數,pH變化大的酸酸性強,變化小的酸酸性弱;酸或堿抑制水電離,酸中氫離子或堿中氫氧根離子濃度越大其抑制水電離程度越大,根據圖知,pH相同的醋酸和HX稀釋相同的倍數,HX的pH變化大,則HX的酸性大于醋酸,所以HX的電離平衡常數大于常數,稀釋后醋酸中氫離子濃度大于HX,
因此,本題正確答案是:>;>;>;
(6)pH=6,則c(H+)=10-6mol/L、c(OH-)=10-8mol/L,
溶液呈存在電荷守恒:c(CH3COO-)+c(OH-)=c(H+)+c(Na+),
則:c(CH3COO-)- c(Na+)=c(H+)-c(OH-) =10-6mol/L-10-8mol/L=9.9×10-7mol/L,
因此,本題正確答案是:9.9×10-7mol/L。


科目:高中化學 來源: 題型:
【題目】已知:4NH3+5O2==4NO+6H2O,若反應速率分別用v(NH3)、v(O2)、v(NO)、v(H2O)表示,單位都為mol/(Ls),則正確的關系是
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 是一種重要的化工原料,可用于合成可降解的高聚物C以及抗腫瘤藥物G。
是一種重要的化工原料,可用于合成可降解的高聚物C以及抗腫瘤藥物G。
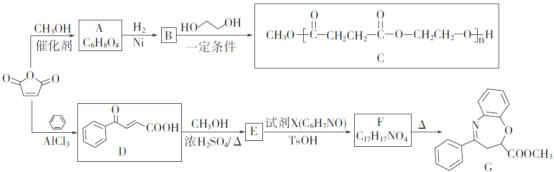
已知: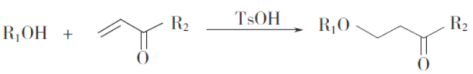
(1)A含有的官能團名稱是______________。
(2)D→E的反應類型是_____________________。
(3)E的分子式是____________;F的結構簡式是_________________。
(4)B→C的化學方程式為________________________________________。
(5)W是B的同分異構體,0.5mol W與足量碳酸氫鈉溶液反應生成44g CO2,W共有______種(不考慮立體異構),其中核磁共振氫譜為三組峰的結構簡式為___________。
(6)設計由甲苯和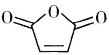 為原料制備化合物
為原料制備化合物![]() 的合成路線(無機試劑任選)______。
的合成路線(無機試劑任選)______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】新冠病毒爆發期間,各類消毒劑大顯身手,ClO2泡騰片就是一種,使用時將其投入水中即可產生ClO2對水體、環境消毒。已知ClO2是一種易溶于水而難溶于有機溶劑的氣體,實驗室制備ClO2的原理是用亞氯酸鈉固體與氯氣反應:2NaClO2+Cl2=2ClO2+2NaCl。如圖是實驗室用于制備和收集一定量純凈的ClO2的裝置(某些夾持裝置和墊持用品省略)。其中E中盛有CCl4液體(用于除去ClO2中的未反應的Cl2)。


(1)儀器P的名稱是__。
(2)寫出裝置A中燒瓶內發生反應的離子方程式__。
(3)B裝置中所盛試劑是__。
(4)F為ClO2收集裝置,應選用的裝置是__(從①②③中選擇),其中與E裝置導管相連的導管口是__(填導管口的字母)
(5)相同條件下,ClO2的消毒能力是Cl2的__倍(以等物質的量的消毒劑得電子的數目計算)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】機動車排放的污染物主要有碳氫化合物、一氧化碳和氮氧化物等。
I.汽油燃油車上安裝三元催化轉化器,可有效降低汽車尾氣污染。
(1)已知:C(s)+O2(g) == CO2(g) △H1 = 393.5kJ·mol1
2C(s)+O2(g) == 2CO(g) △H2 = 221.0 kJ·mol1
N2(g)+O2(g) == 2NO(g) △H 3 = +180.5 kJ·mol1
CO和NO兩種尾氣在催化劑作用下生成N2(g)的熱化學方程式是______。
(2)研究CO和NO的催化反應,用氣體傳感器測得在某溫度下、一定體積的密閉容器中,不同時間NO和CO濃度如下表:
時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(104mol·L1) | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
c(CO)/(103mol·L1) | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
①前4 s內的平均反應速率υ(CO) =______mol·L1·s1。
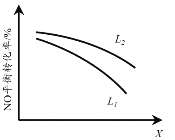
②L、X可分別代表壓強或溫度。下圖表示L一定時,NO(g)的平衡轉化率隨X的變化關系。X代表的物理量是______。判斷L1、L2的大小關系,并簡述理由:______。
II.柴油燃油車是通過尿素-選擇性催化還原(Urea-SCR)法處理氮氧化物。
Urea-SCR的工作原理為:尿素[CO(NH2)2]水溶液通過噴嘴噴入排氣管中,當溫度高于160℃時尿素水解,產生 NH3,生成的NH3與富氧尾氣混合后,加入適合的催化劑,使氮氧化物得以處理。
(3)尿素水解的化學方程式是______。
(4)下圖為在不同投料比[n(尿素)/n(NO)]時NO轉化效率隨溫度變化的曲線。
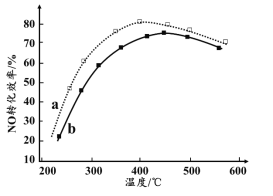
① 尿素與NO物質的量比a______b(填“>”、“=”或“<”)
② 由圖可知,溫度升高,NO轉化效率升高,原因是______。溫度過高,NO轉化效率下降,NO的濃度反而升高,可能的原因是______(寫出一種即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知可逆反應X(g)+2Y(g)![]() Z(g) ΔH <0,一定溫度下,在體積為2 L的密閉容器中加入4 mol Y和一定量的X后,X的濃度隨時間的變化情況如圖所示,則下列說法正確的是( )
Z(g) ΔH <0,一定溫度下,在體積為2 L的密閉容器中加入4 mol Y和一定量的X后,X的濃度隨時間的變化情況如圖所示,則下列說法正確的是( )

A. 若向該容器中加入1molX、2molY,達平衡時,X的平衡濃度小于0.125mol/L
B. a點正反應速率大于逆反應速率
C. 反應達平衡時,降低溫度可以實現c到d的轉化
D. 該條件下,反應達平衡時,平衡常數K=3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】三鹽基硫酸鉛(3PbO·PbSO4·H2O,其相對分子質量為990)簡稱“三鹽”,不溶于水及有機溶劑。以鉛泥(PbSO4、PbO、Pb及其他雜質等)為原料制備三鹽的工藝流程如下圖所示
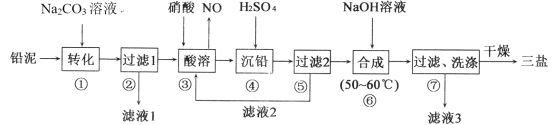
已知:KSP(PbSO4)=1.82×10-8,KSP(PbCO3)=1.46×10-13請回答下列問題:
(1)寫出步驟①“轉化”的主要離子方程式_______。
(2)根據圖溶解度曲線,由濾液I得到Na2SO4固體的操作為:將“濾液1”________、______、用乙醇洗滌后干燥。
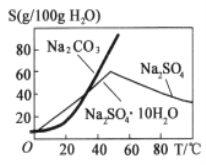
(3)步驟③“酸溶”,為提高酸溶速率,可采取的措施是____________(任意寫出一條)
(4)“濾液2”中可循環利用的溶質為___(填化學式)。若步驟④“沉鉛”后的濾液中c(Pb2+)=1.82×10-5 mol·L-1,則此時c(SO42-)=____mol·L-1。
(5)步驟⑥“合成”三鹽的化學方程式為___________。
(6)若消耗100 t鉛泥,最終得到純凈干燥的三鹽49.5 t,假設鉛泥中的鉛元素有75.0%轉化為三鹽,則鉛泥中鉛元素的質量分數為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】通常情況下,微粒A和B為分子,C和E為陽離子,D為陰離子,它們都含有10個電子;B溶于A后所得的物質可電離出C和D;B溶于A后所得的物質與E微粒反應后可得C和一種白色沉淀。請回答:
(1)A的結構式為______________。
(2)B的電子式為______________。
(3)D的電子式為______________。
(4)B溶于A后所得的物質與E微粒反應后可得C和一種白色沉淀,寫出該反應的離子方程式____________________________(寫一個即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于下列實驗事實的解釋,不合理的是
選項 | 實驗事實 | 解釋 |
A | 加熱蒸干MgSO4溶液能得到MgSO4固體;加熱蒸干MgCl2溶液得不到MgCl2固體 | H2SO4不易揮發,HCl易揮發 |
B | 電解CuCl2溶液陰極得到Cu;電解NaCl溶液,陰極得不到Na | 得電子能力:Cu2+>Na+>H+ |
C | 濃HNO3能氧化NO;稀HNO3不能氧化NO | HNO3濃度越大,氧化性越強 |
D | 鈉與水反應劇烈;鈉與乙醇反應平緩 | 羥基中氫的活潑性:H2O> C2H5OH |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com