
| A. | “地溝油”可以制成肥皂,提高資源的利用率 | |
| B. | 食品中大量添加苯甲酸鈉等防腐劑,可有效延長其保質期 | |
| C. | 加快開發高效潔凈能源轉換技術,緩解能源危機 | |
| D. | “APEC藍”是2014年新的網絡詞匯,形容2014年APEC會議期間北京藍藍的天空,說明京津冀實施道路限行和污染企業停工等措施,對減輕霧霾、保證空氣質量是有效的 |
分析 A.將“地溝油”制成肥皂,可以變廢為寶;
B.添加食品防腐劑應按規定的添加量使用才安全;
C.高效潔凈能源是對生態環境低污染或無污染的能源;
D.道路限行可減少汽車尾氣排放,污染企業停工可減少污染.
解答 解:A.“地溝油”,是一種質量極差、極不衛生的非食用油,將它制成肥皂,實際是使用了油脂的皂化反應,將非食用油變成肥皂,可以提高資源的利用率,故A錯誤;
B.添加食品防腐劑的目的是為了改善食品品質、延長保存期、方便加工和保全營養成分,按規定的添加量使用才是安全的,大量添加,會改變食品的結構和組成,使食品變的不安全,如亞硝酸鹽,過量會致癌,大量添加苯甲酸鈉,會改變食品的口味和營養成分,故B正確;
C.清潔能源技術是指在可再生能源及新能源如煤的清潔高效利用等領域開發的對生態環境低污染或無污染的新技術,加快高效潔凈能源轉換技術的開發,能緩解能源危機,故C正確;
D.道路限行可減少汽車尾氣排放,污染企業停工可減少污染,可減輕霧霾、保證空氣質量,故D正確;
故選A.
點評 本題考查了常見食品添加劑、地溝油等生活中常見的物質的性質,根據相關的知識進行解答,題目較簡單.


科目:高中化學 來源: 題型:解答題
 科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以甲醇為燃料的燃料電池.已知H2(g)、CO(g)和CH3OH(l)的燃燒熱△H分別為-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol.請回答下列問題:
科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以甲醇為燃料的燃料電池.已知H2(g)、CO(g)和CH3OH(l)的燃燒熱△H分別為-285.8kJ/mol、-283.0kJ/mol和-726.5kJ/mol.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
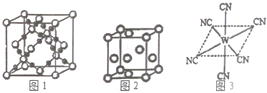 已知A、B、C、D、E、W六種元素的原子序數依次遞增,都位于前四周期.其中A、D原子的最外層電子數均等于其周期序數,且D原子的電子層數是A的3倍;B原子核外電子有6種不同的運動狀態,且s軌道電子數是p軌道電子數的兩倍;C原子L層上有2對成對電子.E有“生物金屬”之稱,E4+離子和氬原子的核外電子排布相同;W位于周期表中第8列,請回答:
已知A、B、C、D、E、W六種元素的原子序數依次遞增,都位于前四周期.其中A、D原子的最外層電子數均等于其周期序數,且D原子的電子層數是A的3倍;B原子核外電子有6種不同的運動狀態,且s軌道電子數是p軌道電子數的兩倍;C原子L層上有2對成對電子.E有“生物金屬”之稱,E4+離子和氬原子的核外電子排布相同;W位于周期表中第8列,請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 實驗裝置 | 實驗目的 |
| A | 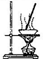 | 加熱硫酸銅晶體獲得無水硫酸銅 |
| B | 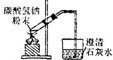 | 加熱碳酸氫鈉,證明它能分解釋放出二氧化碳氣體 |
| C |  | 實驗室制取氯氣 |
| D | 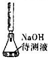 | 用中和滴定的方法測定某氫氧化鈉待測液的濃度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 已知 | 類推 | |
| A | 離子是帶電荷的粒子 | 帶電荷的粒子一定是離子 |
| B | 稀硫酸作電解質溶液時,氫氧燃料電池的負極反應為 2H2-4e-=4H+ | 氫氧化鉀溶液作電解質溶液時,氫氧燃料電池的負極反應為2H2-3e-+4OH-=4H2O |
| C | 將Fe加入到CuSO4溶液中 Fe+Cu2+=Cu+Fe2+ | 將Na加入到CuSO4溶液中 2Na+Cu2+=Cu+2Na+ |
| D | 原電池中通常是活潑金屬做負極,不活潑金屬做正極 | 銅和鋁與濃硝酸構成原電池時,銅是正極 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向Fe(NO3)2和KI混合溶液中加入少量稀鹽酸:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| B. | 向硝酸銀溶液中加入足量的氨水:Ag++2NH3•H2O═Ag(NH3)2++2H2O | |
| C. | 泡沫滅火器的滅火原理:2Al3++3CO32-+3H20═2Al(OH)3↓+3CO2↑ | |
| D. | 用足量的氨水處理硫酸工業的尾氣:SO2+NH3•H2O═NH4++HSO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al14有42個價電子,且與IIA族元素性質相似 | |
| B. | Al13有39個價電子,且與鹵素性質類似 | |
| C. | Al13在氣相中與HI反應可生成HAl13I,且化學方程式為 Al13+HI=HAl13I | |
| D. | Al13原子中A1原子間是通過離子鍵結合的 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 研究表明豐富的CO2完全可以作為新碳源,解決當前應用最廣泛的碳源(石油和天然氣)到本世紀中葉將枯竭的危機,同時又可緩解由CO2累積所產生的溫室效應,實現CO2的良性循環.
研究表明豐富的CO2完全可以作為新碳源,解決當前應用最廣泛的碳源(石油和天然氣)到本世紀中葉將枯竭的危機,同時又可緩解由CO2累積所產生的溫室效應,實現CO2的良性循環.| 實驗組[ | 溫度℃ | 起始量/mol | 平衡量/mol | 達到平衡所需 時間/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 下表列出了斷裂某些化學鍵所需的能量:
下表列出了斷裂某些化學鍵所需的能量:| 化學鍵 | H-H | Cl-Cl | I-I | O═O | C-Cl | C-H | O-H | H-Cl | H-I |
| 斷裂1mol化學鍵所吸收的能量(kJ) | 436 | 247 | 151 | x | 330 | 413 | 463 | 431 | 299 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com