
【題目】(1)0.1 mol/L醋酸溶液中,存在電離平衡CH3COOH![]() H++CH3COO-。經測定溶液中c(CH3COO―)為1.4×10-3 mol/L,此溫度下醋酸的電離平衡常數Ka=________。
H++CH3COO-。經測定溶液中c(CH3COO―)為1.4×10-3 mol/L,此溫度下醋酸的電離平衡常數Ka=________。
(2)已知飽和硫化氫的濃度為0.1 mol/L,硫化氫的電離常數為Ka1=1.0×10-7,Ka2=1.0×10-19,計算飽和硫化氫溶液中氫離子的濃度為__________mol/L。
 發散思維新課堂系列答案
發散思維新課堂系列答案科目:高中化學 來源: 題型:
【題目】某小組為探究K3[Fe(C2O4)3·3H2O(三草酸合鐵酸鉀晶體)的熱分解產物,按如圖所示裝置進行實驗。下列有關敘述錯誤的是( )
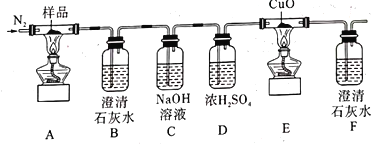
A.通入氮氣的目的有;隔絕空氣、使反應產生的氣體全部進人后續裝置
B.實驗中觀察到裝置F中澄清石灰水變渾濁,裝置E中固體變為紅色,由此可判斷熱分解產物中一定含有CO2和CO
C.為防止倒吸,停止實驗時應進行的操作是:先熄滅裝置A、E的酒精燈,冷卻后停止通人氮氣
D.樣品完全分解后,取少許裝置A中殘留物于試管中,加稀硫酸溶解,滴入1~2滴KSCN溶液,溶液變紅色,可證明殘留物中含有![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家研究出一種以天然氣為燃料的“燃燒前捕獲系統”,其簡單流程如圖所示(條件及物質未標出)。

(1)已知:CH4、CO、H2的燃燒熱分別為890.3 kJ·mol-1、283.0 kJ·mol-1、285.8 kJ·mol-1,則上述流程中第一步反應2CH4(g)+O2(g)===2CO(g)+4H2(g)的ΔH=______________。
(2)工業上可用H2和CO2制備甲醇,其反應方程式為CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),某溫度下,將1 mol CO2和3 mol H2充入體積不變的2 L密閉容器中,發生上述反應,測得不同時刻反應前后的壓強關系如下表:
CH3OH(g)+H2O(g),某溫度下,將1 mol CO2和3 mol H2充入體積不變的2 L密閉容器中,發生上述反應,測得不同時刻反應前后的壓強關系如下表:
時間/h | 1 | 2 | 3 | 4 | 5 | 6 |
| 0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
①用H2表示前2 h 的平均反應速率v(H2)=_________________________________;
②該溫度下,CO2的平衡轉化率為________。
(3)在300 ℃、8 MPa下,將CO2和H2按物質的量之比1∶3 通入一密閉容器中發生(2)中反應,達到平衡時,測得CO2的平衡轉化率為50%,則該反應條件下的平衡常數為Kp=________(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
(4)CO2經催化加氫可合成低碳烯烴:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH。在0.1 MPa時,按n(CO2)∶n(H2)=1∶3投料,如圖所示為不同溫度(T)下,平衡時四種氣態物質的物質的量(n)關系。
C2H4(g)+4H2O(g) ΔH。在0.1 MPa時,按n(CO2)∶n(H2)=1∶3投料,如圖所示為不同溫度(T)下,平衡時四種氣態物質的物質的量(n)關系。

①該反應的ΔH________0(填“>”或“<”)。
②曲線c表示的物質為_______。
③為提高H2的平衡轉化率,除改變溫度外,還可采取的措施______________。(答出一條即可)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CO、CO2是化石燃料燃燒后的主要產物。
(1)將體積比為2:1的CO2和CO混合氣體通入有足量Na2O2固體的密閉容器中,同時不斷地用電火花點燃。將殘留固體溶于水,所得溶液中2c(CO32-)+c(HCO3-)____________c(Na+)(填“>”“<”或“=”) 。
(2)已知:2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ/mol;鍵能E(o=o)=499.0 kJ/mol
①CO(g)+O2(g)![]() CO2(g)+O(g) 的△H=____________kJ/mol
CO2(g)+O(g) 的△H=____________kJ/mol
②已知2500K時,①中反應的平衡常數為0.40。某時刻該反應體系中各物質濃度滿足: c(CO)·c(O2)=c(CO2)·c(O),則此時反應____________(填向左”或“向右”)進行。
(3)已知:反應CO2(g)![]() CO(g)+O(g)在密閉容器中CO2分解實驗的結果如下圖1;反應2CO2(g)
CO(g)+O(g)在密閉容器中CO2分解實驗的結果如下圖1;反應2CO2(g)![]() 2CO(g)+O2(g)中1molCO2在不同溫度下的平衡分解量如下圖2,
2CO(g)+O2(g)中1molCO2在不同溫度下的平衡分解量如下圖2, 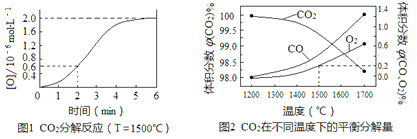
①分析圖1,求2min內v(CO2)=_______。
②分析圖2,1500℃時反應達平衡,此時容器體積為1 L,則反應的平衡常數K=______(計算結果保留1位小數)。
(4)為探究不同催化劑對CO和H2合成CH3OH的選擇性效果,某實驗室控制CO和H2的初始投料比為1:3進行實驗,得到如下數據:
選項 | T/K | 時間/min | 催化劑種類 | 甲醇的含量(%) |
A | 450 | 10 | CuO-ZnO | 78 |
B | 450 | 10 | CuO-ZnO-ZrO2 | 88 |
C | 450 | 10 | ZnO-ZrO2 | 46 |
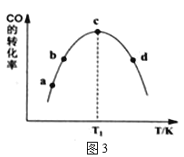
①由表1可知,該反應的最佳催化劑為____________(填編號);圖3中a、b、c、d四點是該溫度下CO的平衡轉化率的是____________。
②有利于提高CO轉化為CH3OH的平衡轉化率的措施有____________。
A. 使用催化劑CuO-ZnO-ZrO2 B. 適當降低反應溫度
C. 增大CO和H2的初始投料比 D. 恒容下,再充入a mol CO和3a mol H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從某廢催化劑(含ZnO、CuO、Fe2O3、石墨及MnO2等)中回收金屬并制取活性氧化鋅的工藝流程如下(已知:Zn及其氧化物、氫氧化物的性質與Al及其相應化合物性質類似):
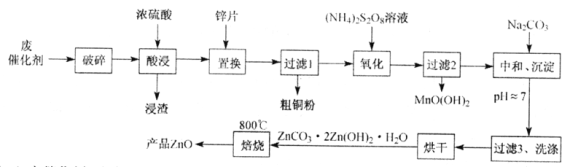
(1)廢催化劑“破碎”的目的是____________________________________________。
(2)“氧化”時Mn2+被氧化的離子方程式為_________________________________。
(3)“中和、沉淀”時,若pH過高,則堿式碳酸鋅的產率偏小。寫出其反應的離子方程式(任寫一個即可):____________________________________________。
(4)測得“粗銅粉”中銅的質量分數的實驗步驟如下:
I.準確稱取粗銅粉mg,加入足量鹽酸和H2O2溶液使其完全溶解。
Ⅱ.將溶液煮沸1~2min,除去過量的H2O2。
Ⅲ.滴入鐵掩蔽劑排除Fe3+的干擾。然后加入稍過量的KI溶液(反應:2Cu2++4I-=2CuI↓+I2),再加入幾滴淀粉溶液作指示劑,用 c mol ·L-1Na2S2O3標準溶液滴定至藍色消失(I2+2S2O32-=2I-+S4O62-)且半分鐘內不變色,共消耗Na2S2O3標準溶液VmL。
①銅的質量分數為______________________。
②缺少步驟Ⅱ噲會使測得的銅的質量分數___________(填“偏大”、“偏小”、或“不變”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)25°C時,若向a mol·L-1的HA溶液中,滴加等體積的b mol·L-1的NaOH溶液,使溶液呈中性,用含a的代數式表示HA的電離平衡常數Ka=____________。
(2)25°C時,將a mol·L-1的氨水與0.01 mol·L-1的鹽酸等體積混合,反應完后溶液中c(NH4+)=c(Cl-),則溶液顯_____性(填“酸”、“堿”或“中”),用含a的代數式表示NH3·H2O的電離平衡常數Kb=____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA表示阿伏加德羅常數,下列說法正確的是
A.含有25.2g HNO3的濃硝酸與足量的銅反應產生的NO2分子數目為0.1NA
B.1L0.6mol/L的Na2CO3溶液中含有的O原子數目為1.8NA
C.標準狀況下,22.4L的CH3COOH中含有的H原子個數為4NA
D.反應4NH3+6NO 5N2+6H2O中,當生成140g的N2時轉移12NA
5N2+6H2O中,當生成140g的N2時轉移12NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】高聚物H是一種有機高分子材料,其合成路線如圖所示:
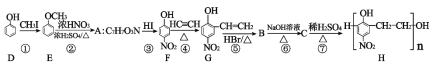
請回答下列問題:
(1)有機物D的名稱是__________________,A的結構簡式為_____________________;
(2)反應④的反應類型為________________;
(3)有機物F的核磁共振氫譜有____________組峰,峰面積之比為__________________;
(4)C到H的化學方程式為__________________________________________________;
(5)設計步驟①和步驟③的目的是_____________________________________________;
(6)滿足下列條件的比G多一個O原子的有機物的同分異構體,有_____________種。
①能夠發生銀鏡反應 ②含有硝基;
③能與FeCl3溶液發生顯色反應; ④苯環上有三個取代基;
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1 mol H—H鍵的鍵能是436kJ,1 mol I—I鍵的鍵能是151kJ,1 mol H—I鍵的鍵能是299kJ,則對反應H2(g)+I2(g)![]() 2HI(g)的說法,不正確的是 ( )
2HI(g)的說法,不正確的是 ( )
A.放熱反應B.吸熱反應C.化合反應D.可逆反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com