
(12分)
(1)鑒別KCl溶液和K2CO3的試劑是 ;離子方程式為
(2)除去混入FeCl3溶液中少量FeCl2雜質的試劑是 ,離子方程式為 .
(3)除去Na2CO3粉末中混入的NaHCO3雜質用 方法,化學方程式為 。
(4)除去混入MgO少量Al2O3雜質的試劑是————————,離子方程式為——————————。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
(12分)
(1)鑒別KCl溶液和K2CO3的試劑是 ;離子方程式為
(2)除去混入FeCl3溶液中少量FeCl2雜質的試劑是 ,離子方程式為 .
(3)除去Na2CO3粉末中混入的NaHCO3雜質用 方法,化學方程式為 。
(4)除去混入MgO少量Al2O3雜質的試劑是————————,離子方程式為——————————。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江蘇省蘇州五中高二第二學期期中考試化學試卷(帶解析) 題型:填空題
(12分)(1)化學平衡常數K表示可逆反應的進行程度,K值越大,表示 _________ ,K值大小與溫度的關系是:溫度升高,K值_____________ 。(填一定增大、一定減小、或可能增大也可能減小)。
(2) 一定條件下,在體積為3 L的密閉容器中,一氧化碳與氫氣反應生成甲醇(催化劑為Cu2O/ZnO):CO(g)+2H2(g) CH3OH(g)
CH3OH(g)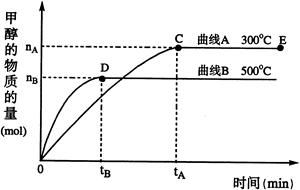
根據題意完成下列各題:
①反應達到平衡時,平衡常數表達式K= ,升高溫度,K值 (填“增大”、“減小”或“不變”)。
②在500 ℃,從反應開始到平衡,氫氣的平均反應速率v (H2)= 。
③據研究,反應過程中起催化作用的為Cu2O,反應體系中含少量CO2有利于維持催化劑Cu2O的量不變,原因是:_________________________(用化學方程式表示)。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年江西省南昌二中高一第二次月考化學試卷 題型:填空題
(12分)
(1)鑒別KCl溶液和K2CO3的試劑是 ;離子方程式為
(2)除去混入FeCl3溶液中少量FeCl2雜質的試劑是 ,離子方程式為 .
(3)除去Na2CO3粉末中混入的NaHCO3雜質用 方法,化學方程式為 。
(4)除去混入MgO少量Al2O3雜質的試劑是————————,離子方程式為——————————。
查看答案和解析>>
科目:高中化學 來源:2014屆陜西省高一下學期期末考試化學試卷(解析版) 題型:填空題
(12分)(1)氫能源是21世紀極具有發展前景的新能源之一,它既是綠色能源,又可循環使用。請在下圖的每個空格中填上循環過程中反應物和生成物的分子式,以完成理想的氫能源循環體系圖(循環中接受太陽能的物質在自然界中廣泛存在):
①_____,②_____。從能量轉換的角度看,過程Ⅱ應是____能轉化為_____能。

(2)圖中的燃料電池也可以用A和氧氣為原料。已知A分子是由碳和氫兩元素的原子構成,并且8.00 g A中含有3.01×1023個分子。實驗測得在298 K時,1 mol該氣體完全燃燒生成液態水和二氧化碳,放出890 kJ的熱量。
①寫出該氣體的化學式:______。
②寫出1 mol該氣體燃燒時的熱化學反應方程式:_____________。
③已知1 mol液態的水變成氣態水時需要吸收44 kJ的熱量,則1 mol該氣體完全燃燒生成氣態水和二氧化碳時放出的熱量為________kJ。
④若該燃料電池中的電解質溶液為氫氧化鉀溶液,則:電池正極反應為______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com