
下圖為制取乙酸乙酯的實驗裝置圖。回答下列問題:

(1)揭示實驗原理
①乙酸與乙醇在催化劑存在的條件下加熱可以發生反應生成乙酸乙酯。請用氧同位素示蹤法寫出乙酸與乙醇發生酯化反應的化學方程式______________________。
②能否用氫同位素示蹤法揭示酯化反應原理? _______(選填“能”或“不能”),原因是___________________。
(2)反應溫度確定:
合成乙酸乙酯的反應為放熱反應。實驗表明,反應溫度應控制在85℃左右為宜。回答:
實驗溫度不宜低于85℃左右的原因是__________________________________________;
實驗溫度不宜高于85℃左右的原因是__________________________________________;
(3)實驗裝置的比較:
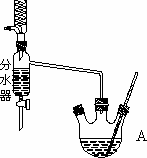
利用如圖裝置制備乙酸乙酯,這種裝置與教材裝置相比較突出的優點是__________________________。
(4)酯層厚度的標示:
為更好地測定酯層厚度,可預先向飽和Na2CO3溶液中滴加1滴____試液,現象是____________________________。
(1)① (2分)
(2分)
②否。醇和羧酸都失H,所以H換成D無法指示何種物質脫羥基。(各1分,共2分)
(2)反應速率低,達不到催化劑活性溫度;溫度過高利于平衡逆向移動,酯產率降低。(各2分,共4分)
(3)用分水器能夠在反應進行時很容易的把水分離出來,從而使平衡正向移動,提高乙酸乙酯的產率。(合理即給分 2分)
(4)酚酞。碳酸鈉層呈紅色,上層的酯層呈無色。(各1分,共2分)
【解析】
試題分析:
(1)酯化反應中羧酸提供羥基,醇應該氫原子,所以反應的機理可以表示為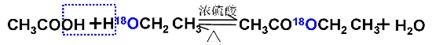 。
。
(2)由于醇和羧酸都失H,所以H換成D無法指示何種物質脫羥基,因此不能用氫同位素示蹤法揭示酯化反應原理。
溫度低,反應速率低,且達不到催化劑活性溫度,所以溫度不能低于85℃;正反應是放熱反應,溫度過高利于平衡逆向移動,酯產率降低,所以也不能高于85℃。
(3)根據裝置圖的結構特點可判斷,用分水器能夠在反應進行時很容易的把水分離出來,從而降低生成物濃度。使平衡正向移動,提高乙酸乙酯的產率。
(4)由于碳酸鈉溶液顯堿性,能使酚酞試液顯紅色,所以應該滴入酚酞試液,實驗現象是碳酸鈉層呈紅色,上層的酯層呈無色。
考點:考查酯化反應原理的探究、外界條件對反應速率和平衡對影響以及實驗評價


 輕巧奪冠周測月考直通中考系列答案
輕巧奪冠周測月考直通中考系列答案科目:高中化學 來源: 題型:
 “酒是陳的香”,這是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用下圖所示裝置制取乙酸乙酯.
“酒是陳的香”,這是因為酒在儲存過程中生成了有香味的乙酸乙酯,在實驗室我們也可以用下圖所示裝置制取乙酸乙酯.| 濃硫酸 |
| △ |
| 濃硫酸 |
| △ |
查看答案和解析>>
科目:高中化學 來源:上海市徐匯區2013年高考一模試卷化學試題 題型:043
下圖為制取乙酸乙酯的實驗裝置圖.回答下列問題:
1.揭示實驗原理
①乙酸與乙醇在催化劑存在的條件下加熱可以發生反應生成乙酸乙酯.請用氧同位素示蹤法寫出乙酸與乙醇發生酯化反應的化學方程式________.
②能否用氫同位素示蹤法揭示酯化反應原理?________(選填“能”或“不能”),原因是________.
2.反應溫度確定:
合成乙酸乙酯的反應為放熱反應.實驗表明,反應溫度應控制在85℃左右為宜.回答:
實驗溫度不宜低于85℃左右的原因是________;
實驗溫度不宜高于85℃左右的原因是________;
3.實驗裝置的比較:利用圖中裝置制備乙酸乙酯,這種裝置與教材裝置相比較突出的優點是________.
4.酯層厚度的標示:
為更好地測定酯層厚度,可預先向飽和Na2CO3溶液中滴加1滴________試液,現象是________.
查看答案和解析>>
科目:高中化學 來源:2011-2012年湖南鳳凰縣華鑫中學高一下學期第三次月考(文)化學卷(解析版) 題型:實驗題
(12分)下圖是實驗室制取乙酸乙酯的實驗裝置。請回答:

(1)在M試管中加碎瓷片的作用是 。
試管N中盛放的溶液是_________________ 。
該溶液的作用為中和乙酸,吸收揮發出的乙醇, ;
導管在其 液面上而不插入液面下的原因是 。
(2)在大試管中配制一定比例的乙醇、濃硫酸和乙酸
混合液時,加入試劑的順序是 。
(3)濃硫酸的作用是 。
(4)反應結束后,試管N內的液體分成兩層,反應生成的乙酸乙酯在 層(填寫“上”或“下”)。若分離N中的液體混合物需要用到的玻璃儀器是燒杯、 。
(5)M試管中發生反應的化學方程式 。
(6)生成乙酸乙酯的反應是可逆反應,反應物不能完全變成生成物,反應一段時間后,
就達到了該反應的限度,也即達到化學平衡狀態。下列描述能說明乙醇與乙酸的酯
化反應已達到化學平衡狀態的是 (填序號)。
①單位時間里,生成1mol乙酸乙酯,同時生成1mol水
②單位時間里,生成1mol乙酸乙酯,同時生成1mol乙酸
③單位時間里,消耗1mol乙醇,同時消耗1mol乙酸
查看答案和解析>>
科目:高中化學 來源:2013屆度北京五中高二第一學期期中考試化學(文)試卷 題型:填空題
(6分)某同學為制取乙酸乙酯,在試管A中加入3 mL 乙醇,然后邊振蕩試管邊慢慢加入2 mL 濃硫酸和2 mL 乙酸,按下圖所示連接好裝置進行實驗。請回答:

(1) 試管B中盛放的溶液是_________________。
(2) 實驗完成后,試管B的液面上有透明的不溶于水的油狀液體產生。 若分離該液體混合物需要用到的玻璃儀器是____________。
(3)乙醇與乙酸反應的化學方程式_____________________;實驗室中用30 g乙酸與46 g乙醇反應,如果實際產率是理論產率的60%,則可得到的有機產物的質量是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com