
【題目】在一定溫度下的定容密閉容器中,當下列物理量不再變化時,表明反應:A(s)+2B(g)![]() C(g)+D(g)已達平衡的是( )
C(g)+D(g)已達平衡的是( )
A. 混合氣體的壓強B. 混合氣體密度
C. A的物質的量濃度保持不變D. 氣體總物質的量保持不變
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】霧霾天氣對環境造成了嚴重影響,部分城市開展PM2.5和臭氧的監測。下列有關說法正確的是( )
A.臭氧的摩爾質量是48 g
B.同溫同壓條件下,等質量的氧氣和臭氧體積比為2∶3
C.16 g臭氧中含有6.02×1023個原子
D.1.00 mol臭氧中含有電子總數為18×6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 時,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示:下列描述正確的是
時,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示:下列描述正確的是

A.平衡時X、Y的轉化率相同
B.達到平衡后,將容器體積擴大為1L,平衡向正反應方向移動
C.![]() 時,該反應的化學方程式為:
時,該反應的化學方程式為:![]() ,平衡常數
,平衡常數![]()
D.![]() 時,若起始時X與Y均為
時,若起始時X與Y均為![]() ,則平衡時Y的轉化率小于
,則平衡時Y的轉化率小于![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鉍酸鈉(NaBiO3)是分析化學中的重要試劑,在水中緩慢分解,遇沸水或酸則迅速分解。某興趣小組設計實驗制取鉍酸鈉并探究其應用。回答下列問題:
Ⅰ.制取鉍酸鈉
制取裝置如圖(加熱和夾持儀器已略去),部分物質性質如下:
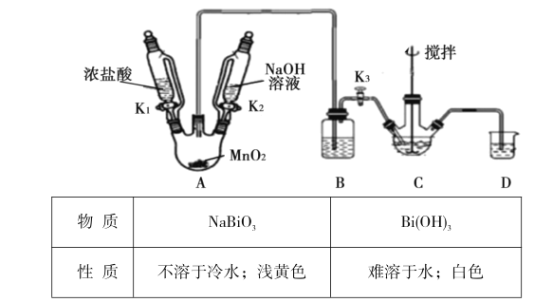
(1)C中盛放Bi(OH)3與NaOH的混合物,與Cl2反應生成NaBiO3,反應的化學方程式為__。B裝置的作用是__。
(2)當觀察到__(填現象)時,可以初步判斷C中反應已經完成。
(3)拆除裝置前必須先除去殘留的Cl2,以免污染空氣。除去燒瓶A中殘留Cl2的操作是:關閉__;打開__。
(4)反應結束后,為從裝置C中獲得盡可能多的產品,需要的操作有_。
Ⅱ.鉍酸鈉的應用——檢驗Mn2+
(5)往待檢液中加入鉍酸鈉晶體,加硫酸酸化,生成Bi3+,且溶液變為紫紅色,證明待檢液中存在Mn2+。產生紫紅色現象的離子方程式為__。
Ⅲ.產品純度的測定
(6)取上述NaBiO3產品ag,加入足量稀硫酸和MnSO4稀溶液使其完全反應,再用bmo1L-1的H2C2O4標準溶液滴定生成的MnO4-(已知:H2C2O4+MnO4-—CO2+Mn2++H2O,未配平),當溶液紫紅色恰好褪去時,消耗cmL標準溶液。該產品的純度為__(用含a、b、c的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在定溫定容的密閉容器中合成SO3 ,下列能說明反應 2SO2(g)+O2(g)![]() 2SO3(g)達到化 學平衡狀態的是
2SO3(g)達到化 學平衡狀態的是
A.cSO2 :cO2 :cSO3 =2:1:2B.容器內的密度不再改變
C.SO2 的轉化率不再改變D.SO3 的生成速率與 SO2 的消耗速率相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在![]() 時,將
時,將![]()
![]() 氣體充入2L密閉容器中,發生下列反應:
氣體充入2L密閉容器中,發生下列反應:![]() ,每隔一段時間對該容器的物質進行測量,得到的數據如表:下列說法中正確的是
,每隔一段時間對該容器的物質進行測量,得到的數據如表:下列說法中正確的是
時間 | 0 | 20 | 40 | 60 | 80 |
|
|
|
|
|
|
|
|
|
|
|
|
A.反應開始20s內![]() 的平均反應速率是
的平均反應速率是![]()
![]()
B.80s時混合氣體的顏色與60s時顏色相同,比40s時的顏色深
C.80s時向容器內加![]() molHe,容器體積保持不變,化學反應速率加快
molHe,容器體積保持不變,化學反應速率加快
D.80s時升高溫度,則正反應速率加快,逆反應速率也加快
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】處于平衡狀態的反應:2H2S(g)![]() 2H2(g)+S2(g) ΔH>0,不改變其他條件的情況下,下列敘述正確的是( )
2H2(g)+S2(g) ΔH>0,不改變其他條件的情況下,下列敘述正確的是( )
A.加入催化劑,反應途徑將發生改變,ΔH也將隨之改變
B.升高溫度,正、逆反應速率都增大,H2S分解率也增大
C.增大壓強,平衡向逆反應方向移動,將引起體系溫度降低
D.若體系恒容,注入一些H2后達新平衡,H2的濃度將減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NiSO4·6H2O是一種綠色易溶于水的晶體,廣泛用于化學鍍鎳、生產電池等。可由電鍍廢渣(除含鎳外,還含有Cu、Zn、Fe、Cr等雜質)為原料獲得。工藝流程如下圖:
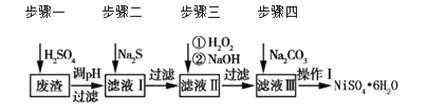
請回答下列問題:
(1)用稀硫酸溶解廢渣時,為了提高浸取率可采取的措施有_______(任寫一點)。
(2)向濾液中滴入適量的Na2S溶液,目的是除去Cu2+、Zn2+,寫出除去Cu2+的離子方程式________。
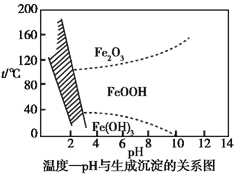
(3)在40 ℃左右,用6%的H2O2氧化Fe2+,再在95 ℃時加入NaOH調節pH,除去鐵和鉻。此外,還常用NaClO3作氧化劑,在較小的pH條件下水解,最終生成一種淺黃色的黃鐵礬鈉![]() (OH)12]沉淀除去。如圖是溫度—pH與生成的沉淀關系圖,圖中陰影部分是黃鐵礬穩定存在的區域[已知25 ℃時,Fe(OH)3的Ksp=2.64×10-39]。下列說法正確的是_______(選填序號)。
(OH)12]沉淀除去。如圖是溫度—pH與生成的沉淀關系圖,圖中陰影部分是黃鐵礬穩定存在的區域[已知25 ℃時,Fe(OH)3的Ksp=2.64×10-39]。下列說法正確的是_______(選填序號)。
a.FeOOH中鐵為+2價
b.若在25 ℃時,用H2O2氧化Fe2+,再在pH=4時除去鐵,此時溶液中c(Fe3+)=2.64×10-29
c.用氯酸鈉在酸性條件下氧化Fe2+的離子方程式為:6Fe2++Cl![]() +6H+
+6H+![]() 6Fe3++Cl-+3H2O
6Fe3++Cl-+3H2O
d.工業生產中常保持在85~95 ℃生成黃鐵礬鈉,此時水體的pH為1.2~1.8
(4)上述流程中濾液Ⅲ的主要成分是_______。
(5)確定步驟四中Na2CO3溶液足量,碳酸鎳已完全沉淀的簡單實驗方法是_______。
(6)操作Ⅰ的實驗步驟依次為(實驗中可選用的試劑:6 mol·L-1的H2SO4溶液、蒸餾水、pH試紙):
①___________;
②___________;
③蒸發濃縮、冷卻結晶,過濾得NiSO4·6H2O晶體;
④用少量乙醇洗滌NiSO4·6H2O晶體并晾干。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酰硫酸![]() 是染料、醫藥等工業的重要原料;溶于濃硫酸,可在濃硫酸存在時用
是染料、醫藥等工業的重要原料;溶于濃硫酸,可在濃硫酸存在時用![]() 和濃硝酸反應制得。實驗室用如圖裝置制備少量亞硝酰硫酸(夾持裝置略),并測定產品的純度。
和濃硝酸反應制得。實驗室用如圖裝置制備少量亞硝酰硫酸(夾持裝置略),并測定產品的純度。

(1)儀器B的名稱____________。
(2)B中產生SO2,其化學方程式為_______________________________________。
(3)三頸燒瓶C中濃硝酸與![]() 在濃硫酸作用下反應制得
在濃硫酸作用下反應制得![]()
①實驗前濃硝酸和濃硫酸混合的操作為______________________________________。
②C中反應溫度不能太高的原因為___________________________________。
③用冷水浴維持C溫度不變,開始反應較慢,待生成少量![]() 后,反應明顯加快,其原因可能是______________________。
后,反應明顯加快,其原因可能是______________________。
(4)測定產品的純度
準確稱取1.5g產品放入錐形瓶中,加入![]() 、100.00mL的
、100.00mL的![]() 溶液和足量稀硫酸,搖勻充分反應。然后用0.5000mol/L草酸鈉標準溶液滴定,消耗草酸鈉溶液的體積為30.00mL。
溶液和足量稀硫酸,搖勻充分反應。然后用0.5000mol/L草酸鈉標準溶液滴定,消耗草酸鈉溶液的體積為30.00mL。
已知:![]()
①草酸鈉與高錳酸鉀溶液反應的離子方程式為__________________________________。
②滴定終點的現象為______________________________________________。
③亞硝酰硫酸的純度![]() ________。[保留三位有效數字,M(NOSO4H)=127g/mol]
________。[保留三位有效數字,M(NOSO4H)=127g/mol]
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com