

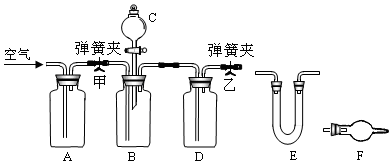
分析 根據實驗裝置圖可知,A、B是制備氯氣和二氧化氯的;C是用于吸收氯氣的;D是用于吸收二氧化氯的,E是用于重新釋放二氧化氯的,F是用于驗證二氧化氯的,F中的顏色不變,從而驗證C的作用是吸收氯氣,
(1)根據儀器特征,可知儀器D是錐形瓶;F裝置應是Cl2和KI反應,還需要連接尾氣處理裝置,所以應長管進氣,短管出氣;
(2)為使ClO2在D中被穩定劑充分吸收,產生ClO2的速率要慢;
(3)F裝置中發生Cl2+2KI=2KCl+I2時,碘遇淀粉變藍,而F中溶液的顏色不變,說明Cl2被吸收;
(4)在酸性條件下NaClO2可發生反應生成NaCl并釋放出ClO2,根據元素守恒可知應還有水生成,該反應的離子方程式為4H++5ClO2-=Cl-+4ClO2↑+2H2O; 在ClO2釋放實驗中,打開E的活塞,D中發生反應,則裝置F的作用是驗證是否有ClO2 生成;
(5)由圖可知,穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度.
解答 解:(1)根據儀器特征,可知儀器D是錐形瓶;F裝置應是Cl2和KI反應,還需要連接尾氣處理裝置,所以應長管進氣,短管出氣,故選b,
故答案為:錐形瓶;b;
(2)為使ClO2在D中被穩定劑充分吸收,產生ClO2的速率要慢,故滴加稀鹽酸的速度要慢,
故答案為:慢;
(3)F裝置中發生Cl2+2KI=2KCl+I2時,碘遇淀粉變藍,而F中溶液的顏色不變,則裝置C的作用是吸收Cl2,
故答案為:吸收Cl2;
(4)在酸性條件下NaClO2可發生反應生成NaCl并釋放出ClO2,根據元素守恒可知應還有水生成,該反應的離子方程式為:4H++5ClO2-=Cl-+4ClO2↑+2H2O; 在ClO2釋放實驗中,打開E的活塞,D中發生反應,則裝置F的作用是驗證是否有ClO2 生成,
故答案為:4H++5ClO2-=Cl-+4ClO2↑+2H2O;驗證是否有ClO2 生成;
(5)由圖可知,穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度,所以穩定劑Ⅱ好,
故答案為:穩定劑Ⅱ;穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度.
點評 本題以ClO2的制備、吸收、釋放為載體,考查實驗制備方案設計、基本操作、對裝置及操作的分析評價等,為高考常見題型,注意根據問題進行制備流程分析,難度中等.


 應用題天天練四川大學出版社系列答案
應用題天天練四川大學出版社系列答案科目:高中化學 來源: 題型:選擇題
 在一定溫度下,在體積為2L的恒容密閉容器中,某一反應中X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示,下列表述中正確的是( )
在一定溫度下,在體積為2L的恒容密閉容器中,某一反應中X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示,下列表述中正確的是( )| A. | 反應的化學方程式為2X=3Y+Z | |
| B. | t時,正、逆反應都不再繼續進行,反應達到化學平衡 | |
| C. | 若t=4,則0~t的X的化學反應速率為0.1 mol•L-1•min-1 | |
| D. | 溫度、體積不變,t時刻充入1 mol He使壓強增大,正、逆反應速率都增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯堿工業中電解飽和食鹽水:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| B. | 氯化鐵溶液腐蝕銅板:Fe3++Cu=Fe2++Cu2+ | |
| C. | 氫氧化鈉溶液吸收少量二氧化硫SO2+OH-=HSO3- | |
| D. | 稀硫酸中加氫氧化鋇溶液至中性:Ba2++H++OH-+SO42-=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na+、Mg2+、Cl-、I- | B. | Fe2+、Ba2+、S2-、Cl- | ||
| C. | Na+、Al3+、Cl-、HCO3- | D. | K+、Fe2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com