
0.5mol·L-1的一元酸A和未知濃度的一元強堿B以1∶2的體積比混合,所得溶液中[OH-]=0.1mol·L-1,用B中和20mL[H+]為0.01mol·L-1的一元弱酸C,當恰好完全反應時,用去5mL B溶液,求弱酸C的電離度.(電離度是指弱電解質達到電離平衡時,已電離的電解質分子數占原電解質分子數的百分數)
 名校名師培優作業本加核心試卷系列答案
名校名師培優作業本加核心試卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化學 來源: 題型:
《環境空氣質量標準》中,有害氣體的濃度常用標準狀況下,每立方米氣體中含有害氣體的毫克值(mg/m3)來表示,對CO的濃度限值規定為:
一、二級標準:4.00,三級標準:6.00 。一環保檢測中心對采集的0.02m3(標況)某區域空氣樣品中所含CO的濃度進行測定,其方法和實驗步驟如下:
① 首先將空氣樣品通過盛有I2O5固體的加熱管,反應生成CO2和I2(不考慮其他氣體的反應);
② 用30.0mL 5.00×10-5mol·L-1過量的硫代硫酸鈉溶液完全吸收反應所產生的碘,發生的反應為:I2+2S2O32-=2I-+S4O62-
③ 將②反應后溶液取出1/2,放入錐形瓶中,加入幾滴指示劑,用1.00×10-5mol·L-1的標準碘溶液進行滴定,滴定至終點,實驗記錄如下:

(1) 寫出中反應的化學方程式:
(2) 計算該空氣樣品中CO的濃度,并說明符合幾級標準。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年四川省雙流市外語學校高三9月月考化學試卷(解析版) 題型:選擇題
酸性高錳酸鉀溶液能將醇氧化成一系列產物,反應中KMnO4被還原為Mn2+。用0.5mol·L-1的酸性高錳酸鉀溶液滴定20.0mL0.25mol·L-1的乙二醇溶液,當用去20.0mL高錳酸鉀溶液時,再加一滴高錳酸鉀溶液恰好呈紫色,振蕩后不褪色。則乙二醇被氧化為
A.HOCH2-CHO B.OHC-CHO C.HOOC-CHO D.CO2
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
硫酸銅是一種應用極其廣泛的化工原料。銅不能與稀硫酸直接反應,本實驗中將適量濃硝酸分多次加入到銅粉與稀硫酸的混合物中,加熱使之反應完全,通過蒸發、結晶得到硫酸銅晶體(裝置如圖1、2所示)。
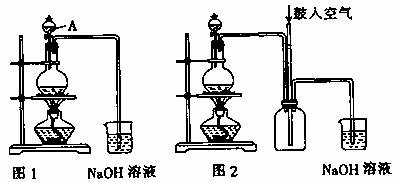
(1)圖1燒瓶中發生的反應的離子反應方程式為: 。
(2)圖2是圖1的改進裝置,其優點有:
① ;
② 。
(3)為符合綠色化學的要求,某研究性學習小組進行如下設計:
第一組:以空氣為氧化劑法
方案1:以空氣為氧化劑。將銅粉在儀器B中反復灼燒,使銅與空氣充分反應生成氧化銅,再將氧化銅與稀硫酸反應。
方案2:將空氣或氧氣直接通入到銅粉與稀硫酸的混合物中,發現在常溫下幾乎不反應。向反應液中加FeSO4或Fe2(SO4)3,即發生反應。反應完全后向其中加物質甲調節pH到3―4,產生Fe(OH)3沉淀,過濾、蒸發、結晶,濾渣作催化劑循環使用。(已知Fe(OH)3和Cu(OH)2完全沉淀時的pH分別為3.7、6.4。)
請回答下列問題:
①方案1中的B儀器名稱是 。
②方案2中甲物質是 (填字母序號)。
a、CaO b、CuCO3 c、CaCO3
第二組:過氧化氫為氧化劑法
將3.2g銅絲放到45 mL 1.5mol?L-1的稀硫酸中,控溫在50℃。加入18mL 10%的H2O2,反應0.5h后,升溫到60℃,持續反應1 h后,過濾、蒸發結晶、減壓抽濾等,用少量95%的酒精淋洗后晾干,得CuSO4?5H2O 10.6g。
請回答下列問題:
③加熱時溫度不宜過高的原因是 ,晶體采用酒精淋洗的優點是 。
④上述兩種氧化法中,更符合綠色化學理念的是 (填“第一組”或“第二組”),理由是 、
、 。
查看答案和解析>>
科目:高中化學 來源: 題型:
某同學為測定某燒堿樣品中含NaOH的純度(設樣品中雜質為NaCl),進行如下實驗:
(1)稱取樣品:調節托盤天平到零點后,在天平兩盤放質量大小相同紙片,使天平保持平衡,向左盤放一個5g砝碼,將游碼撥0.2g處;向右盤紙片上緩緩小心加燒堿顆粒到天平達平衡。該操作的錯誤之處有: 。按如上操作,該同學稱取燒堿樣品的實際量應是 。
(2)配制溶液:將紙片上的燒堿樣品小心移入100mL容量瓶中,加蒸餾水到刻度,蓋緊瓶塞,反復倒置搖勻,該操作的錯誤是 。按此方法所配制得的溶液濃度應 (從“偏高”或“偏低”等詞中選填)
(3)取液:將用蒸餾水洗凈的錐形瓶再用所配制堿液潤洗2~3次,再用蒸餾水洗凈的移液管取10mL所配堿液移入錐形瓶,再向瓶中加入約15mL蒸餾水將堿液稀釋。此操作中錯誤之處是 。
(4)滴定:向錐形瓶中加入約2mL酚酞溶液,用濃度為0.5mol?L-1的鹽酸標準液進行滴定,滴定時左手操作滴定管,右手猛力振蕩錐形瓶,當錐形瓶中溶液顏色剛變粉紅色時,停止滴定,記下耗酸體積數,此步操作中錯誤之處是 。
將(3)(4)操作重復一次
(5)計算:取兩次操作耗標準酸液體積平均值為20.00mL,依此數據計算出燒堿樣品中含NaOH的質量分數為 。
查看答案和解析>>
科目:高中化學 來源:2013屆四川省雙流市棠中外語學校高三9月月考化學試卷(帶解析) 題型:單選題
酸性高錳酸鉀溶液能將醇氧化成一系列產物,反應中KMnO4被還原為Mn2+。用0.5mol·L-1的酸性高錳酸鉀溶液滴定20.0mL0.25mol·L-1的乙二醇溶液,當用去20.0mL高錳酸鉀溶液時,再加一滴高錳酸鉀溶液恰好呈紫色,振蕩后不褪色。則乙二醇被氧化為
| A.HOCH2-CHO | B.OHC-CHO | C.HOOC-CHO | D.CO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com