
| A. | 蓋斯定律實質上是能量守恒定律的體現 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,含0.5mol H2SO4的濃硫酸與含1 mol NaOH的溶液混合,放出的熱量大于57.3 kJ | |
| C. | 由C(石墨)→C(金剛石)△H=+73 kJ/mol,可知石墨比金剛石穩定 | |
| D. | 在101 kPa時,2 g H2完全燃燒生成液態水,放出285.8 kJ熱量,氫氣燃燒的熱化學方程式表示為:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
分析 A.蓋斯定律是變化過程中能量變化和途徑無關,與反應物和生成物能量有關,是能量守恒的體現;
B.濃硫酸溶于水放熱;
C.能量越低越穩定;
D.2g氫氣為1mol,熱化學方程式中反應熱數據錯誤.
解答 解:A.蓋斯定律是變化過程中能量變化和途徑無關,與反應物和生成物能量有關,可以看作是能量守恒的體現,故A正確;
B.濃硫酸溶于水放熱,如稀溶液:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,則濃硫酸反應生成1mol水放出的熱量大于57.3kJ,故B正確;
C.由C(石墨)-→C(金剛石)△H=+73 kJ/mol,可知石墨比金剛石的能量低,能量越低越穩定,故C正確;
D.2g氫氣為1mol,熱化學方程式中反應熱數據錯誤,應為△H=-571.6 kJ/mol,故D錯誤.
故選D.
點評 本題考查化學反應與能量的變化,為高頻考點,側重于學生的分析能力和計算能力的考查,注意把握反應熱的計算、比較方法,難度不大.


 每課必練系列答案
每課必練系列答案科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:200 | B. | 200:1 | C. | 100:1 | D. | 1:100 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
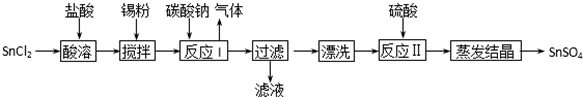
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 硫酸是工業生產中重要的產品之一,在很多領域都有重要用途.回答下列問題:
硫酸是工業生產中重要的產品之一,在很多領域都有重要用途.回答下列問題:| 壓強 SO2轉化率 溫度 | 1.0×105Pa | 5.0×105Pa | 1.0×106Pa | 1.5×106Pa |
| 400℃ | 0.9961 | 0.9972 | 0.9984 | 0.9989 |
| 500℃ | 0.9675 | 0.9767 | 0.9852 | 0.9894 |
| 600℃ | 0.8528 | 0.8897 | 0.9276 | 0.9468 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 燃燒熱是101kPa時,1mol純物質完全燃燒生成穩定的氧化物時所放出的熱量 | |
| B. | 工業上用點燃H2、Cl2混合氣體的方法生產鹽酸 | |
| C. | 金屬鈉著火時可用干燥的沙土來滅火 | |
| D. | 馳名世界的中國瓷器是硅酸鹽材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
| 實驗目的 | 實驗操作 | 現象 | 結論 |
| 自來水中離子檢驗 | 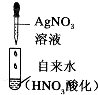 | 出現不溶于稀HNO3的沉淀 | 自來水中含氯離子 |
| 水的提純 | 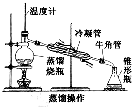 | 蒸餾燒瓶中水沸騰,冷凝管中有無色液體凝結,并通過冷凝管流入錐形瓶中 | 錐形瓶中收集到無色液體 |
| 蒸餾水中雜質離子的檢驗 | 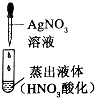 | 無明顯現象 | 蒸餾水中不含氯離子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑤ | B. | ②③④⑤ | C. | ①③⑤⑥ | D. | ①②③⑤ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com