
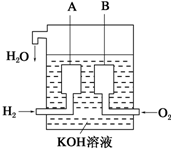
 (1)對于反應(yīng):K2Cr2O7+HCl→KCl+CrCl3+Cl2↑+H2O,回答下列問題:
(1)對于反應(yīng):K2Cr2O7+HCl→KCl+CrCl3+Cl2↑+H2O,回答下列問題:分析 (1)①該反應(yīng)中,Cr元素化合價由+6價變?yōu)?3價、Cl元素化合價由-1價變?yōu)?價;根據(jù)化合價升高值=化合價降低值=轉(zhuǎn)移電子數(shù)來回答;
②根據(jù)發(fā)生氧化反應(yīng)的HCl和K2Cr2O7的關(guān)系式計算;
(2)根據(jù)v=$\frac{△c}{△t}$來計算速率;不同物質(zhì)表示的速率之比等于系數(shù)之比,據(jù)此計算;
(3)在燃料電池中,通入正極的一極氧氣,通入負極的一極氧氣是燃料,負極的電極反應(yīng)=總反應(yīng)-正極的電極反應(yīng).
解答 解:(1)①反應(yīng)中所有Cr元素化合價降低了6價,被還原,K2Cr2O7具有氧化性,為氧化劑,部分Cl元素的化合價從-1升高到了0價,共升高了6價,根據(jù)電子守恒,所以重鉻酸鉀的系數(shù)是1,CrCl3的系數(shù)是2,氯氣的系數(shù)是3,根據(jù)K元素守恒,KCl的系數(shù)是2,根據(jù)Cl元素守恒,HCl的系數(shù)是14,根據(jù)H元素守恒,生成的水的系數(shù)是7,轉(zhuǎn)移電子數(shù)目為6,用單線橋法標出電子轉(zhuǎn)移的方向和數(shù)目可表示為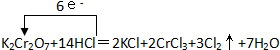 ,
,
故答案為:1;14;2;2;3;7;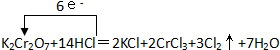 ;
;
②若反應(yīng)中,假設(shè)有14molHCl參加反應(yīng),有6molHCl被氧化,所以發(fā)生氧化反應(yīng)的HCl為1.2mol,則被還原的K2Cr2O7物質(zhì)的量=$\frac{1.2mol}{6}$=0.2mol,
故答案為:0.2;
(2)在容積為2L的密閉容器中進行,反應(yīng)經(jīng)過10min后,生成10mol NH3,則用NH3表示的化學反應(yīng)速率是$\frac{\frac{10mol}{2L}}{10min}$=0.5mol•(L•min)-1,用氮氣表示的速率是氨氣表示速率的一半,即用N2表示的化學反應(yīng)速率是0.25,mol•(L•min)-1,該反應(yīng)是可逆反應(yīng),1 mol N2和3 mol H2不能完全反應(yīng),因此放出的熱量總是小于92 kJ;
故答案為:0.25;該反應(yīng)是可逆反應(yīng),1 mol N2和3 mol H2不能完全反應(yīng),因此放出的熱量總是小于92 kJ;
(3)燃料電池的總反應(yīng)離子方程式為:CH4+2O2+2OH-=CO32-+3H2O,正極上通的是氧氣,電極反應(yīng):O2+2H2O+4e-═4OH-,負極一定是燃料失電子的過程,因正極和負極相加即為總反應(yīng),所以:CH4+8e-+10OH-=CO32-+7H2O,
故答案為:O2+2H2O+4e-═4OH-;CH4+8e-+10OH-=CO32-+7H2O.
點評 本題考查原電池工作原理、氧化還原反應(yīng)的計算、化學反應(yīng)速率的計算知識,可以根據(jù)所學知識進行回答,難度不大.需要注意的是電解質(zhì)溶液的酸堿性不同,電極反應(yīng)不同.


 小學教材全測系列答案
小學教材全測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 干冰、液態(tài)氯化氫都是電解質(zhì) | |
| B. | 根據(jù)是否具有丁達爾效應(yīng),將分散系分為溶液、濁液和膠體 | |
| C. | NaOH晶體中既含有離子鍵又含有共價鍵 | |
| D. | Na2O、Fe2O3、Al2O3既屬于堿性氧化物,又屬于離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
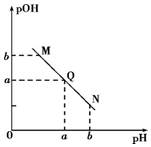
| A. | N點處pH>pOH,則N點處所示溶液呈酸性 | |
| B. | 該溫度下水的離子積Kw=1×10-2a | |
| C. | Q點所示溶液呈中性,則M、N、Q三點中只有Q點溶液中水的電離出的c(H+)與水的電離c(OH-)相等 | |
| D. | M點所示溶液的導電能力強于Q |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 水和四氯化碳可以用分液漏斗進行分離 | |
| B. | 提取溴水中的溴單質(zhì),可以用四氯化碳進行萃取 | |
| C. | 可以用高溫加熱的方法除去CaO中混有的CaCO3 | |
| D. | 可以用蒸發(fā)結(jié)晶的方法除去KNO3固體中混有的少量NaCl |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
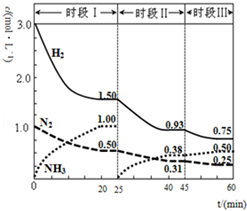 N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1.恒容時,體系中各物質(zhì)濃度隨時間變化的曲線如圖.
N2(g)+3H2(g)?2NH3(g);△H=-94.4kJ•mol-1.恒容時,體系中各物質(zhì)濃度隨時間變化的曲線如圖.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃度均為0.2 mol•L-1的AgNO3溶液和CH3COONa溶液等體積混合一定產(chǎn)生CH3COOAg沉淀 | |
| B. | 將0.001 mol•L-1的AgNO3溶液滴入0.001 mol•L-1的KCl和0.001 mol•L-1的K2CrO4的混合溶液中,先產(chǎn)生Ag2CrO4沉淀 | |
| C. | c(Mg2+)為0.11 mol•L-1的溶液中要產(chǎn)生Mg(OH)2沉淀,溶液的pH要控制在9以上 | |
| D. | 在其他條件不變的情況下,向飽和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na在空氣中燃燒,發(fā)出黃色火焰 | B. | Na在空氣中燃燒,產(chǎn)物是Na2O | ||
| C. | Na是銀白色金屬,硬度小,熔點低 | D. | Na、K合金可作原子反應(yīng)堆的導熱劑 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com