
 前四周期元素X、Y、Z、Q、R、W的原子序數依次增大.X基態原子的2p軌道為半充滿狀態;Y基態原子的L層有2個未成對電子;Z基態原子的最外層電子排布為3s23p2;Q、R、W都屬于金屬元素,Q、W基態原子核外均沒有未成對電子,R基態原子的d軌道上有3個空軌道.
前四周期元素X、Y、Z、Q、R、W的原子序數依次增大.X基態原子的2p軌道為半充滿狀態;Y基態原子的L層有2個未成對電子;Z基態原子的最外層電子排布為3s23p2;Q、R、W都屬于金屬元素,Q、W基態原子核外均沒有未成對電子,R基態原子的d軌道上有3個空軌道.分析 前四周期元素X、Y、Z、Q、R、W的原子序數依次增大.X基態原子的2p軌道為半充滿狀態,原子核外電子排布式為1s22s22p3,故X為N元素;Y基態原子的L層有2個未成對電子,原子序數大于N,則Y原子核外電子排布式為1s22s22p4,故Y為O元素;Z基態原子的最外層電子排布為3s23p2,則Z為Si;Q、R、W都屬于金屬元素,只能處于第四周期,其中R基態原子的d軌道上有3個空軌道,其原子外圍電子排布式為3d24s2,則R為Ti,Q、W基態原子核外均沒有未成對電子,Q原子序數小于Ti,則Q為Ca,W外圍電子排布式為3d104s2,則W為Zn,據此解答.
解答 解:前四周期元素X、Y、Z、Q、R、W的原子序數依次增大.X基態原子的2p軌道為半充滿狀態,原子核外電子排布式為1s22s22p3,故X為N元素;Y基態原子的L層有2個未成對電子,原子序數大于N,則Y原子核外電子排布式為1s22s22p4,故Y為O元素;Z基態原子的最外層電子排布為3s23p2,則Z為Si;Q、R、W都屬于金屬元素,只能處于第四周期,其中R基態原子的d軌道上有3個空軌道,其原子外圍電子排布式為3d24s2,則R為Ti,Q、W基態原子核外均沒有未成對電子,Q原子序數小于Ti,則Q為Ca,W外圍電子排布式為3d104s2,則W為Zn.
(1)R基態原子的d軌道上有3個空軌道,基態原子的電子排布式為1s22s22p63s23p63d24s,上述六種元素中,屬于ds區的元素符號是Zn,
故答案為:1s22s22p63s23p63d24s;Zn;
(2)含有16個中子的Si的核素符號為3014Si,同周期隨原子序數增大第一電離能呈增大趨勢,同主族自上而下第一電離能減小,氮元素原子2p能級為半滿穩定狀態,第一電離能高于氧元素的,故第一電離能:N>O>Si,
故答案為:3014Si;N>O>Si;
(3)NO3-中N原子孤電子對數=$\frac{5+1-2×3}{2}$=0、價層電子對數=3+0=3,故離子空間構型為平面三角形,與該離子互為等電子體的一種分子是SO3等,
故答案為:平面三角形;SO3等;
(4)X、Y分別與氫元素形成的最簡單氫化物分別為NH3、H2O,NH3、H2O的中心原子雜化方式相同,由于氨分子存在一對孤電子對,水分子存在兩對孤電子對,水分子中孤電子對對成鍵電子排斥力更強,所以水分子的鍵角比氨分子的鍵角小,
故答案為:NH3、H2O的中心原子雜化方式相同,由于氨分子存在一對孤電子對,水分子存在兩對孤電子對,水分子中孤電子對對成鍵電子排斥力更強,所以水分子的鍵角比氨分子的鍵角小;
(5)晶胞中Ti原子位于頂點,Ti數目為8×$\frac{1}{8}$=1,O原子為位于面心,O原子數目為6×$\frac{1}{2}$=3,Ca原子為體心,Ca數目為1,故該化合物的化學式為CaTiO3,晶胞質量為$\frac{136}{{N}_{A}}$g,Y與最近的R的距離為a cm,則晶胞邊長為2a cm×$\frac{\sqrt{2}}{2}$=$\sqrt{2}$a cm,晶體的密度為$\frac{136}{{N}_{A}}$g÷($\sqrt{2}$a cm)3=$\frac{136}{(\sqrt{2}a)^{3}×{N}_{A}}$g/cm3,
故答案為:CaTiO3;$\frac{136}{(\sqrt{2}a)^{3}×{N}_{A}}$.
點評 本題是對物質結構與性質的考查,涉及核外電子排布、元素周期表、電離能、空間構型、等電子體、價層電子對互斥理論、晶胞計算等,推斷元素是解題關鍵,注意利用均攤法進行晶胞有關計算,難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
| 50mL鹽酸 | 50mL鹽酸 | 50mL鹽酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| V(CO2)(標況) | 2.24L | 3.36L | 3.36L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 化學反應速率是化學反應進行快慢程度的物理量 | |
| B. | 化學反應速率通常用單位時間內生成或消耗某物質的質量的多少來表示 | |
| C. | 在同一個反應中,可以用反應物或生成物來表示反應速率 | |
| D. | 化學反應速率的常用單位有mol/(L•s)和mol/(L•min) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
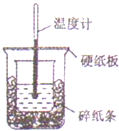 50ml0.5mol•L-1鹽酸與50ml•L-1NaOH溶液進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,下列說法正確的是( )
50ml0.5mol•L-1鹽酸與50ml•L-1NaOH溶液進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,下列說法正確的是( )| A. | 從實驗裝置上看,除了缺少環形玻璃攪拌棒外沒有其他問題 | |
| B. | 大燒杯上如不蓋硬紙板,測得的中和熱數值會偏大 | |
| C. | 用相同濃度和體積的氨水代替NaOH溶液進行上述實驗,測得中和熱的數值會偏大 | |
| D. | 實驗中改用60ml0.5mol•L-1鹽酸跟50ml0.55mol•L-1NaOH溶液進行反應,與上實驗相比,所放出的熱量不相等,但是所求中和熱相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵制品銹蝕時主要發生析氫腐蝕 | |
| B. | 施用適量石膏可以降低鹽堿地(含較多NaCl、Na2CO3)的堿性 | |
| C. | 電鍍廠未經處理的廢水可以直接用來灌溉農田 | |
| D. | 將水壩的鋼鐵閘門與直流電的正極相連可以防閘門腐蝕 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硫酸、純堿、氯化鈣 | B. | 鹽酸、燒堿、小蘇打 | ||
| C. | 碳酸、乙醇、醋酸鈉 | D. | 磷酸、熟石灰、過氧化鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 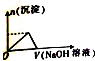 | B. | 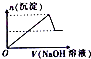 | C. | 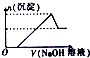 | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定有SO2、NH3和NO | B. | 一定有NO和HCl | ||
| C. | 可能有Cl2和O2 | D. | 一定沒有Cl2、NO2、NH3和O2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com