
近年來,為提高能源利用率,西方提出共生理念——為提高經濟效益,人類生產活動盡可能多功能化.共生工程將會大大促進化學工業的發展.
(1)由于共生工程的應用,利用發電廠產生的SO2制成自發電池,其電池反應方程式為:2SO2+O2+2H2O=2H2SO4,該電池電動勢為1.06V.實際過程中,將SO2通入電池的 極(填“正”或“負”),負極反應式為 .用這種方法處理SO2廢氣的優點是 .
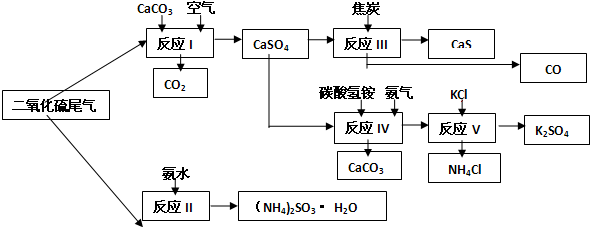
(2)以硫酸工業的SO2尾氣、氨水、石灰石、焦炭、碳酸氫銨和氯化鉀等為原料,可以合成有重要應用價值的硫化鈣、硫酸鉀、亞硫酸銨等物質.合成路線如下:
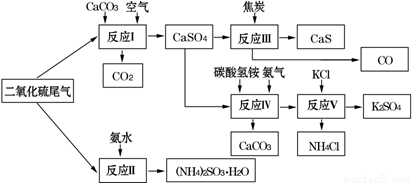
①生產中,向反應Ⅱ中的溶液中加入適量還原性很強的對苯二酚等物質,其目的是 .
②下列有關說法正確的是 .
A.反應Ⅰ中需鼓入足量空氣,以保證二氧化硫充分氧化生成硫酸鈣
B.反應Ⅲ中發生反應的化學方程式為CaSO4+4C  CaS+4CO↑
CaS+4CO↑
C.反應Ⅳ需控制在60~70℃,目的之一是減少碳酸氫銨的分解
D.反應Ⅴ中的副產物氯化銨可用作氮肥
③反應Ⅴ中選用了40%的乙二醇溶液做溶劑,溫度控制在25℃,此時硫酸鉀的產率超過90%,選用40%的乙二醇溶液做溶劑的原因是 .
④(NH4)2SO3可用于電廠等煙道氣中脫氮,將氮氧化物轉化為氮氣,同時生成一種氮肥,形成共生系統.寫出二氧化氮與亞硫酸銨反應的化學方程式 .
(共15分)
(1) 負(2分) SO2+2H2O-2e-=SO42-+4H+ (2分)
利用上述電池,可回收大量有效能,副產品為H2SO4,減少環境污染,實現(能質)共生。(2分)
(2)①防止亞硫酸銨被氧化(1分) ②ABCD(4分)
③K2SO4在有機溶劑乙二醇中溶解度小,能充分析出(2分)
④4(NH4)2SO3+2NO2=4(NH4)2SO4+N2(2分)
【解析】
試題分析:
(1)原電池負極發生氧化反應,正極發生還原反應,依據元素化合價變化可知,二氧化硫中硫元素化合價升高,失電子發生氧化反應。因此應將SO2通入電池的負極,電極反應為:SO2+2H2O-2e-=SO42-+4H+;此方法的優點是污染小,生成產物可以循環利用,可以回收有效能;
(2)①向反應II中的溶液中加入適量還原性很強的對苯二酚等物質,防止亞硫酸根被氧化,以更好的得到亞硫酸銨晶體;
②A、依據流程圖結合反應生成物分析,過量的空氣把亞硫酸鈣氧化為硫酸鈣,正確;
B、依據流程圖中的反應物和生成物,結合元素化合價變化分析,正確;
C、防止碳酸氫銨在溫度過高時分解得不到需要的目標產物,正確;
D、氯化銨是一種氮肥,正確;
③硫酸鉀在40%的乙二醇溶液中溶解度比在水中的小,有利于析出;
④二氧化氮具有強氧化性能氧化亞硫酸銨,生成硫酸銨,本身被還原為氮氣,原子守恒配平書寫出的化學方程式為:4(NH4)2SO3+2NO2=4(NH4)2SO4+N2;
考點:考查了二氧化硫的污染及治理,原電池和電解池的工作原理,物質的制備流程分析,反應產物判斷,反應條件的選擇和原因等相關知識,培養學生仔細審讀題意的能力。


科目:高中化學 來源: 題型:閱讀理解
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
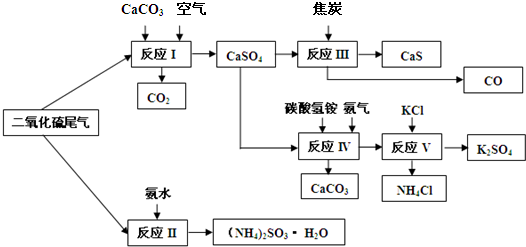
 CaS+4CO↑
CaS+4CO↑查看答案和解析>>
科目:高中化學 來源:豐臺區一模 題型:填空題
| ||
查看答案和解析>>
科目:高中化學 來源:北京模擬題 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com