
| A、25℃時,pH=12的1.0 L NaClO溶液中水電離出OH-的數目為0.01 NA |
| B、標準狀況下,22.4 L甲醇中含有的氧原子數為1.0 NA |
| C、0.1 mol乙醇中含有0.6 NA個C-H共價鍵 |
| D、常溫、常壓下,3.5 g 35Cl2所含中子數為0.1 NA |


 中考利劍中考試卷匯編系列答案
中考利劍中考試卷匯編系列答案 教育世家狀元卷系列答案
教育世家狀元卷系列答案 黃岡課堂作業本系列答案
黃岡課堂作業本系列答案 單元加期末復習先鋒大考卷系列答案
單元加期末復習先鋒大考卷系列答案科目:高中化學 來源: 題型:
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、17 g NH3中含有的質子數為1 mol |
| B、同溫同壓下CO與N2氣體密度相同 |
| C、20 g CuSO4?5H2O溶于80 g水所得溶液溶質質量分數為20% |
| D、16 g CH4在標準狀況下體積為 11.2 L |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、H2和T2 互為同素異形體 | ||||
B、
| ||||
| C、乙醇和二甲醚互為同分異構體 | ||||
| D、苯和甲苯互為同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:
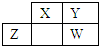 四種短周期元素X、Y、Z、W在元素周期表中的相對位置如表所示,Y、Z質子數之和為20,下列說法中不正確的是( )
四種短周期元素X、Y、Z、W在元素周期表中的相對位置如表所示,Y、Z質子數之和為20,下列說法中不正確的是( )| A、X、Y、Z、W均為非金屬元素 |
| B、X、Y、W的氫化物中,Y的氫化物沸點最高 |
| C、Z的陽離子與Y的陰離子電子層結構相同 |
| D、W元素的簡單離子半徑大于Z元素的簡單離子半徑 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、分散質微粒能透過半透膜 |
| B、是不穩定的分散系 |
| C、該膠體帶電,帶正電荷 |
| D、滴加入鹽酸至過量,先產生紅褐色沉淀,然后溶解 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、鋁表面易形成一層致密的氧化膜保護層,所以鋁要以廣泛用來制造炊具和包裝食品 |
| B、制備氫氧化鐵膠體是將FeCl3飽和溶液滴入沸水中并煮沸至紅褐色 |
| C、向試管中滴加液體時,膠頭滴管都不能伸入試管中 |
| D、金屬鈉﹑鎂等活潑金屬著火時,不能用直接用水滅火,而要用干粉滅火器滅火 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 時間/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
| A、當容器中氣體的密度不變時,說明該反應已達到平衡狀態 |
| B、用O2表示0~4 min內該反應的平均速率為0.005 mol/(L?min) |
| C、若升高溫度,則SO2的反應速率會變大,平衡常數K值會增大 |
| D、平衡時再通入18O2,平衡右移,再次平衡時各物質均含有18O,O2的轉化率減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com