
【題目】下列生產或實驗事實引出的結論不正確的是( )
選項 | 事實 | 結論 |
A | 其他條件相同, | 當其他條件不變時,升高反應溫度,化學反應速率加快 |
B | 工業制硫酸過程中,在 | 增大氣液接觸面積,使 |
C | 在2L密閉容器中發生反應:
| 反應速率減慢 |
D | A、B兩支試管中分別加入等體積5%的 | 當其他條件不變時,催化劑可以改變化學反應速率 |
A.AB.BC.CD.D
科目:高中化學 來源: 題型:
【題目】微生物燃料電池是指在微生物的作用下將化學能轉化為電能的裝置。某微生物燃料電池的工作原理如圖所示,下列說法正確的是(已知質子交換膜的作用是只允許H+通過)( )
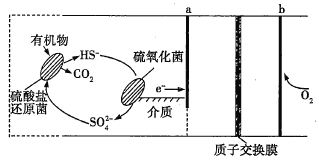
A.該電池在高溫下工作的速度更快
B.HS-在硫氧化菌作用下轉化為S的電極反應式為HS-+4H2O-8e-=SO42-+9H+
C.b電極是電池的負極
D.該電池工作時,H+向左通過質子交換膜
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲醇是一種重要的化工原料,又是一種可再生能源,具有開發和應用的廣闊前景。
(1)在一容積為2L的密閉容器內,充入0.2molCO與0.4molH2發生反應如下:CO(g)+2H2(g)CH3OH(g),CO的平衡轉化率與溫度,壓強的關系如圖所示。
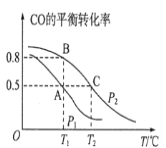
①A、B兩點對應的壓強大小關系是PA________PB(填“>、<、=”)。
②A、B、C三點的平衡常數KA,KB,KC的大小關系是______。
③下列敘述能說明上述反應能達到化學平衡狀態的是__(填代號)。
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的體積分數不再改變 c.混合氣體的密度不再改變 d.CO和CH3OH的物質的量之和保持不變
(2)在P1壓強、T1℃時,該反應的平衡常數K=___,再加入1.0molCO后重新到達平衡,則CO的轉化率__(填“增大,不變或減小”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質的轉化在指定條件下能實現的是
A.Cu ![]() Cu2(OH)2CO3
Cu2(OH)2CO3 ![]() Cu(OH)2
Cu(OH)2
B.MgO![]() MgCl2(aq)
MgCl2(aq) ![]() MgCl2(s)
MgCl2(s)
![]() C.CaCl2(aq)
C.CaCl2(aq) ![]() CaCO3
CaCO3 ![]() CaSiO3
CaSiO3
D.S![]() SO3
SO3 ![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學實驗設計和操作中必須十分重視安全問題和環境保護問題。下列實驗問題處理方法不正確的是( )
①配制稀硫酸時,可先在燒杯中加一定體積的水,再邊攪拌邊加入濃硫酸
②在氣體發生裝置上直接點燃一氧化碳氣體時,必須先檢驗一氧化碳氣體的純度。最簡單的方法是用排空氣的方法收集一試管氣體,點燃氣體,聽爆鳴聲
③實驗結束后將所有的廢液倒入下水道排出實驗室,以免污染實驗室
④給試管中的液體加熱時不時移動試管,以免暴沸傷人
⑤不慎將酸濺到眼中,應立即用水沖洗,邊洗邊眨眼睛
A.②③B.②⑤C.③④D.①③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】公元八世紀,Jabir ibn Hayyan在干餾硝石的過程中首次發現并制得硝酸(4KNO3![]() 2K2O+4NO↑+3O2↑),同時他也是硫酸和王水的發現者。下列說法正確的是
2K2O+4NO↑+3O2↑),同時他也是硫酸和王水的發現者。下列說法正確的是
A. 干餾產生的混合氣體理論上可被水完全吸收
B. 王水是由3體積濃硝酸與1體積濃鹽酸配制而成的
C. 王水溶解金時,其中的鹽酸作氧化劑(Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O)
D. 實驗室可用NaNO3與濃硫酸反應制備少量的HNO3,利用的是濃硫酸的氧化性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】灼熱的焦炭與水蒸氣反應所得產物為H2、CO和少量CO2,為了檢驗產物中的H2和CO(設氣體均被充分吸收),設計如下實驗裝置。下列有關說法錯誤的是
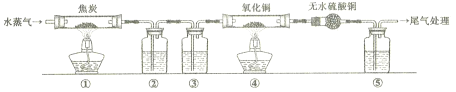
A. 為了實驗安全,應先點燃①處酒精燈,后點燃④處酒精燈
B. ②、③、⑤中依次盛裝氫氧化鈉溶液、濃硫酸和澄清石灰水
C. ④中黑色固體變紅色,即可證明產物中一定含有H2和CO中的一種或兩種
D. 若用堿石灰替換無水硫酸銅,也可以達到檢驗H2和CO目的
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下的定容容器中,反應:A(s)+2B(g)![]() C(g) +D(g)。下列不能表明反應
C(g) +D(g)。下列不能表明反應
達到平衡狀態的是( )。
A.氣體的壓強不變B.氣體平均相對分子質量不變
C.氣體的密度不變D.B物質的量濃度不變
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T時,向2 L的密閉容器中充入一定量的A和B,發生反應:A(g)+B(g)![]() C(g)+xD(g) ΔH>0,容器中A、B、D的物質的量隨時間的變化如圖所示。下列說法正確的是( )
C(g)+xD(g) ΔH>0,容器中A、B、D的物質的量隨時間的變化如圖所示。下列說法正確的是( )

A.反應前10 min內反應的平均速率為v(D)=0.3 mol·L-1·min-1
B.若平衡時保持溫度不變,壓縮容器體積,平衡逆向移動,平衡常數K值減小
C.反應至15 min時,其他條件不變,改變的條件可能是縮小容器體積
D.反應至15 min時,其他條件不變,改變的條件可能是降低反應體系溫度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com