
已知A、B、C、D、E、F都是周期表中前四周期的元素,它們的核電荷數A<B<C<D<E<F。其中A、B、C是同一周期的非金屬元素。化合物DC的晶體為離子晶體,D的二價陽離子與C的陰離子具有相同的電子層結構。AC2為非極性分子。B、C的氫化物的沸點比它們同族相鄰周期元素氫化物的沸點高。E元素是第四周期元素中未成對電子數最多的元素,ECl3能與B、C的氫化物形成六配位的配合物,且兩種配體的物質的量之比為2∶1,1mol配合物與足量的AgNO3溶液反應能立即生成3molAgCl。F原子的一種核素的質量數為65,中子數為 36。請根據以上情況,回答下列問題:(答題時要用元素符號表示)
(1)B氫化物與HCl反應生成的含有B元素粒子的空間構型是 .F元素原子的最外層電子數為 個。
(2)B3-離子分別與AC2、由B、C組成的氣態化合物互為等電子體,則B、C組成的化合物化學式為 ;B3-離子還可以和一價陰離子互為等電子體,這陰離子電子式為 ,這種陰離子常用于檢驗日常生活中的一種金屬陽離子,這金屬陽離子符號為
(3)A、B、C的第一電離能由小到大的順序為
(4)E3+的核外電子排布式是 ,ECl3形成的六配位的配合物化學式為 。
(5)B的最高價氧化物對應的水化物的稀溶液與D的單質反應時,B被還原到最低價,該反應的化學方程式是
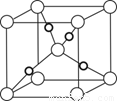
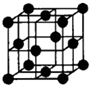
(6)在F的+1價氧化物的晶胞結構如圖,F為 球(“黑”“白”)
(15分)(1)正四面體型(1分) 1 (1分) (2)N2O(1分) 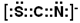 (1分) Fe3+ (1分)
(1分) Fe3+ (1分)
(3)C<O<N (2分) (4)1s22s22p63s23p63d3 (2分) [Cr(NH3)4(H2O)2]Cl3 (2分)
(5)4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O (2分) (6)黑 ( 2分)
【解析】
試題分析:A、B、C是同一周期的非金屬元素, AC2為非極性分子,因此A是碳元素,C是氧元素。B的原子序數介于A和C正價,所以B是氮元素。化合物DC的晶體為離子晶體,D的二價陽離子與C的陰離子具有相同的電子層結構,所以D是鎂元素。E元素是第四周期元素中未成對電子數最多的元素,則E是鉻元素。F原子的一種核素的質量數為65,中子數為 36,則F的原子序數是65-36=29,即F是銅元素。
(1)B氫化物是氨氣,與HCl反應生成的含有B元素粒子是NH4+,其空間構型是正四面體型;根據構造原理可知,銅原子的最外層電子是4s1,所以最外層電子數是1個。
(2)原子數和價電子數分別都相等的是等電子體,B3-離子含有3×5+1=16個價電子,所以B3-離子分別與AC2、由B、C組成的氣態化合物互為等電子體,則B、C組成的化合物化學式為N2O。B3-離子還可以和一價陰離子互為等電子體,這種陰離子應該是SCN-離子,其電子式為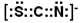 ,該陰離子常用于檢驗Fe3+。
,該陰離子常用于檢驗Fe3+。
(3)同周期第一電離能自左而右具有增大趨勢,所以第一電離能O>C。由于氮元素原子2p能級有3個電子,處于半滿穩定狀態,能量較低,第一電離能大于相鄰元素,所以A、B、C的第一電離能由小到大的順序為C<O<N。
(4)根據構造原理可知,E3+的核外電子排布式是1s22s22p63s23p63d3;ECl3能與B、C的氫化物形成六配位的配合物,且兩種配體的物質的量之比為2∶1,1mol配合物與足量的AgNO3溶液反應能立即生成3molAgCl,這說明氯離子不參與配位鍵的形成。由于Cr元素的化合價是+3價,所以所以該配位化合物中含有6個配體,其中氨氣是4個,水是2個,因此該配位化合物的化學式是[Cr(NH3)4(H2O)2]Cl3。
(5)B的最高價氧化物對應的水化物的稀溶液與D的單質反應時,B被還原到最低價,由于氮元素的最低價是-3價,這說明還原產物是硝酸銨,所以該反應的化學方程式是4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O。
(6)根據晶胞的結構并結合均攤法可知,白球個數=8×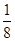 +1=2個,黑球個數是4個,即二者的個數之比是1:2。又因為F的+1價氧化物是Cu2O,所以F是黑球。
+1=2個,黑球個數是4個,即二者的個數之比是1:2。又因為F的+1價氧化物是Cu2O,所以F是黑球。
考點:考查元素周期表的結構和元素周期律、核外電子排布、第一電離能、等電子體、電子式、空間構型、晶體結構以及氧化還原反應方程式的書寫等


科目:高中化學 來源: 題型:


查看答案和解析>>
科目:高中化學 來源: 題型:
 已知A、B、C、D、E五種物質有如圖所示的轉化關系(部分反應物及反應條件未列出,若解題時需要,可作合理假設),且五種物質中均含有A元素.
已知A、B、C、D、E五種物質有如圖所示的轉化關系(部分反應物及反應條件未列出,若解題時需要,可作合理假設),且五種物質中均含有A元素.
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
 (Ⅰ)通常情況下,微粒A和B為分子,C和E為陽離子,D為陰離子,它們都含有10個電子;B溶于A后所得的物質可電離出C和D;A、B、E三種微粒反應后可得C和一種白色沉淀.請回答:
(Ⅰ)通常情況下,微粒A和B為分子,C和E為陽離子,D為陰離子,它們都含有10個電子;B溶于A后所得的物質可電離出C和D;A、B、E三種微粒反應后可得C和一種白色沉淀.請回答:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、Fe、Cu、Al、Ag | B、Al、Cu、Fe、Ag | C、Cu、Ag、Al、Fe | D、Ag、Al、Cu、Fe |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com