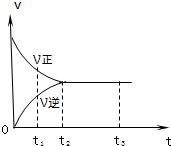
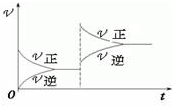
I、超音速飛機在平流層飛行時,尾氣中的NO會破壞臭氧層.科學家正在研究利用催化技術處理尾氣,化學方程式為2NO+2CO
2CO
2+N
2,為了測定在某種催化劑作用下的反應速率,在某溫度下用氣體傳感器測得不同時間的NO和CO濃度如下表:
| 時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol?L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol?L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
請回答(均不考慮溫度變化對催化效率的影響):
(1)若上述反應的平衡常數K,隨溫度增高而減小,則反應的△H______0(填“>”、“<”或“=”).
(2)前2s內的平均反應速度v(N
2)=______.
(3)該溫度下,反應的平衡常數K=______.
II、甲醇空氣燃料電池(酸性電解質溶液)的工作原理如圖一所示.
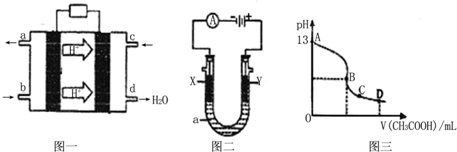
(1)該電池正極的電極反應式為______.
(2)以上述電池為電源,構成圖二電解池,其中X、Y為石墨,a為KCl溶液,寫出電解總反應的離子方程式______.
(3)常溫時,按“(2)”電解一段時間后,取25mL上述電解后的溶液,滴加0.2mol/L的醋酸溶液,滴加過程的pH變化如圖三所示,則C點對應溶液中各離子濃度的大小關系為(忽略電解后溶液中的其他成分,只考慮其中的堿與加入的酸)______.




 名校課堂系列答案
名校課堂系列答案