
| 40.32L |
| 22.4L/mol |
| 100g |
| 100g/mol |


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
| 放電 | 充電 |
查看答案和解析>>
科目:高中化學 來源:四川 題型:問答題
| 放電 |
| 充電 |
查看答案和解析>>
科目:高中化學 來源:2011普通高等學校招生全國統一考試化學卷(四川) 題型:填空題
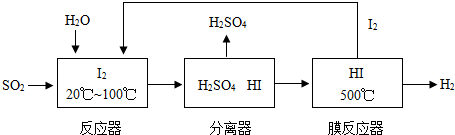
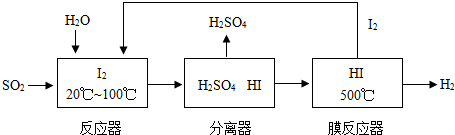
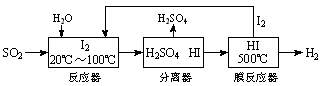
開發氫能是實現社會可持續發展的需要。硫鐵礦(FeS2)燃燒產生的SO2通過下列碘循環工藝過程既能制H2SO4,又能制H2。

請回答下列問題:
(1)已知1gFeS2完全燃燒放出7.1kJ熱量,FeS2燃燒反應的熱化學方程式為______________。
(2)該循環工藝過程的總反應方程式為_____________。
(3)用化學平衡移動的原理分析,在HI分解反應中使用膜反應器分離出H2的目的是____________。
(4)用吸收H2后的稀土儲氫合金作為電池負極材料(用MH)表示),NiO(OH)作為電池正極材料,KOH溶液作為電解質溶液,可制得高容量,長壽命的鎳氫電池。電池充放電時的總反應為:

①電池放電時,負極的電極反應式為____________。
②充電完成時,Ni(OH)2全部轉化為NiO(OH)。若繼續充電將在一個電極產生O2,O2擴散到另一個電極發生電極反應被消耗,從而避免產生的氣體引起電池爆炸,此時,陰極的電極反應式為______________
查看答案和解析>>
科目:高中化學 來源:四川省高考真題 題型:填空題
 Ni(OH)2+M
Ni(OH)2+M 查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com