
| ||
| 12g |
| 100g/mol |
| 0.1mol×106g/mol |
| 12.28g |


 全能練考卷系列答案
全能練考卷系列答案科目:高中化學 來源: 題型:閱讀理解

| 10-7b |
| a-b |
| 10-7b |
| a-b |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義。
![]() (1)硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:
(1)硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g) 2SO3(g),混合體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:

![]() ①2SO2(g)+O2(g) 2SO3(g)的△H 0(填“>”或“<”);若在恒溫、
①2SO2(g)+O2(g) 2SO3(g)的△H 0(填“>”或“<”);若在恒溫、
恒壓條件下向上述平衡體系中通入氦氣,平衡 移動(填“向左”、“向右”或
“不”);
②若溫度為T1、T2,反應的平衡常數分別為K1、K2,則K1 K2;若反應進行到狀
態D時,![]()
![]() (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
 (2)氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用。
(2)氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用。
①右圖是一定的溫度和壓強下是N2和H2反應生成1molNH3過程中能量變化示意圖,請寫出工業合成氨的熱化學反應方程式: 。(△H的數值用含字母a、b的代數式表示)②氨氣溶于水得到氨水。在25°C下,將a mol·L-1的氨水與b mol·L-1的鹽酸等體積混合,反應后溶液中顯中性,則c(NH+4) c(Cl-)(填“>”、“<”或“=”);用含a和b的代數式表示出氨水的電離平衡常數表達式 。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合態存在。在25°C下,向0.1mol·L-1的NaCl溶液中逐滴加入適量的0.1mol·L-1硝酸銀溶液,有白色沉淀生成。從沉淀溶解平衡的角度解釋產生沉淀的原因是 ,向反應后的濁液中,繼續加入0.1mol·L-1的NaI溶液,看到的現象是 ,產生該現象的原因是(用離子方程式表示) 。
(已知25°C時![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義。
(1)硫酸生產中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g),混合體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:
2SO3(g),混合體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:
①2SO2(g)+O2(g)![]() 2SO3(g)的△H 0(填“>”或“<”);若在恒溫、
2SO3(g)的△H 0(填“>”或“<”);若在恒溫、
恒壓條件下向上述平衡體系中通入氦氣,平衡 移動(填“向左”、“向右”或“不”);
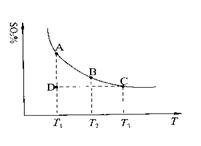
②若溫度為T1、T2,反應的平衡常數分別為K1、K2,則K1 K2;若反應進行到狀態D時,![]()
![]() (填“>”、“<”或“=”)(2)氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用。
(填“>”、“<”或“=”)(2)氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用。
①右圖是一定的溫度和壓強下是N2和H2反應生成1molNH3過程中能量變化示意圖,
請寫出工業合成氨的熱化學反應方程式: 。
(△H的數值用含字母a、b的代數式表示)
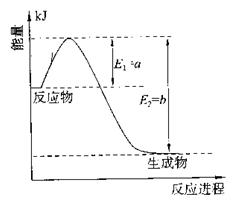
②氨氣溶于水得到氨水。在25°C下,將x mol·L-1的氨水與y mol·L-1的鹽酸等體積混合,反應后溶液中顯中性,則c(NH+4) c(Cl-)(填“>”、“<”或“=”);用含x和y的代數式表示出氨水的電離平衡常數 。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合態存在。在25°C下,向0.1mol·L-1的NaCl溶液中逐滴加入適量的0.1mol·L-1硝酸銀溶液,有白色沉淀生成,向反應后的濁液中,繼續加入0.1mol·L-1的NaI溶液,看到的現象是 ,產生該現象的原因是(用離子方程式表示) 。
(已知25°C時![]() )
)
查看答案和解析>>
科目:高中化學 來源:2011-2012學年山東省濟寧市高三上學期期末階段性教學質量檢測化學試卷 題型:填空
(13分)運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義。
(1)硫酸生產中,SO2催化氧化生成SO3:
 混合體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:
混合體系中SO3的百分含量和溫度的關系如下圖所示(曲線上任何一點都表示平衡狀態)。根據圖示回答下列問題:

① 的△H 0(填“>”
的△H 0(填“>”
或“<”);若在恒溫、恒壓條件下向上述平衡體系中通入氦氣,
平衡 移動(填“向左”、“向右”或“不”);
②若溫度為T1、T2,反應的平衡常數分別為K1、K2,
則K1 K2;反應進行到狀 態D時,V正 v逆(填“>”、“<”或“=)
(2)氮是地球上含量豐富的一種元素,氮及其化合物在工農業
生產、生活中有著重要作用。
① 圖是一定的溫度和壓強下是N2和H2反應生成1molNH3過
程中能量變化示意圖,請寫出工業合成氨的熱化學反應方程式:
。(△H的數值用含字母Q1、Q2的代數式表示)
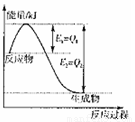
②氨氣溶于水得到氨水。在25°C下,將a mol·L-1的氨水與
b mol·L-1的鹽酸等體積混合,反應后溶液中顯中性,則
c(NH+4) c(Cl-)(填“>”、“<”或“=”);用含a和b的代數式表示該混合溶液中一水合出氨的電離平衡常數表達式 。
(3)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合態存在。已知:25℃時,KSP(AgCl)=1.6×10-10mol2·L-2、KSP(AgI)=1.5×10-16mol·L-2,在25℃下,向100mL 0.002mol·L-1的NaCl溶液中逐滴加入100mL 0.002mol·L-1硝酸銀溶液,有白色沉淀生成。從沉淀溶解平衡的角度解釋產生沉淀的原因是 ,向反應后的濁液中,繼續加入0.1mol·L-1的NaI溶液,看到的現象是 ,產生該現象的原因是(用離子方程式表示) 。
查看答案和解析>>
科目:高中化學 來源:2010年海南省高三五校聯考化學試題 題型:填空題
(9分)運用化學反應原理研究氮、硫、氯、碘等單質及其化合物的反應有重要意義。
(1)氮是地球上含量豐富的元素,氮及其化合物在工農業生產、生活中有著重要作用。
①下圖是一定的溫度和壓強下是N2和H2反應生成1molNH3過程中能量變化示意圖,請寫出工業合成氨的熱化學反應方程式: 。(△H的數值用含字母a、b的代數式表示)

②氨氣溶于水得到氨水。在25°C下,將m mol·L-1的氨水與n mol·L-1的鹽酸等體積混合,反應后的溶液呈中性,則c(NH+4) c(Cl-)(填“>”、“<”或“=”);用含m和n的代數式表示出混合液中氨水的電離平衡常數表達式 。
(2)海水中含有大量的元素,常量元素如氯、微量元素如碘在海水中均以化合態存在。
25°C下,向0.1mol·L-1的NaCl溶液中逐滴加入適量的0.1mol·L-1硝酸銀溶液,有白色沉淀生成。從沉淀溶解平衡的角度解釋產生沉淀的原因是 ,向反應后的濁液中,繼續加入適量0.1mol·L-1的NaI溶液,振蕩、靜置,看到的現象是 ,產生該現象的原因是(用離子方程式表示) 。
(已知25°C時 )
)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com