
【題目】在80℃時,將0.4mol的四氧化二氮氣體充入2L已抽空的固定容積的密閉容器中,隔一段時間對該容器內的物質進行分析,得到如下數據:反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺.
時間(s) c(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.20 | a | 0.10 | c | d | e |
c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)表中b_____c(填“<”、“=”、“>”).
(2)20s時,N2O4的濃度為_____mol/L,0~20s內N2O4的平均反應速率為_________.
(3)該反應在80℃時該反應的平衡常數K值為_______(保留2位小數).
【答案】 > 0.14 0.003mol/(Ls) 0.54
【解析】(1)將0.4mol的四氧化二氮氣體充入2L已抽空的固定容積的密閉容器中,反應的化學方程式為:N2O42NO2。反應進行至100s后將反應混合物的溫度降低,發現氣體的顏色變淺,說明反應逆向進行,逆反應是放熱反應,正反應是吸熱反應;進行到40s和進行到60s時;
N2O42NO2
起始量(mol) 0.4 0
變化量(mol) 0.2 0.4
40s末(mol) 0.2 0.4
得到b=0.2mol/L;進行到60s時;
N2O42NO2
起始量(mol) 0.4 0
變化量(mol) 0.22 0.44
60s末(mol) 0.18 0.44
c=0.18mol/L,因此b>c;故答案為:>;
(2)進行到20s;
N2O42NO2
起始量(mol) 0.4 0
變化量(mol) 0.12 0.24
20s末(mol) 0.28 0.24
20s時,N2O4的濃度=![]() =0.14mol/L;0~20s內N2O4的平均反應速率=
=0.14mol/L;0~20s內N2O4的平均反應速率=![]() =0.003 mol/(Ls);故答案為:0.14;0.003 mol/(Ls);
=0.003 mol/(Ls);故答案為:0.14;0.003 mol/(Ls);
(3)80°C時,60s是平衡狀態,平衡濃度c(NO2)=0.22mol/L,c(N2O4)=0.09mol/L,平衡常數K=![]() =
=![]() =0.54mol/L;故答案為:0.54。
=0.54mol/L;故答案為:0.54。


 ABC考王全優卷系列答案
ABC考王全優卷系列答案科目:高中化學 來源: 題型:
【題目】在FeCl3和CuCl2的混合液中逐漸加入鐵粉,溶液中Fe2+的物質的量濃度和加入鐵粉的物質的量之間關系如圖所示。則該溶液中FeCl3與CuCl2的物質的量濃度之比為

A. 3∶1 B. 1∶2 C. 2∶1 D. 1∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯氣是一種重要的化工原料,在生活和生產中的應用十分廣泛。請回答:
(1)在工業上,“氯堿工業”是生產氯氣的主要方法。請寫出工業制備氯氣的離子方程式____。
(2)實驗室常用MnO2與濃鹽酸反應制備Cl2,裝置如圖所示:
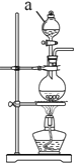
儀器a的名稱為____。制備實驗開始時,先檢査裝置氣密性,接下來的操作依次是____(填序號)。
①往燒瓶中加入MnO2粉末 ②加熱 ③往燒瓶中加入濃鹽酸
(3)為證明Cl2與H2O反應為可逆反應,將生成的氣體通入圖所示裝置:
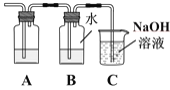
①裝置A中應加入的試劑是____。
②證明可逆反應,需驗證在B中反應物和生成物同時存在,證明氯水中有Cl2存在的現象是____,僅使用一種試劑證明氯水中HCl和HClO均存在,合適的試劑是____。
A.AgNO3溶液 B.石蕊試液 C.NaOH溶液 D.品紅溶液
③裝置C中NaOH溶液的作用是____。
(4)制備反應會因鹽酸濃度下降而停止,為測定反應殘余液中鹽酸的濃度(殘余液體積已知)。甲同學提出下列具體方案。請你從下列實驗方案中選擇合理的實驗方法____。
A.在殘余液中加入足量AgNO3溶液,過濾,洗滌,干燥,稱量沉淀的質量
B.在殘余液中加入足量NaHCO3固體,將反應后的氣體直接用堿石灰吸收,測定生成的氣體的質量
C.在殘余液中加入足量鋅片,測量生成氣體的體積,折算成標準狀況下的體積
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海藻中含有豐富的、以離子形式存在的碘元素。下圖是實驗室從海藻里提取碘的流程中的一部分。
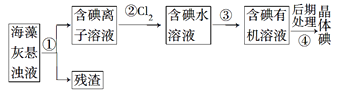
下列判斷正確的是
A. 步驟①③的操作分別是過濾、萃取
B. 可用淀粉溶液檢驗步驟②的反應是否進行完全
C. 步驟③中加入的有機溶劑是裂化汽油或乙醇
D. 步驟④的操作是過濾
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是以鉛蓄電池為電源,模擬氯堿工業電解飽和食鹽水的裝置圖(C、D均為石墨電極)。
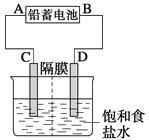
已知:鉛蓄電池在放電時發生下列電極反應:
負極Pb+SO![]() -2e-===PbSO4
-2e-===PbSO4
正極PbO2+4H++SO![]() +2e-===PbSO4+2H2O
+2e-===PbSO4+2H2O
(1)請寫出電解飽和食鹽水的化學方程式_______________________________________。
(2)若在電解池中C極一側滴酚酞試液,電解一段時間后未呈紅色,說明鉛蓄電池的A極為________極。
(3)用鉛蓄電池電解1 L飽和食鹽水(食鹽水足量)時,
①若收集到11.2 L(標準狀況下)氯氣,溶液pH=_________________。
②若鉛蓄電池消耗H2SO4 2 mol,則可收集到H2的體積(標準狀況下)為___________L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】世界環保聯盟建議全面禁止使用氯氣用于飲用水的消毒,而建議采用高效“綠色”消毒劑二氧化氯。二氧化氯是一種極易爆炸的強氧化性氣體,易溶于水、不穩定、呈黃綠色,在生產和使用時必須盡量用稀有氣體進行稀釋,同時需要避免光照、震動或加熱。實驗室以電解法制備ClO2的流程如下:

(1) ClO2中所有原子_____________(填“是”或“不是”)都滿足8電子結構。上圖所示電解法制得的產物中雜質氣體B能使石蕊試液顯藍色,除去雜質氣體可選用_________
A.飽和食鹽水 B.堿石灰 C.濃硫酸 D.蒸餾水
(2) 穩定性二氧化氯是為推廣二氧化氯而開發的新型產品,下列說法正確的是_________
A.二氧化氯可廣泛用于工業和飲用水處理
B.穩定性二氧化氯的出現大大增加了二氧化氯的使用范圍
C.在工作區和成品儲藏室內,要有通風裝置和監測及警報裝置
(3) 歐洲國家主要采用氯酸鈉氧化濃鹽酸制備。化學反應方程式為______________________。
(4) 我國廣泛采用經干燥空氣稀釋的氯氣與固體亞氯酸鈉(NaClO2)反應制備,化學方程式是 __________________,此法相比歐洲方法的優點是______________________。
(5) 科學家又研究出了一種新的制備方法,利用硫酸酸化的草酸(H2C2O4)溶液還原氯酸鈉,化學反應方程式為_____________________________。此法提高了生產及儲存、運輸的安全性,原因是 _________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式正確的是( )
A. 0.01mol/L NH4Al(SO4)2溶液與0.02mol/L Ba(OH)2溶液等體積混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3·H2O
B. FeCl2酸性溶液放在空氣中變質:2Fe2++4H++O2=2Fe3++2H2O
C. 用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑
D. 電解MgCl2水溶液的離子方程式:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】認真觀察下列裝置,回答下列問題:

(1)裝置B中PbO2上發生的電極反應方程式為__________________。
(2)裝置A中總反應的離子方程式為____________________________。
(3)裝置D中總反應的離子方程式為_____________________________。
(4)若裝置E的目的是在Cu材料上鍍銀,則X為________,極板N的材料為__________。
(5)當裝置A中Cu電極質量改變6.4 g時,裝置D中產生的氣體體積為____L(標準狀況下)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用如圖所示各裝置設計一個實驗,驗證濃硫酸與木炭粉在加熱條件下反應產生的各種產物。

(1)如按氣流由左向右流向,連接上述裝置的正確順序是(填各接口字母):
A接G,H接C,D接_______,_______接C,D接B ;
(2)儀器乙、丙應有怎樣的實驗現象才表明已檢驗出CO2?乙中_____________________________,丙中_____________________________;
(3)丁中酸性KMnO4溶液的作用是___________________________________________;
(4)寫出甲中反應的化學方程式_________________________________________ 。
(5)硫酸有很多的性質,將下列性質對應的字母填入各小題后面對應的括號中:
A.脫水性 B.酸性 C.強氧化性 D.吸水性
Ⅰ.在化學實驗中,濃硫酸可做SO2、CO2等氣體的干燥劑。 (_______)
Ⅱ.Na2CO3與H2SO4反應,可生成Na2SO4和CO2。 (_______)
Ⅲ.向濾紙上滴加濃H2SO4 ,濾紙變黑。 (_______)
Ⅳ.在冷濃H2SO4中放入鐵片沒明顯現象 (_______)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com