
【題目】鍺(Ge)是典型的半導體元素,在電子、材料等領域應用廣泛。回答下列問題:
(1)基態Ge原子的核外電子排布式為[Ar]________,有________個未成對電子。
(2)Ge與C是同族元素,C原子之間可以形成雙鍵、叁鍵,但Ge原子之間難以形成雙鍵或叁鍵。從原子結構角度分析,原因是_______________________________。
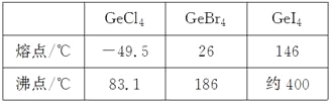
(3)比較下列鍺鹵化物的熔點和沸點,分析其變化規律及原因_____________________。
(4)光催化還原CO2制備CH4反應中,帶狀納米Zn2GeO4是該反應的良好催化劑。Zn、Ge、O電負性由大至小的順序是________________。
(5)Ge單晶具有金剛石型結構,其中Ge原子的雜化方式為____________,微粒之間存在的作用力是________________。
(6)晶胞有兩個基本要素:
①原子坐標參數,表示晶胞內部各原子的相對位置,下圖為Ge單晶的晶胞,其中原子坐標參數A為(0,0,0);B為(1/2,0,1/2);C為(1/2,1/2,0)。則D原子的坐標參數為________。

②晶胞參數,描述晶胞的大小和形狀,已知Ge單晶的晶胞參數a=565.76 pm,其密度為________g·cm-3(列出計算式即可)。
【答案】3d104s24p2 2 Ge原子半徑大,原子間形成的σ單鍵較長,pp軌道肩并肩重疊程度很小或幾乎不能重疊,難以形成π鍵 GeCl4、GeBr4、GeI4的熔、沸點依次增高。原因是分子結構相似,相對分子質量依次增大,分子間相互作用力逐漸增強 O>Ge>Zn sp3 共價鍵 (![]() ,
,![]() ,
,![]() )
) ![]()
【解析】
(1)Ge是32號元素,位于第四周期第IVA族,基態Ge原子核外電子排布式為[Ar]3d104s24p2;
(2)Ge原子半徑大,難以通過“肩并肩”方式形成π鍵;
(3)鍺的鹵化物都是分子晶體,相對分子質量越大,分子間作用力越強,熔沸點越高;
(4)元素的非金屬性越強,吸引電子的能力越強,元素的電負性越大;
(5)①Ge單晶具有金剛石型結構,Ge原子與周圍4個Ge原子形成正四面體結構,向空間延伸的立體網狀結構,屬于原子晶體;②Ge單晶具有金剛石型結構,則晶胞中Ge原子數目為8,結合阿伏伽德羅常數表示出晶胞的質量,再根據ρ=m/V計算晶胞密度。
(1)鍺為32號元素,根據原子核外電子的排布規律,可寫出其電子排布式為1s22s22p63s23p63d104s24p2,其核外電子排布簡式為[Ar]3d104s24p2,其中4p能級有2個未成對電子,故答案為:3d104s24p2;2;
(2) 雖然Ge與C是同族元素,C原子之間可以形成雙鍵、叁鍵,但考慮Ge的原子半徑大,難以通過“肩并肩”方式形成π鍵,所以Ge原子之間難以形成雙鍵或叁鍵,
故答案為:Ge原子半徑大,原子間形成的σ單鍵較長,pp軌道肩并肩重疊程度很小或幾乎不能重疊,難以形成π鍵;
(3)由表中數據可知,鍺的鹵化物都是分子晶體,分子間通過分子間作用力結合,對于組成與結構相似的分子晶體,相對分子質量越大,分子間作用力越強,熔沸點越高,由于相對分子質量:GeCl4<GeBr4<GeI4,故沸點:GeCl4<GeBr4<GeI4,故答案為:GeCl4、GeBr4、GeI4的熔、沸點依次增高。原因是分子結構相似,分子量依次增大,分子間相互作用力逐漸增強;
(4)Zn、Ge、O三種元素中,Zn和Ge是金屬元素,O是非金屬元素。O的電負性比Zn和Ge的大,又根據同周期元素的電負性從左到右逐漸增大的規律,可知電負性:O>Ge>Zn,故答案為O>Ge>Zn;
(5)由于鍺單晶具有金剛石型的結構,故每個鍺原子與相鄰的四個鍺原子形成四個共價鍵,其原子軌道雜化類型為sp3雜化,故答案為: sp3 ;共價鍵;
(6)①由Ge單晶晶胞結構示意圖,可知D原子與A原子及位于3個相鄰面面心的3個原子構成了正四面體結構,D原子位于正四面體的中心,再根據A、B、C三個原子的坐標參數可知D原子的坐標參數為(![]() ,
,![]() ,
,![]() ),故答案為:(
),故答案為:(![]() ,
,![]() ,
,![]() );②由鍺單晶的晶胞結構示意圖,可知該晶胞中位于頂點的有8個原子,位于面心的有6個原子,位于內部的有4個原子,則一個晶胞中所含有的鍺原子個數為8×
);②由鍺單晶的晶胞結構示意圖,可知該晶胞中位于頂點的有8個原子,位于面心的有6個原子,位于內部的有4個原子,則一個晶胞中所含有的鍺原子個數為8×![]() +6×
+6×![]() +4=8,再由晶胞參數可知該晶胞的邊長為565.76 pm的正方體,則其密度為:
+4=8,再由晶胞參數可知該晶胞的邊長為565.76 pm的正方體,則其密度為:![]() ,故答案為:
,故答案為:![]() 。
。


科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 按系統命名法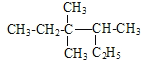 的名稱為3,3-二甲基-2-乙基戊烷
的名稱為3,3-二甲基-2-乙基戊烷
B. 分子式為C5H12O的醇共有8 種,其中能催化氧化成醛的同分異構體有3 種
C. 在一定條件下,乙酸、氨基乙酸、蛋白質均能與NaOH發生反應
D. 乙烯和苯均能使溴水因發生化學反應褪色
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按下列要求填寫以下空格:
(1)-COOH的名稱是 ________________,
(2)-CHO的名稱是___________________
(3)寫出羥基的化學式_______________________
(4)苯的結構簡式是_______________
(5)寫出乙酸與碳酸鈉反應的化學方程式______________________________________________ ,
該反應說明,乙酸的酸性____(填強或弱)于碳酸 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定條件下存在反應:2SO2(g)+ O2 (g)![]() 2SO3(g),其正反應放熱。現有三個體積相同的密閉容器
2SO3(g),其正反應放熱。現有三個體積相同的密閉容器
I、II、III,按如下圖所示投料,并在400℃條件下開始反應。達到平衡時,下列說法正確的是

A. 容器I、III中平衡常數相同
B. 容器II、III中正反應速率相同
C. 容器II、III中的反應達平衡時, SO3的體積分數:II > III
D. 容器I中SO2的轉化率與容器II中SO3的轉化率之和小于1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酰氯(SO2C12)常用于制造醫藥品、染料等。通常情況下其熔點為-54.1℃,沸點69.2℃,遇水發生劇烈反應生成氯化氫氣體。某實驗小組擬用干燥的氯氣和二氧化硫在活性炭催化下制取硫酰氯,其實驗裝置如下:

(1)有關冷凝管的使用原理,下列說法正確的是(填字母)______________。
a.蒸氣冷凝在內管的外壁上
b.當蒸餾液體的沸點超過140℃,水冷易炸裂儀器,此時多采用空氣冷凝管
c.蛇形冷凝管多用于有機制備的回流,適用于沸點較低的液體
d.內外管所圍出的空間為行水區,有吸收蒸氣熱量并將熱量移走的功用
(2)B中的試劑為___________,作用為______________________________。
(3)在不改變裝置的前提下,丁中的KClO3可用_____________代替(填化學式)。
(4)該小組向Cu(NO3)2·3H2O晶體中滴加SO2C12制備少量無水Cu(NO3)2。
①請寫出SO2C12與水反應的化學方程式__________________________________。
②滴加SO2C12的作用除了吸水之外,還有_____________________________。
(5)測定無水Cu(NO3)2的純度,可用分光光度法。現測得[Cu(NH3)4]2+的吸光度A與Cu2+標準濃度關系如圖所示(已知4NH3·H2O+Cu2+==[Cu(NH3)4]2++4H2O)。
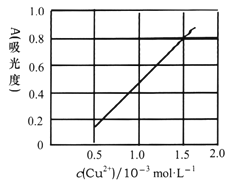
稱取0.3150g制得的無水Cu(NO3)2樣品,用蒸餾水溶解并配制成100mL溶液,用__________(填儀器名稱)準確量取10.00mL,加過量氨水,再用蒸餾水稀釋至100mL,測得其吸光度A=0.8。則此無水Cu(NO3)2樣品的純度是___________(保留三位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關第114號和第116號兩種元素的說法錯誤的是( )
A. 兩種元素位于同一周期 B. 116號元素位于ⅥA族
C. 兩種元素都是活潑的非金屬元素 D. 114號元素與Si元素在同一主族
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CuSO4溶液是中學化學及農業生產中常見的一種試劑。
(1)某同學配制CuSO4溶液時,需加入一定量的硫酸溶液,用離子方程式說明其原因是___________。
(2)該同學利用制得的CuSO4溶液,進行以下實驗探究。
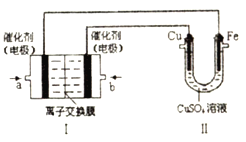
如圖,Ⅰ是甲烷燃料電池(電解質溶液為KOH溶液)的結構示意圖,該同學想在Ⅱ中實現鐵上鍍銅,則a處電極上發生的電極反應式是___________。若只把Ⅱ中電極均換為惰性電極,電解時的化學反應方程式為___________。若把Ⅱ中電極均換為惰性電極,電解液換為含有0.04mol CuSO4和0.04mol NaCl的混合溶液400mL,當陽極產生的氣體為672mL(標準狀況下)時,溶液的pH=___________(假設電解后溶液體積不變)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. 含有金屬元素的離子—定是陽離子
B. 含有離子鍵和共價鍵的化合物一定是離子化合物
C. 目前使用的元素周期表中,最長的周期含有36種元素
D. 第ⅦA族元素的陰離子還原性越強,其最高價氧化物的水化物的酸性越強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科研人員在蘭州合成了鏷元素的一種同位素鏷239,并測知其原子核內有148個中子。現有A元素的一種同位素,比鏷239的原子核內少54個質子和100個中子,則A元素在周期表中的位置是( )
A. 第三周期第IA族 B. 第四周期第IA族
C. 第五周期第IA族 D. 第二周期第IIA族
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com