
| A. | 元素非金屬性由強到弱的順序是:Z>Y>X | |
| B. | Y元素最高價氧化物對應水化物的化學式可表示為H4YO4 | |
| C. | 3種元素的氣態氫化物中,Z的氣態氫化物最穩定 | |
| D. | 原子半徑由大到小的順序為 Z>Y>X |
分析 X、Y、Z是3種短周期元素,X原子的最外層電子數是其電子層數的3倍,則X有2個電子層,最外層電子數為6,故X為氧元素;X、Y位于同一族,故Y為硫元素;Y、Z處于同一周期,Z原子的核外電子數比Y少1,則Z原子的核外電子數為15,故Z為磷元素,結合元素周期律解答.
解答 解:X、Y、Z是3種短周期元素,X原子的最外層電子數是其電子層數的3倍,則X有2個電子層,最外層電子數為6,故X為氧元素;X、Y位于同一族,故Y為硫元素;Y、Z處于同一周期,Z原子的核外電子數比Y少1,則Z原子的核外電子數為15,故Z為磷元素.
A.同周期自左而右非金屬性增強,同主族自上而下非金屬性減弱,所以非金屬性P<S<O,即Z<Y<X,故A錯誤;
B.Y為硫元素,最高價氧化物對應水化物的化學式可表示為H2SO4,故B錯誤;
C.非金屬性P<S<O,非金屬性越強,氫化物越穩定,所以氫化物穩定性Z<Y<X,故C錯誤;
D.同周期自左而右原子半徑減小,同主族自上而下原子半徑增大,所以原子半徑P>S>O,即Z>Y>X,故D正確,
故選D.
點評 本題考查結構與位置關系、元素周期律等,難度不大,推斷元素是關鍵,突破口為X原子的最外層電子數是其電子層數的3倍,注意對元素周期律的掌握.


 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
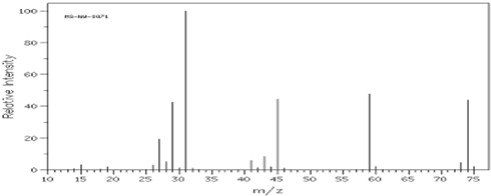
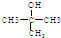 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液的pH值可能是5 | B. | 此溶液不存在 | ||
| C. | 該溶液的pH值一定是9 | D. | 該溶液的pH值可能是7 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

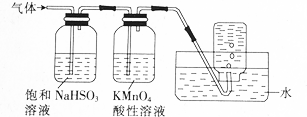
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2CO3固體 | B. | 水 | C. | 硫酸鉀固體 | D. | NaOH固體 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com