
| 元素 | A | B | C |
| 結構信息 | 基態原子核外有兩個電子層,最外層有3個未成對的電子 | 基態原子的M層有1對成對的p電子 | 基態原子核外電子排布為[Ar]3s104sx,有+1、+2兩種常見化合價 |
分析 A的基態原子核外有兩個電子層,最外層有3個未成對的電子,得到A的基態電子排布式1s22s22p3,為N元素;B基態原子的M層有1對成對的p電子,即有兩個未成對的電子得到B原子的基態電子排布式為:1s22s22p63s23p4,為S元素;C態原子核外電子排布為[Ar]3s104sx,有+1、+2兩種常見化合價,說明最外層有1或2個電子,如為2,則為Zn,但化合價只有+2價,則應為[Ar]3d104s1,即Cu元素,
(1)B基態原子的M層有1對成對的p電子,即有兩個未成對的電子,則電子數為16;
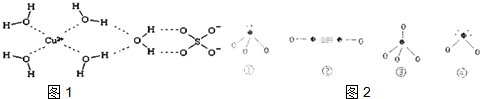
(2)在氨水中,由于N和O的非金屬性較強,可形成氫鍵;N的氫化物分子結合一個H+形成陽離子后,為正四面體結構,鍵角變大;
(3)硫酸銅溶液中逐滴加入過量氨水溶液,生成的配合物為[Cu(NH3)4]SO4;
(4)根據膽礬晶體的結構圖可知,在晶體中水分子與銅離子之間是配位鍵,氫氧之間是極性共價鍵,硫酸根和銅離子之間為離子鍵,水分子與水分子之間有氫鍵;
(5)①為氨氣②為乙炔③為甲烷,④為水.
解答 解:A的基態原子核外有兩個電子層,最外層有3個未成對的電子,得到A的基態電子排布式1s22s22p3,為N元素;B基態原子的M層有1對成對的p電子,即有兩個未成對的電子得到B原子的基態電子排布式為:1s22s22p63s23p4,為S元素;C態原子核外電子排布為[Ar]3s104sx,有+1、+2兩種常見化合價,說明最外層有1或2個電子,如為2,則為Zn,但化合價只有+2價,則應為[Ar]3d104s1,即Cu元素,
(1)B基態原子的M層有1對成對的p電子,即有兩個未成對的電子得到B原子的基態電子排布式為:1s22s22p63s23p4,
故答案為:1s22s22p63s23p4;
(2)在氨水中,由于N和O的非金屬性較強,可形成氫鍵,溶液中存在的氫鍵有:N-H…N-或N-H…O-或 O-H…N-或O-H…O-等,N的氫化物分子結合一個H+形成陽離子后,為正四面體結構,鍵角變大,
故答案為:N-H…N-或N-H…O-或 O-H…N-或O-H…O-;變大;
(3)硫酸銅溶液中逐滴加入過量氨水溶液,生成的配合物為[Cu(NH3)4]SO4;
故答案為:[Cu(NH3)4]SO4;
(4)根據膽礬晶體的結構圖可知,在晶體中水分子與銅離子之間是配位鍵,氫氧之間是極性共價鍵,硫酸根和銅離子之間為離子鍵,水分子與水分子之間有氫鍵,
故答案為:ABCE;
(5)①為氨氣②為乙炔③為甲烷,④為水,其中氨氣、甲烷和水的中心原子均以sp3雜化形成化學鍵;
故答案為:①③④.
點評 本題綜合考查物質結構與性質知識,題目涉及電子排布式、氫鍵、配位鍵以及雜化類型等知識,難度中等,注意氫鍵的形成特點和配位鍵的形成.


科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳-12的原子符號:12 6C | |
| B. | 次氯酸分子的結構式:H-O-Cl | |
| C. | 硫離子的電子排布式為:1s22s22p63s23p6 | |
| D. | 二氧化硅的分子式:SiO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
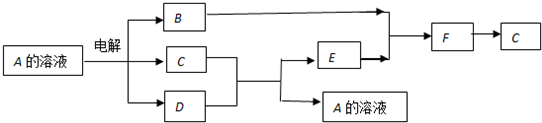
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
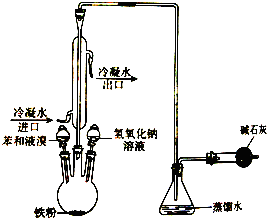 如圖是實驗室制取溴苯的裝置圖,請回答下列問題:
如圖是實驗室制取溴苯的裝置圖,請回答下列問題:
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
 ,B 同周期第一電離能最小的主族元素,C的最外層有三個成單電子,E的外圍電子排布式為3d64s2.回答下列問題:
,B 同周期第一電離能最小的主族元素,C的最外層有三個成單電子,E的外圍電子排布式為3d64s2.回答下列問題: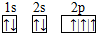 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
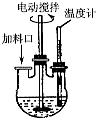 實驗室制取高純NaI晶體(無色)可按下列步驟進行:按化學計量稱取各原料,在三頸燒瓶中(如圖)先加入適量的高純水,然后按Na2CO3、I2和水合肼的投料順序分批加入.
實驗室制取高純NaI晶體(無色)可按下列步驟進行:按化學計量稱取各原料,在三頸燒瓶中(如圖)先加入適量的高純水,然后按Na2CO3、I2和水合肼的投料順序分批加入.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com