
第四周期的Cr、Fe、Co、Ni、Cu、Zn等許多金屬能形成配合物。
(1)Cr3+的核外電子排布式為____________________, 配離子[Cr(H2O)6] 3+中,與Cr3+形成配位鍵的原子是________(填元素符號)。
(2)NH3是一種很好的配體,氨分子是____________(填“極性”或“非極性”)分子,NH3的沸點_____________(填“高于”、“等于”或“低于”)AsH3。
(3)科學家通過X-射線測得膽礬(CuSO4·5H2O)的結構示意圖可簡單表示如下:
圖中虛線表示的作用力為_______________________;

(4)膽礬溶液與氨水在一定條件下可以生成Cu(NH3)4SO4·H2O晶體。在Cu(NH3)4SO4·H2O晶體中,[Cu(NH3)4]2+為平面正方形結構,呈正四面體結構的原子團是_________,其中心原子的雜化類型是______。
(5)金屬鎳粉在CO氣流中輕微加熱,生成無色揮發性液態Ni(CO)4,呈正四面體構型。Ni(CO)4易溶于_________(填標號)。
A.水 B.四氯化碳 C.苯 D.硫酸鎳溶液
科目:高中化學 來源:2017屆吉林省高三第五次摸底考試理綜化學試卷(解析版) 題型:選擇題
化學與生活密切相關。下列有關說法錯誤的是
A. SO2和NO2是主要的大氣污染物
B. 大氣中的SO2和CO2溶于水形成酸雨
C. 以液化石油氣代替燃油可減少大氣污染
D. 對煤燃燒后形成的煙氣脫硫,目前主要用石灰法
查看答案和解析>>
科目:高中化學 來源:2017屆山東省濟南市高三第一次模擬考試理科綜合化學試卷(解析版) 題型:簡答題
近年我國汽車擁有量呈較快增長趨勢,汽車尾氣已成為重要的空氣污染物。回答下列問題:
(l)汽車發動機工作時會引起反應:N2(g)+O2(g) 2NO(g),是導致汽車尾氣中含有NO的原因之一。2000K時,向容積為2L的密閉容器中充入2molN2與2molO2,發生上述反應,經過5min達到平衡,此時容器內NO的體積分數為0.75% .則該反應在5min內的平均反應速率v(O2)=_______mol/(Lmin),N2的平衡轉化率為_______,2000K時該反應的平衡常數K=_____。
2NO(g),是導致汽車尾氣中含有NO的原因之一。2000K時,向容積為2L的密閉容器中充入2molN2與2molO2,發生上述反應,經過5min達到平衡,此時容器內NO的體積分數為0.75% .則該反應在5min內的平均反應速率v(O2)=_______mol/(Lmin),N2的平衡轉化率為_______,2000K時該反應的平衡常數K=_____。
(2)一定量NO發生分解的過程中,NO的轉化率隨時間變化的關系如右圖所示。

① 反應2NO(g) N2(g)+O2(g)為______反應(填“吸熱”或“放熱”) ;
N2(g)+O2(g)為______反應(填“吸熱”或“放熱”) ;
②一定溫度下,能夠說明反應2NO(g) N2(g)+O2(g)已達到平衡的是_____(填序號);
N2(g)+O2(g)已達到平衡的是_____(填序號);
a.容器內的壓強不發生變化
b.混合氣體的密度不發生變化
c. 2NO、N2、O2的濃度保持不變
d.單位時間內分解4molNO,同時生成2molN2
③ 在四個容積和溫度均完全相同的密閉容器中分別加入下列物質,相應物質的量(mol)如下表所示。相同條件下達到平衡后,N2的體積分數最大的是_______(填容器代號);
容器代號 | NO | N2 | O2 |
A | 2 | 0 | 0 |
B | 0 | l | l |
C | 0.4 | 0.6 | 0.8 |
D | l | 0.5 | 0.4 |
(3)當發動機采用稀薄燃燒時,尾氣中的主要污染物為NOx。可用CH4催化還原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ·mol-1
①寫出CH4與NO反應生成N2、CO2、H2O(g)的熱化學方程式:___________;
②使用催化劑可以將汽車尾氣的主要有害成分一氧化碳(CO)和氮氧化物(NOx)轉化為無毒氣體,該反應的化學方程式為___________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省南昌市高一下學期第一次月考化學試卷(解析版) 題型:選擇題
下圖是部分短周期元素化合價與原子序數的關系圖,下列說法正確的是
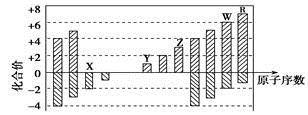
A. 原子半徑:Z>Y>X
B. 氣態氫化物的穩定性:R<W
C. WX3和水反應形成的化合物是離子化合物
D. Y和Z兩者最高價氧化物對應的水化物能相互反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省南昌市高一下學期第一次月考化學試卷(解析版) 題型:選擇題
某核素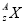 可形成 HmX型氫化物,則 a g HmX 含有
可形成 HmX型氫化物,則 a g HmX 含有
A.  HmX B.
HmX B. 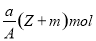 電子
電子
C. 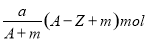 中子 D.
中子 D.  質子
質子
查看答案和解析>>
科目:高中化學 來源:寧夏勤行校區2016-2017學年高二下學期第一次(3月)月考化學試卷 題型:選擇題
下列敘述與范德華力無關的是( )
A. 氣體物質加壓或降溫時能凝結或凝固
B. 通常狀況下氯化氫為氣體
C. 氟、氯、溴、碘單質的熔、沸點依次升高
D. 氟、氯、溴、碘的氣態氫化物的穩定性越來越弱
查看答案和解析>>
科目:高中化學 來源:寧夏勤行校區2016-2017學年高二下學期第一次(3月)月考化學試卷 題型:選擇題
下列離子的VSEPR模型與其立體構型一致的是( )
A. SO B. ClO
B. ClO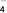 C. NO
C. NO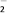 D. ClO
D. ClO
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省大同市高二3月月考化學試卷(解析版) 題型:簡答題
(I)(1)以下列出的是一些原子的2p能級和3d能級中電子排布的情況,試判斷哪些違反了泡利原理____________,哪些違反了洪特規則_______________。哪些既沒有違反泡利原理又沒有違反洪特規則_______________。

(Ⅱ)等電子原理:原子數相同、最外層電子總數相同的分子互稱為等電子體。等電子體的結構相似、物理性質相近。
(1)根據上述原理,僅由第二周期元素組成的分子中,互為等電子體的是:______和______;______和______.
(2)此后,等電子原理又有所發展.例如,由短周期元素組成的粒子,只要其原子數相同,各原子最外層電子數之和相同,也可互稱為等電子體,它們也具有相似的結構特征.在短周期元素組成的物質中,與NO2-互為等電子體的分子有:______、______.
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南師范大學附屬中學高一下學期第一次階段性測試化學試卷(解析版) 題型:填空題
已知A、B、C、D分別是中學化學中常見的四種不同粒子,它們之間有如下圖所示反應關系:

(1)如果A、B、C、D均是1O電子的粒子。請寫出A的電子式:______,D的結構式:_____。
(2)如果A、C均是18電子的粒子,B、D均是10電子的粒子。A與B在溶液中反應生成C和D的離子方程式為_______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com