
| A. | 常溫下,0.1mol Fe與酸完全反應時,失去的電子數一定為0.3NA | |
| B. | 0.1mol/L的 CaCl2溶液中所含Cl-數為0.2NA | |
| C. | 7.8g Na2O2與足量水反應,轉移電子數為0.2NA | |
| D. | 常溫常壓下,8g CH4含有的分子數為0.5NA |
分析 A、根據鐵與酸反應后可能變?yōu)?2價也可能變?yōu)?3價來分析;
B、溶液體積不明確;
C、求出過氧化鈉的物質的量,然后根據過氧化鈉與水的反應為歧化反應來分析;
D、分子個數N=$\frac{m}{M}{N}_{A}$.
解答 解:A、由于鐵與酸反應后可能變?yōu)?2價也可能變?yōu)?3價,故0.1mol鐵與酸反應后,失去的電子數不一定為0.3NA,還可能為0.2NA個,故A錯誤;
B、溶液體積不明確,故溶液中的氯離子的個數無法計算,故B錯誤;
C、7.8g過氧化鈉的物質的量為0.1mol,而過氧化鈉與水的反應為歧化反應,氧元素的價態(tài)由-1價變?yōu)?價,故0.1mol過氧化鈉轉移0.1mol電子即0.1NA個,故C錯誤;
D、分子個數N=$\frac{m}{M}{N}_{A}$=$\frac{8g}{16g/mol}{N}_{A}/mol$=0.5NA個,故D正確.
故選D.
點評 本題考查了阿伏伽德羅常數的有關計算,掌握物質的量的計算公式和物質結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液中一定不含K+、NH4+、A13+、SiO32- | |
| B. | 該溶液中一定含有A13+、CO32-、Cl- | |
| C. | 該溶液中可能含有Cl- | |
| D. | 該溶液中一定含有K+、AlO2-、CO32-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 質量相等的N2和C2H4 | B. | 等體積的CO和CO2 | ||
| C. | 等溫等體積的O2和N2 | D. | 等壓等體積的N2和CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu與Cu2O的物質的量之比為2:1 | |
| B. | 沉淀為氫氧化銅 | |
| C. | 產生的NO在標準狀況下的體積為4.48 L | |
| D. | Cu、Cu2O與硝酸恰好完全反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
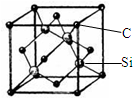 銅、鎵、硒、硅等元素的化合物是生產第三代太陽能電池的重要材料.請回答:
銅、鎵、硒、硅等元素的化合物是生產第三代太陽能電池的重要材料.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 若反應中轉移的電子為n mol,則0.15<n<0.25 | |
| B. | n(Na+):n(Cl-) 可能為7:3 | |
| C. | 與NaOH反應的氯氣一定為0.15 mol | |
| D. | n(NaCl):n(NaClO):n(NaClO3)可能為11:2:1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com