
| A. | 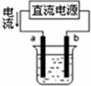 用如圖裝置精煉銅,a極為粗銅,b為精銅,電解質溶液為CuSO4溶液 | |
| B. | 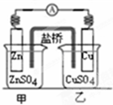 如圖裝置的鹽橋中KCl的Cl-移向乙燒杯 | |
| C. |  如圖裝置中鋼閘門應與外接電源的負極相連獲得保護 | |
| D. | 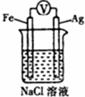 裝置中滴入2滴黃色K3[Fe(CN)6]溶液,溶液中可能出現藍色沉淀 |
分析 A.電解精煉銅,粗銅做陽極,精銅做陰極;
B.鹽橋是起到平衡電解質液的電荷守恒,甲池中鋅離子增多,氯離子移向甲池;
C.電解陰極被保護;
D.形成原電池反應,為鐵的吸氧腐蝕裝置.
解答 解:A.電解精煉銅,粗銅做陽極,精銅做陰極,用圖裝置精煉銅,電流從電源正極流出,則a與正極相連是電解池的陽極,a極為粗銅,電解質溶液為CuSO4溶液,故A正確;
B.鹽橋是起到平衡電解質液的電荷守恒,甲池中鋅離子增多,氯離子移向甲池;裝置鹽橋中KCl的Cl-移向甲燒杯,故B錯誤;
C.裝置中鋼閘門應與外接電源的負極相連獲得保護,電解陰極被保護,故C正確;
D.形成原電池反應,鐵為負極,被氧化生成亞鐵離子,滴入2滴黃色K3[Fe(CN)6]溶液,溶液中出現藍色沉淀,故D正確.
故選B.
點評 本題考查了原電池和電解池的工作原理應用,主要考查電解精煉銅、原電池鹽橋作用,電解陰極保護的原理,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 10mol氧約含有6.02×1024個氧分子 | |
| B. | NA 約等于6.02×1023 | |
| C. | 摩爾是國際科學界廣泛使用的一種物理量 | |
| D. | 摩爾是物質的量的單位,簡稱摩,符號為mol |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 以NaCl等為原料制備KClO4的過程如下:
以NaCl等為原料制備KClO4的過程如下:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com