
在如圖所示的有關物質轉化關系中,各物質均是我們中學化學所學的物質。C為一種黑色粉末,D為一種氣體。
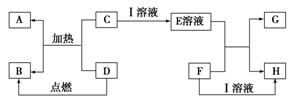
請根據框圖中物質的轉化關系及相關信息,用化學式填寫下列空白:
(1)若F為可溶性堿,G為藍色沉淀,則A為_________________;D可能為__________________。
(2)若G為藍色沉淀,H為難溶性鹽,則I為_________________。
(3)若G、H都屬于鹽,且G為藍色溶液,則I可能為______________;F可能為_____________。
 課前課后同步練習系列答案
課前課后同步練習系列答案 課堂小作業系列答案
課堂小作業系列答案 黃岡小狀元口算速算練習冊系列答案
黃岡小狀元口算速算練習冊系列答案 成功訓練計劃系列答案
成功訓練計劃系列答案 倍速訓練法直通中考考點系列答案
倍速訓練法直通中考考點系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作業本系列答案
名校作業本系列答案科目:高中化學 來源:2016屆山東省高三上10月階段質檢化學試卷(解析版) 題型:選擇題
在1.0L密閉容器中放入0.10 mol X,在一定溫度下發生反應:X(g) Y(g)+Z(g)△H<0容器內氣體總壓強p隨反應時間t的變化關系如下圖所示.以下分析正確的是
Y(g)+Z(g)△H<0容器內氣體總壓強p隨反應時間t的變化關系如下圖所示.以下分析正確的是
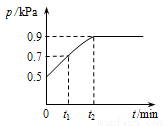
A.從反應開始到t1時的平均反應速率v(X)=0.2/t1mol/(L•min)
B.該溫度下此反應的平衡常數K=0.32mol/L
C.欲提高平衡體系中Y的含量,可升高體系溫度或減少Z的量
D.其他條件不變,再充入0.1 mol 氣體X,平衡正向移動,X的轉化率增大
查看答案和解析>>
科目:高中化學 來源:2016屆湖北省高三上學期10月調考理綜化學試卷(解析版) 題型:填空題
(15分)燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺顆粒物)污染也跟冬季燃煤密切相關。SO2、CO、CO2也是對環境影響較大的氣體,對它們的合理控制、利用是優化我們生存環境的有效途徑。
(1)如圖所示,利用電化學原理將SO2 轉化為重要化工原料C
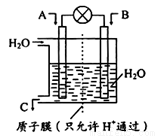
若A為SO2,B為O2,則負極的電極反應式為:________________________;
(2)有一種用CO2生產甲醇燃料的方法:CO2+3H2 CH3OH+H2O
CH3OH+H2O
已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
CH3OH(g)+H2O(g)△H=-a kJ·mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-b kJ·mol-1;
H2O(g)=H2O(l)△H=-c kJ·mol-1;
CH3OH(g)=CH3OH(l)△H=-d kJ·mol-1,
則表示CH3OH(l)燃燒熱的熱化學方程式為:____________________________;
(3)光氣 (COCl2)是一種重要的化工原料,用于農藥、醫藥、聚酯類材料的生產,工業上通過Cl2(g)+CO(g)
 COCl2(g)制備。左圖為此反應的反應速率隨溫度變化的曲線,右圖為某次模擬實驗研究過程中容器內各物質的濃度隨時間變化的曲線。回答下列問題:
COCl2(g)制備。左圖為此反應的反應速率隨溫度變化的曲線,右圖為某次模擬實驗研究過程中容器內各物質的濃度隨時間變化的曲線。回答下列問題:
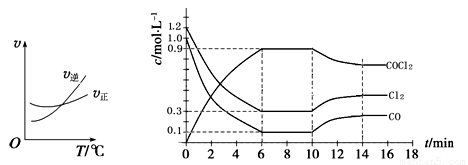
① 0~6 min內,反應的平均速率v(Cl2)= ;
② 若保持溫度不變,在第7 min 向體系中加入這三種物質各2 mol,則平衡 移動(填“向正反應方向”、“向逆反應方向”或“不”);
③ 若將初始投料濃度變為c(Cl2)=0.7 mol/L、c(CO)=0.5 mol/L、c(COCl2)= mol/L,保持反 應溫度不變,則最終達到化學平衡時,Cl2的體積分數與上述第6 min時Cl2的體積分數相同;
④ 隨溫度升高,該反應平衡常數變化的趨勢是 ;(填“增大”、“減小”或“不變”)
⑤比較第8 min反應溫度T(8)與第15 min反應溫度T(15)的高低:T(8)______________T(15)(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化學 來源:2016屆福建省莆田市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
為了證明硫酸亞鐵銨[(NH4)2Fe(SO4)·26H2O]晶體的成分中含有NH4+、Fe2+、SO42-和H2O,下列實驗敘述中不正確的是
A.取少量硫酸亞鐵銨晶體放入試管中,加熱,試管口有液體生成,則可證明晶體的成分中含有結晶水
B.取少量硫酸亞鐵銨晶體放入試管,加濃NaOH溶液,加熱,試管口濕潤的藍色石蕊試紙變紅,則可證明晶體的成分中含有NH4+
C.取適量硫酸亞鐵銨晶體溶于水,加少量稀鹽酸,無現象,再滴入幾滴BaCl2溶液,有白色沉淀生成,則可證明晶體的成分中含有SO42-
D.取適量硫酸亞鐵銨晶體溶于水,得淺綠色溶液,滴入2滴KSCN溶液,溶液不顯血紅色,再滴入幾滴新制氯水,溶液變為血紅色,則可證明晶體的成分中含有Fe2+
查看答案和解析>>
科目:高中化學 來源:2016屆甘肅省高三上學期第二次檢測化學試卷(解析版) 題型:填空題
【化學與技術】鈦鐵礦的主要成分可表示為FeTiO3(Ti 為+4 價),某鈦鐵礦中含FeTiO3 為76%。鈦白粉在涂料、塑料、油墨、造紙等行業具有廣泛的用途,鈦白粉的主要成分為TiO2。利用該鈦鐵礦生產鈦白粉及綠礬的工藝流程如下:
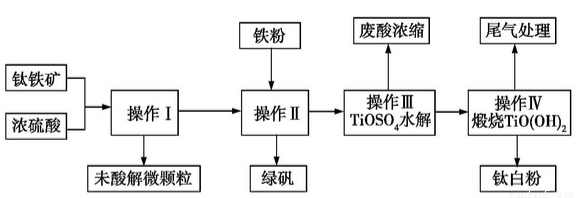
(1)若鈦鐵礦與濃硫酸反應時Ti 的轉化率為92%,操作Ⅰ~Ⅳ中Ti 的轉化率均為96%,則1t 該礦石可生產鈦白粉(TiO2) t (計算結果保留兩位小數,下同),能否計算生成的綠礬(FeSO4·7H2O)的質量? (能則寫出計算結果,不能則說明理由)。
(2)鈦鐵礦與硫酸的反應可表示為FeTiO3+H2SO4 →TiOSO4+X+H2O(未配平)。其中X的化學式為 。
(3)操作Ⅰ的名稱是 ,操作Ⅱ包括冷卻結晶、 。操作Ⅱ中加入鐵粉的目的是 (用離子方程式表示)。
(4)寫出操作Ⅲ中TiOSO4水解的化學方程式: 。
查看答案和解析>>
科目:高中化學 來源:2016屆江西省高三上學期第一次月考化學試卷(解析版) 題型:選擇題
下列各組分類中正確的是
A.同位素:1H、D+、T2
B.電解質:H2O、CH3COOH、NH4HCO3
C.膠體:飽和氯化鐵溶液、淀粉溶液、蛋白質溶液
D.硅酸鹽產品:晶體硅、水泥、陶瓷
查看答案和解析>>
科目:高中化學 來源:2016屆上海市高三上學期摸底測試化學試卷(解析版) 題型:填空題
有機推斷題(共6分)
有一烴A,能發生如下圖所示的一系列轉化:

已知兩個E分子間可發生縮合反應生成環狀化合物C6H8O4,試解答下列問題:
1.寫出A和E的結構簡式_____________、______________
2.在反應①—⑦屬于取代反應的有______________________
寫出下列反應的化學方程式:
反應①_________________________
反應④_________________________
反應⑦_________________________
查看答案和解析>>
科目:高中化學 來源:2016屆江西省南昌市高三上學期第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
①非金屬氧化物一定是酸性氧化物
②依據丁達爾現象可將分散系分為溶液、膠體與濁液
③利用金屬鈉可區分乙醇和乙醚
④堿性氧化物一定是金屬氧化物
⑤某鉀鹽溶于鹽酸,產生能使澄清石灰水變渾濁的無色無味氣體,說明該鉀鹽是K2CO3
⑥欲配制1L1.00mol/L的KCl溶液,可將74.5gKCl溶于1L水中
⑦質子數、中子數和電子數都相同的粒子一定是同一種粒子。
A.全部 B.①②③④⑦ C.①②④ D.③④
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高一上第一次月考化學試卷(解析版) 題型:選擇題
將0.5L 1mol/L FeCl3溶液加水稀釋至1L ,所得溶液中氯離子的物質的量濃度是
A.3mol/L B.2mol/L C.1mol/L D.1.5mol/L
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com